Цирроз печени с гиперспленизмом
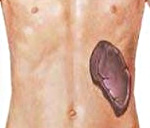
Гиперспленизм – это патологическое состояние, характеризующееся усиленной деструкцией в синусоидах селезенки форменных элементов крови (эритроцитов, тромбоцитов, лейкоцитов). Является следствием увеличения селезенки. Клиническая картина определяется основным заболеванием, а также цитопеническим синдромом – анемия, кровотечения, инфекции. Диагноз ставится по наличию спленомегалии, данным УЗИ или КТ брюшной полости, лабораторного подтверждения снижения одного из типов клеток крови. Лечение зависит от болезни, вызвавшей гиперспленизм. При крайне выраженной цитопении проводится спленэктомия (удаление селезенки).
Общие сведения
Гиперспленизм – не самостоятельное заболевание, а клинико-лабораторный синдром, который является специфическим закономерным осложнением длительной спленомегалии. Однако иногда он может развиться и при нормальных размерах селезенки. В норме селезенка служит своеобразным фильтром, в котором задерживаются и разрушаются клетки крови, перестающие выполнять свои функции, или же аномальные клетки. При гиперспленизме этот процесс приобретает патологический характер. Его возникновение свидетельствует о неблагоприятном течении основного заболевания, так как синдром часто ассоциирован с летальным исходом.
Гиперспленизм
Причины гиперспленизма
Этиологические факторы аномально повышенной функции селезенки те же, что и у спленомегалии. Однако у некоторых пациентов не удается точно установить причину (первичный, идиопатический гиперспленизм). Вторичный процесс развивается на фоне различных патологических состояний. Наиболее распространенными из них считаются:
- Цирроз печени. Признаки гиперспленизма наблюдаются у 60% больных хроническими болезнями печени. Самая частая причина — цирроз. В этом случае синдром является компонентом портальной гипертензии и сопровождается асцитом, варикозным расширением вен пищевода и симптомами печеночной недостаточности.
- Гематологические заболевания. Это вторая по частоте причина гиперспленизма. Особенно ярко синдром выражен при гемоглобинопатиях (серповидно-клеточной анемии, талассемиях). Также гиперфункция селезенки встречается при миелопролиферативных, лимфопролиферативных патологиях (лейкозах, лимфомах), гемолитических анемиях.
- Инфекции. Спленомегалия, осложненная гиперспленизмом, довольно часто встречается при инфекционном эндокардите. Гиперфункция селезенки может наблюдаться при вирусных (инфекционный мононуклеоз), бактериальных (брюшной тиф, бруцеллез) и протозойных инфекциях (малярия, висцеральный лейшманиоз).
- Системные заболевания. Гиперспленизм также нередко развивается при системных воспалительных патологиях (саркоидоз, системная красная волчанка), метаболических расстройствах (амилоидоз, гемохроматоз). Наиболее тяжело синдром протекает у людей, страдающих наследственными болезнями накопления (болезнь Гоше, Нимана-Пика).
Патогенез
Механизм развития усиленного разрушения клеток крови (секвестрации) в селезенке напрямую зависит от патогенеза спленомегалии, а значит, и от основного заболевания. При циррозе печени, гемоглобинопатиях, а также некоторых инфекциях (бактериальном эндокардите), возникает застой крови в системе воротной или селезеночной вены, что ведет к переполнению селезенки кровью. Из-за того, что через селезенку проходит больший объем крови, секвестрация форменных элементов усиливается.
При инфекциях и системных воспалительных процессах гиперспленизм обусловлен гиперактивацией ретикулоэндотелиальной системы селезенки. В результате селезеночные макрофаги захватывают клетки крови в большем, чем обычно, количестве. Данный процесс носит название «рабочая гипертрофия (гиперплазия) селезенки». При болезнях накопления и злокачественных гематологических заболеваниях селезенка увеличивается за счет опухолевой пролиферации и отложения в ней патологических белков, липидов и т. д.
На ранних этапах развития гиперспленизма главного патологического компонента — цитопенического синдрома — может не быть. Это связано с компенсаторным усилением гемопоэтической функции костного мозга. Однако при дальнейшем прогрессировании основного заболевания и гиперспленизма этого механизма становится недостаточно, что приводит к уменьшению содержания клеток в периферической крови.
Симптомы гиперспленизма
Клиническая картина складывается из признаков спленомегалии, цитопенического синдрома и симптомов основного заболевания. Увеличенная селезенка вызывает тяжесть, ноющие или распирающие боли в левом подреберье. При многих патологиях спленомегалия сопровождается гепатомегалией, что проявляется тяжестью и болями в правом подреберье. Иногда селезенка достигает таких размеров, что сдавливает диафрагму, и больной начинает испытывать затруднения дыхания (невозможность совершить глубокий вдох) из-за уменьшенной амплитуды экскурсии грудной клетки. Особенно часто одышка наблюдается у пациентов с болезнями накопления и миелопролиферативными заболеваниями.
Цитопенический синдром заключается в уменьшении содержания в крови форменных элементов. Может встречаться как изолированное снижение одного типа клеток, так и всех трех (панцитопения). Клиника зависит от того, дефицит каких клеток крови наступает у пациента:
Анемический синдром
Низкий уровень эритроцитов приводит к анемическому синдрому – кожа и слизистые оболочки становятся бледными, появляется повышенная чувствительность к холоду. В дальнейшем присоединяются симптомы сниженного артериального давления (слабость, головокружения, учащенное сердцебиение).
Геморрагический синдром
Падение концентрации тромбоцитов в крови вызывает геморрагический синдром. Возникают носовые кровотечения, кровоточивость десен. У женщин менструации становятся обильными и продолжительными. Кожа покрывается петехиальными высыпаниями, экхимозами, как спонтанно, так и при малейшем механическом повреждении.
Лейкопенический синдром
Из-за снижения содержания лейкоцитов, а именно гранулоцитов, уменьшается сопротивление организма различным бактериальным инфекциям. На коже часто появляются гнойничковые образования (фурункулы, карбункулы). Развиваются постоянно рецидивирующие воспалительные инфекционные процессы ‒ пневмонии, пиелонефриты, отиты.
Осложнения
Гиперспленизм характеризуется большим количеством осложнений. Наиболее частые неблагоприятные последствия связаны с тромбоцитопенией. Развиваются обширные внутренние кровотечения. Самое опасное из них – геморрагический инсульт, имеющий высокий процент летальности (около 30%). Выраженная быстропрогрессирующая анемия приводит к декомпенсации хронической сердечной недостаточности (отек легких, кардиогенный шок), усугублению ишемической болезни сердца в виде нестабильной стенокардии и инфаркта миокарда. Вследствие гранулоцитопении инфекционные заболевания приобретают тяжелое молниеносное течение, стремительно переходящее в септическое состояние и септический шок.
Диагностика
Профиль специалиста, который курирует пациента с гиперспленизмом, определяется основной патологией. Главным образом, такими больными занимаются врачи-гепатологи и гематологи, так как наиболее частыми этиологическими факторами выступают цирроз печени и гематологические болезни. Во время общего осмотра обращает на себя внимание увеличенная и болезненная при пальпации селезенка. Дополнительное обследование включает:
- Анализы крови. Основное лабораторное исследование для диагностики гиперспленизма – это клинический анализ крови. Отмечаются снижение показателей эритроцитов, тромбоцитов, гранулоцитарных лейкоцитов (нейтрофилов). Обычно эритроцитопения намного выраженнее тромбоцитопении и нейтропении. Характерен ретикулоцитоз.
- Инструментальные исследования. Главный визуализирующий метод – это УЗИ органов брюшной полости. Обнаруживается увеличенная селезенка с диффузными изменениями, нередко увеличена печень. Иногда селезенка может сохранять нормальные размеры. Для более детального изучения структуры селезенки применяется КТ.
- Биопсия. В редких случаях, когда требуется выявить скрытый гиперспленизм или отдифференцировать причины цитопенического синдрома, прибегают к стернальной пункции или трепанобиопсии для получения образца костного мозга. При микроскопии отмечается гиперплазия ростков костного мозга – гранулоцитарного, эритроцитарного, мегакариоцитарного.
Дифференциальная диагностика гиперспленизма осуществляется с учетом компонента цитопенического синдрома. Эритроцитопению нужно отличать от других видов анемий (железодефицитных, при хронических заболеваниях). При тромбоцитопении необходимо дифференцировать гиперспленизм от других геморрагических диатезов, обусловленных низким уровнем тромбоцитов (иммунной тромбоцитопении, тромбоцитопенической пурпуры). Развитие панцитопении требует исключения апластической анемии, выраженного дефицита цианкобаламина (витамина В12).
Лечение гиперспленизма
Пациенты подлежат обязательной госпитализации в стационарное отделение (гематологии, гастроэнтерологии). Главным условием успешной терапии является лечение основного заболевания, на фоне которого возникло патологическое усиление секвестрационной функции селезенки – антицирротическая, антибактериальная терапия, химиотерапия и пр. Так как сам гиперспленизм характеризуется упорным прогрессирующим течением, лечение представляет собой тяжелую задачу. Для устранения проявлений синдрома используются различные способы.
Консервативная терапия
Лекарственных препаратов, позволяющих полностью избавиться от признаков гиперспленизма, не существует. Так как главную опасность для жизни представляет цитопенический синдром, используют меры по поддержанию клеток крови на должном уровне. В первую очередь, это переливания цельной крови или отдельных ее компонентов (размороженной, отмытой эритроцитарной массы, концентрата тромбоцитов).
Иногда назначают фармакологические препараты, воздействующие на отдельные ростки костного мозга – эритропоэтин, филграстим, тромбопоэтин. К этим медикаментам прибегают очень редко и только тогда, когда другие методы оказались безуспешными, т. к. костный мозг при гиперспленизме уже находится в состоянии гиперплазии. Поэтому дополнительное применение лекарственных стимуляторов гемопоэза патогенетически мало оправдано.
Хирургическое лечение
Наиболее радикальный способ лечения гиперспленизма, позволяющий добиться нормализации показателей клеток крови – спленэктомия (оперативное удаление селезенки). Однако эта операция сопряжена с большим числом осложнений — тромбозами, повышенной чувствительностью организма к таким бактериям, как пневмококк, менингококк, гемофильная палочка. В связи с этим в последнее время все чаще выполняются малоинвазивные эндоваскулярные вмешательства ‒ эмболизация селезеночной артерии или ее ветвей. Это позволяет устранить гиперспленизм и сохранить нормальную функцию селезенки.
Прогноз и профилактика
Выживаемость и частота неблагоприятных последствий зависит от основной патологии, вызвавшей гиперспленизм. Главная причина летального исхода – геморрагический инсульт, обширные кровотечения, септическое состояние. Первичная профилактика гиперспленизма заключается в своевременной диагностике и грамотном лечении основного заболевания. Пациенты, которым было проведено удаление селезенки, подлежат обязательной вакцинации против гемофильной палочки, менингококка, пневмококка. Дети до 6 лет, перенесшие спленэктомию, должны длительно получать профилактические дозы пенициллиновых антибиотиков.
Источник
Цирро́з пе́чени (др.-греч. κίρρως — рыжий, янтарный) — хроническое заболевание печени, сопровождающееся необратимым замещением паренхиматозной ткани печени фиброзной соединительной тканью, или стромой. Цирротичная печень увеличена или уменьшена в размерах, необычно плотная, бугристая, шероховатая. Десятилетняя смертность от постановки диагноза составляет 34-66%, в зависимости от причин: алкогольный цирроз имеет худший прогноз, чем связанный с другими причинами. Первое известное описание заболевания было за авторством Гиппократа в 5-м веке до нашей эры[2]. Сам термин «цирроз» был изобретен в 1819 году из-за желтоватого цвета больной печени.[3]
Эпидемиология[править | править код]
Годы жизни, скорректированные по нетрудоспособности пациентов с циррозом печени на 100 000 населения в 2004 году.[4]
Нет данных Менее 50 50—100 100—200 200—300 300—400 400—500 500—600 600—700 700—800 800—900 900—1000 Более 1000
В экономически развитых странах цирроз входит в число шести основных причин смерти пациентов от 35 до 60 лет, составляя 14—30 случаев на 100 тыс. населения. Ежегодно в мире умирают 40 млн человек[5] от вирусного цирроза печени и гепатоцеллюлярной карциномы, развивающейся на фоне носительства вируса гепатита B. В странах СНГ цирроз встречается у 1 % населения.
Чаще наблюдается у мужчин: соотношение мужчин и женщин составляет в среднем 3:1. Заболевание может развиться во всех возрастных группах, но чаще после 40 лет[6].
Этиология[править | править код]
Чаще цирроз развивается при длительной интоксикации алкоголем (по разным данным, от 40—50 % до 70—80 %) и на фоне вирусных гепатитов B, С и D (30—40 %) и паразитарных инфекций. Более редкие причины цирроза — болезни желчевыводящих путей (внутри- и внепечёночных), застойная сердечная недостаточность, различные химические (гепатотоксины) и лекарственные интоксикации. Цирроз может развиваться и при наследственных нарушениях обмена веществ (гемохроматоз, гепатолентикулярная дегенерация, недостаточность α1-антитрипсина) и окклюзионными процессами в системе воротной вены (флебопортальный цирроз). Среди инфекционных факторов: хронические вирусные гепатиты, особенно B и C и паразитарные инфекции, особенно грибковые и трематодозные (шистосомоз, описторхоз, кандидоз, аспергиллёз). Первичный билиарный цирроз печени возникает первично без видимой причины. Приблизительно у 10—35 % больных этиология остаётся неясной[6].
Патогенез[править | править код]
За многие месяцы и годы меняется геном гепатоцитов и создаются клоны патологически изменённых клеток. Вследствие этого развивается иммуновоспалительный процесс.
Выделяют следующие этапы патогенеза цирроза[7]:
- Действие этиологических факторов: цитопатогенное действие вирусов, иммунные механизмы, влияние гепатотоксичных цитокинов, хемокинов, прооксидантов, эйкозоноидов, ацетальдегида, железа, продуктов перекисного окисления липидов
- Активизация функции клеток Ито, что приводит к избыточному разрастанию соединительной ткани в пространствах Диссе и перицеллюлярному фиброзу печени
- Нарушение кровоснабжения паренхимы печени за счёт капилляризации синусоидов и уменьшения сосудистого русла с развитием ишемических некрозов гепатоцитов
- Активация иммунных механизмов цитолиза гепатоцитов
При мостовидном некрозе гепатоцитов в зону поражения стягиваются Т-лимфоциты, которые активизируют клетки Ито, приобретающие фибробластоподобные свойства: синтезируют коллаген I типа, что и ведёт в итоге к фиброзу. Кроме того, микроскопически в печёночной паренхиме образуются ложные дольки, не имеющие центральной вены.
Алкогольный цирроз печени. Этапы: острый алкогольный гепатит и жировая дистрофия печени с фиброзом и мезенхимальной реакцией. Важнейший фактор — некроз гепатоцитов, обусловленный прямым токсическим действием алкоголя, а также аутоиммунными процессами.
Вирусный цирроз печени. Важным фактором является сенсибилизация иммуноцитов к собственным тканям организма. Основной мишенью аутоиммунной реакции является печёночный липопротеид.
Застойный цирроз печени. Некроз гепатоцитов связан с гипоксией и венозным застоем.
Развивается портальная гипертензия — повышение давления в системе портальной вены, обусловленное обструкцией внутри- или внепечёночных портальных сосудов. Это приводит к появлению портокавального шунтирования крови, спленомегалии и асцита. Со спленомегалией связаны тромбоцитопения (усиленное депонирование тромбоцитов в селезёнке), лейкопения, а также анемия вследствие повышенного гемолиза эритроцитов. Асцит приводит к ограничению подвижности диафрагмы, гастроэзофагальному рефлюксу с пептическими эрозиями, язвами и кровотечениями из варикозно-расширенных вен пищевода, брюшным грыжам, бактериальному перитониту, гепаторенальному синдрому. У больных циррозом печени часто наблюдаются гепатогенные энцефалопатии.
Первичный билиарный цирроз печени. Основное место принадлежит генетическим нарушениям иммунорегуляции. Вначале происходит разрушение билиарного эпителия с последующим некрозом сегментов канальцев, а позднее — их пролиферация, что сопровождается нарушениями экскреции жёлчи. Стадии процесса следующие:
- хронический негнойный деструктивный холангит
- дуктулярная пролиферация с деструкцией жёлчных канальцев
- рубцевание и уменьшение жёлчных канальцев
- крупноузловой цирроз с холестазом
Патологоанатомическая картина первичного билиарного цирроза включает инфильтрацию эпителия лимфоцитами, плазматическими клетками, макрофагами[6].
Лабораторными исследованиями выявляются антимитохондриальные антитела (АМА), наиболее специфичны — М2-АМА, направленные против Е2-субъединицы пируватдегидрогеназы, повышение IgM в сыворотке. Помимо этого выявляются иммуноопосредованные внепечёночные проявления — тиреоидит Хашимото, синдром Шегрена, фиброзирующий альвеолит, тубулоинтерстициальный нефрит, целиакия, а также сочетание с заболеваниями ревматического круга — системной склеродермией, ревматоидным артритом, системной красной волчанкой[8].
Симптомы[править | править код]
Большинство внепечёночных симптомов обусловлено повышением давления в синусоидах, что ведёт к возрастанию давления в системе воротной вены. Портальная гипертензия. Также характерным симптомом является «голова медузы» — перенаполнение вен передней брюшной стенки.
Для цирроза характерны общие симптомы: слабость, пониженная трудоспособность, неприятные ощущения в животе, диспепсические расстройства, повышение температуры тела, боли в суставах, также отмечаются метеоризм, боль и чувство тяжести в верхней половине живота, похудение, астения. При осмотре выявляется увеличение печени, уплотнение и деформация её поверхности, заострение края. Сначала отмечается равномерное умеренное увеличение обеих долей печени, позднее как правило преобладает увеличение левой доли. Портальная гипертензия проявляется умеренным увеличением селезёнки.
Развёрнутая клиническая картина проявляется синдромами печёночно-клеточной недостаточности и портальной гипертензии. Имеют место вздутие живота, плохая переносимость жирной пищи и алкоголя, тошнота, рвота, диарея, чувство тяжести или боль в животе (преимущественно в правом подреберье). В 70 % случаев обнаруживается гепатомегалия, печень уплотнена, край заострён. У 30 % больных при пальпации выявляется узловатая поверхность печени. Спленомегалия у 50 % больных.
Субфебрильная температура, возможно, связана с прохождением через печень кишечных бактериальных пирогенов, которые она не в состоянии обезвредить. Лихорадка резистентна к антибиотикам и проходит только при улучшении функции печени.
Могут быть внешние признаки — пальмарная или плантарная эритема, сосудистые звёздочки, скудный волосяной покров в подмышечной области и на лобке, белые ногти, гинекомастия у мужчин вследствие гиперэстрогенемии. В ряде случаев пальцы приобретают вид «барабанных палочек».
В терминальной стадии болезни в 25 % случаев отмечается уменьшение размеров печени. Также возникают желтуха, асцит, периферические отёки из-за гипергидратации (прежде всего отёки ног), внешние венозные коллатерали (варикозно-расширенные вены пищевода, желудка, кишечника). Кровотечение из вен часто заканчивается летальным исходом. Реже возникают геморроидальные кровотечения, они менее интенсивны.
Энцефалопатия может быть следствием как печёночно-клеточной, так и портально-печёночной недостаточности[6].
Осложнения[править | править код]
- печёночная кома
- кровотечение из варикозно-расширенных вен пищевода
- тромбоз в системе воротной вены
- гепаторенальный синдром
- формирование рака печени — гепатоцеллюлярной карциномы
- инфекционные осложнения — пневмонии, «спонтанный» перитонит при асците, сепсис
Диагностика[править | править код]
Цирроз печени с уменьшением объёма органа. Компьютерная томография брюшной полости.
Характерно повышение активности АЛТ, АСТ, щелочной фосфатазы, лейкоцитоз. При гепатолиенальном синдроме может развиваться гиперспленизм, проявляющийся лейкопенией, тромбоцитопенией, анемией и увеличением клеточных элементов в костном мозге.
Расширенные и извитые венозные коллатерали выявляются при ангиографии, компьютерной томографии, ультразвуковом исследовании или в ходе оперативного вмешательства.
Классификация[править | править код]
Морфологическая классификация[править | править код]
Предложена Всемирной ассоциацией гепатологов (Акапулько, 1974) и ВОЗ (1978)[6].
- мелкоузловой, или мелконодулярный цирроз (диаметр узлов от 1 до 3 мм)
- крупноузловой, или макронодулярный цирроз (диаметр узлов более 3 мм)
- неполная септальная форма
- смешанная (при которой наблюдаются различные размеры узлов) форма
Этиологическая классификация[править | править код]
Различают следующие формы цирроза[6]:
- вирусный
- алкогольный
- лекарственный
- вторичный билиарный
- врождённый, при следующих заболеваниях:
- гепатолентикулярная дегенерация
- гемохроматоз
- дефицит α1-антитрипсина
- тирозиноз
- галактоземия
- гликогенозы
- застойный (недостаточность кровообращения)
- болезнь и синдром Бадда-Киари
- обменно-алиментарный, при следующих состояниях:
- наложение обходного тонкокишечного анастомоза
- ожирение
- тяжёлые формы сахарного диабета
- цирроз печени неясной этиологии
- криптогенный
- первичный билиарный
- индийский детский
Шкала оценки тяжести печёночной недостаточности по Чайлду — Пью[править | править код]
Функция печёночных клеток при циррозе печени оценивается по Чайльду — Пью[9][10].
| Параметр | Баллы | ||
|---|---|---|---|
| 1 | 2 | 3 | |
| Асцит | Нет | Мягкий, легко поддаётся лечению | Напряжённый, плохо поддаётся лечению |
| Энцефалопатия | Нет | Лёгкая (I—II) | Тяжёлая (III—IV) |
| Билирубин, мкмоль/л(мг%) | менее 34 (2,0) | 34—51 (2,0—3,0) | более 51 (3,0) |
| Альбумин, г/л | более 35 | 28—35 | менее 28 |
| ПТВ, (сек) или ПТИ (%) | 1—4 (более 60) | 4—6 (40—60) | более 6 (менее 40) |
Класс цирроза выставляется в зависимости от суммы баллов по всем параметрам. Сумма баллов 5—6 соответствует классу A, при сумме 7—9 — классу B, а при сумме в 10—15 баллов — классу C[6].
Ожидаемая продолжительность жизни у больных класса А составляет 15—20 лет, послеоперационная летальность при полостном хирургическом вмешательстве — 10 %. Класс В является показанием для рассмотрения вопроса о пересадке печени; при этом послеоперационная летальность при полостном хирургическом вмешательстве достигает 30 %. У больных класса С ожидаемая продолжительность жизни достигает 1—3 года, а послеоперационная летальность при полостном вмешательстве — 82 %. На основании критериев Чайлда — Пью предложено оценивать необходимость в трансплантации печени: высокая необходимость у больных, относящихся к классу С, умеренная — у больных класса В и низкая — у больных класса А[11].
Система критериев SAPS[править | править код]
В последние годы для определения прогноза у пациентов в момент развития желудочно-кишечного кровотечения, комы, сепсиса и других осложнений используется система критериев SAPS (Simplified Acute Physiology Score), включающая основные физиологические параметры[12]. В стратификации имеют значение: возраст, ЧСС, ЧДД, систолическое артериальное давление, температура тела, диурез, гематокрит, лейкоциты крови, мочевина, калий, натрий, и бикарбонаты плазмы, а также стадия печёночной комы[6].
Критерии оценки по системе SAPS
Критерий | Баллы | |||||||
4 | 3 | 2 | 1 | 1 | 2 | 3 | 4 | |
Возраст, годы | ≤45 | 46-55 | 56-65 | 66-75 | >75 | |||
ЧСС в минуту | ≥180 | 140—179 | 110—139 | 70-109 | 55-69 | 40-54 | <40 | |
Систолическое артериальное давление, мм рт. ст. | ≥190 | 150—189 | 80-149 | 55-79 | <55 | |||
Температура тела, ºС | ≥41 | 39,0-40,9 | 38,5-38,9 | 36,0-38,4 | 34,0-35,9 | 32,0-33,9 | 30,0-31,9 | <30 |
Частота дыхательных движений в минуту | ≥50 | 35-49 | 25-34 | 12-24 | 10-11 | 6-9 | ИВЛ или ППДВ | <6 |
Количество мочи, л/сут | ≥5,00 | 3,50-4,99 | 0,70-3,49 | 0,50-0,69 | 0,20-0,49 | <0,2 | ||
Мочевина крови, ммоль/л | ≥55 | 36 −54,9 | 29 −35,9 | 7,5 −28,9 | 3,5 −7,4 | <3,5 | ||
Гематокрит, % | ≥60,0 | 50,0-59,9 | 46,0-49,9 | 30,0-45,9 | 20,0-29,9 | <20,0 | ||
Количество лейкоцитов, ×109/л | ≥40 | 20,0-39,9 | 15,0-19,9 | 3,0-14,9 | 1,0-2,9 | <1 | ||
Глюкоза крови, ммоль/л | ≥44,4 | 27,8-44,3 | 13,9-27,7 | 3,9-13,8 | 2,8-3,8 | 1,6-2,7 | <1,6 | |
Калий крови, мэкв/л | ≥7,0 | 6,0-6,9 | 5,5-5,9 | 3,5-5,4 | 3,0-3,4 | 2,5-2,9 | <2,5 | |
Натрий крови, мэкв/л | ≥180 | 161—179 | 156—160 | 151—155 | 130—150 | 120—129 | 110—119 | <110 |
НСО3, мэкв/л | ≥40 | 30,0-39,9 | 20,0-29,9 | 10,0-19,9 | 5,0-9,9 | <5,0 | ||
Шкала Глазго, баллы | 13-15 | 10-12 | 7-9 | 4-6 | 3 |
ППДВ — постоянное положительное давление воздуха.
Формулировка диагноза[править | править код]
Диагноз выставляется по следующей схеме:[источник не указан 3358 дней]
- Основной:
- Цирроз печени,
- морфология (если есть), этиология,
- активность, класс по шкале Чайлда-Пью, стадия компенсации.
- Осложнения:
- Портальная гипертензия.
- Присутствующие синдромы (асцит, варикозно-расширенные вены пищевода (степень расширения)),
- гиперспленизм (степень),
- энцефалопатия (этиология, степень, стадия …)
Лечение[править | править код]
Лечение цирроза печени заключается в употреблении лекарственных препаратов и строгом соблюдении диеты, однако сформировавшийся цирроз печени необратим: печень в таком состоянии вылечить невозможно, единственный способ спасти жизнь пациенту — трансплантация печени.
Профилактические мероприятия[править | править код]
- предупреждение заражения острым вирусным гепатитом
- отказ от алкоголя
- защита от гепатотоксических препаратов
Диета[править | править код]
Диета при ЦП должна быть полноценной, содержащей 70—100 г белка (1—1,5 г на 1 кг массы тела), 80—90 г жиров (из них 50 % — растительного происхождения), 400—500 г углеводов. Необходимо учитывать привычки больного, переносимость продуктов и сопутствующие заболевания органов пищеварения. Исключаются химические добавки, консерванты и токсические ингредиенты. Диета модифицируется при наличии осложнений портальной гипертензии (отечно-асцитический, гепаторенальный синдром, печёночная энцефалопатия и др.)[7].
Урсодезоксихолевая кислота[править | править код]
Для восполнения дефицита жёлчных кислот в кишечнике, вызванного билиарной недостаточностью, целесообразно применять урсодезоксихолевую кислоту (УДХК). Дозировка — 10-15 мг на 1 кг веса пациента 1 раз в день на ночь — способствует восстановлению процессов пищеварения. Действие УДХК включает следующие моменты[7]:
- увеличение поступления жёлчи и панкреатического сока в кишку за счёт стимуляции их продукции
- разрешение внутрипечёночного холестаза
- усиление сокращения жёлчного пузыря
- омыление жиров и повышения активности липазы
- повышение моторики кишечника, улучшающей смешивание ферментов с химусом
- нормализация иммунного ответа
Гепатопротекторы[править | править код]
- Семена расторопши пятнистой и другие желчегонные препараты запрещены к использованию при циррозе[13].
Клеточная терапия[править | править код]
Традиционное лечение в основном заключается в применении фармацевтических средств для защиты печёночных клеток от повреждения, стимуляции выделения жёлчи, коррекции нарушений обмена веществ. Без сомнения, это улучшает состояние больного, но не в силах остановить развитие заболевания. Если вышеуказанные методы лечения не помогают, проводят трансплантацию (пересадку) печени.
Цирроз печени у животных[править | править код]
Болезнь развивается постепенно. Проходят недели и даже месяцы до наступления длительного и постоянного расстройства функций пищеварения с явлением атонии преджелудков, гастрита и энтерита. У животных извращается аппетит и появляются диспепсические явления, что приводит к истощению и общей слабости организма. Характерны для цирроза умеренная анемия и лейкопения. Нарушение обмена при циррозе печени влечёт за собой кахексию и анемию. Прогноз обычно неблагоприятный[14].
Примечания[править | править код]
- ↑ Monarch Disease Ontology release 2018-06-29sonu — 2018-06-29 — 2018.
- ↑ Cohn, Stephen M. Cohn, Steven T. Brower. Surgery: Evidence-Based Practice. — PMPH-USA, 2012. — 1018 с. — ISBN 9781607951094.
- ↑ Ariel Roguin. Rene Theophile Hyacinthe Laënnec (1781–1826): The Man Behind the Stethoscope // Clinical Medicine and Research. — 2006-9. — Т. 4, вып. 3. — С. 230–235. — ISSN 1539-4182.
- ↑ WHO Disease and injury country estimates. World Health Organization (2009). Дата обращения 11 ноября 2009. Архивировано 19 августа 2011 года.
- ↑ Циррозы печени. Вопросы этиологии, патогенеза, клиники, диагностики, лечения (недоступная ссылка). Дата обращения 6 декабря 2008. Архивировано 5 ноября 2008 года.
- ↑ 1 2 3 4 5 6 7 8 Садовникова И. И. Циррозы печени. Вопросы этиологии, патогенеза, клиники, диагностики, лечения // РМЖ. — 2003. — Т. 5, № 2. Архивировано 5 ноября 2008 года.
- ↑ 1 2 3 А. В. Яковенко, Э. П. Яковенко. Цирроз печени: вопросы терапии // Consilium medicum. — 2006. — Т. 8, № 7. Архивировано 25 декабря 2008 года.
- ↑ Аутоиммунные поражения печени – первичный билиарный цирроз печени и первичный склерозирующий холангит (недоступная ссылка). Медицина Алтая. Дата обращения 5 августа 2011. Архивировано 7 апреля 2016 года.
- ↑ Child C.G., Turcotte J.G. Surgery and portal hypertension // The liver and portal hypertension. — Philadelphia: W.B.Saunders Co., 1964. — P. 50.
- ↑ Pugh R.N.Н., Murray-Lyon I.M., Danson J.L. et al. Transection of the oesophagus for bleeding oesophageal varices // Brit. J. Surg. — 1973. — Vol. 60. — № 8. — P. 646—648.
- ↑ Habib A., Bond W. M., Heuman D. M. Long-term management of cirrhosis: appropriate supportive care is both critical and difficult // Postgrad. Med. — 2001. — Vol. 109, № 3. — P. 101—113.
- ↑ Le Gall J.-R., Lourait PH., Alperoviych A. et al. A simplified acute physiology score for ICU patients // Crit. Care Med. — 1984. — Vol. 12. — P. 975—977.
- ↑ Баева В. М. Расторопши семена — Sylibi semen // Лечение растениями: Основы фитотерапии (учебное пособие для студентов медиков и практикующих врачей). — М.: Астрель; АСТ, 2004. — С. 115—116. — 202 с. — 5100 экз. — ISBN 5-17-023217-9.
- ↑ Б.В.Уша и др. Внутренние болезни животных. — М.: КолосС, 2010. — 311 с.
Литература[править | править код]
- Ивашкин В. Т., Маевская М. В., Павлов Ч. С., Федосьина Е. А., Бессонова Е. Н., Пирогова И. Ю., Гарбузенко Д. В. Клинические рекомендации Российского общества по изучению печени и Российской гастроэнтерологической ассоциации по лечению осложнений цирроза печени // Рос. журн. гастроэнтерол., гепатол., колопроктол. — 2016. — Т. 26, № 4. — С. 71-102.
- Гарбузенко Д. В. Мультиорганные гемодинамические нарушения при циррозе печени // Терапевтический архив — 2007. — Т.79, № 2. — С.73-77
- Шерлок Ш., Дули Дж. Заболевания печени и жёлчных путей. — М. : ГЭОТАР Медицина, 1999. — 864 с.
- Е. М. Климова, И. А. Вотякова, Г. С. Лобынцева, Н. Ф. Ефимова, И. А. Кривцова. Обоснование применения криоконсервированных препаратов эмбрионального происхождения у больных с циррозом печени. Гематология и переливание крови. Т.30.. Тезисы 4-го з»їзда гематологів та трансфузіологів України., 2001, Киев. С.160.
Ссылки[править | править код]
- Б. Н. Левитан, А. В. Дедов / 50-летний опыт клинического изучения цирроза печени Кафедра факультетской терапии Астраханской государственной медицинской академии
- Популярная статья о циррозе печени
- Система SAPS
Источник


