Гемолиз при циррозе печени
В последнее время цирроз печени (ЦП) является достаточно актуальной социальной и медицинской проблемой. Это связано с увеличением частоты заболеваемости и смертности от осложнений цирроза печени.

Цирроз в подавляющем числе случаев характеризуется необратимым поражением печени. В крайне редких случаях и на ранних стадиях цирроза вероятно частичное восстановление функций печени после устранения причины, вызвавшей заболевание. Такое возможно, например, при вторичном билиарном циррозе печени, после устранения причин нарушения оттока желчи.
Клинические проявления цирроза печени
Появление и выраженность проявлений цирроза прямо зависит от степени поражения печени.
Если ЦП выявляется на стадии ранних симптомов, то вероятность успешного лечения и улучшения качества жизни больного достаточно высока. Поздние симптомы свидетельствуют о декомпенсированном течении ЦП, когда уже произошли глубокие и необратимые изменения паренхимы печени.

При декомпенсации течения заболевания страдают практически все функции печени, что проявляется разнообразными симптомами и синдромами. Самыми грозными из них являются: развитие портальной гипертензии и/или печеночной недостаточности.
Но не менее важными являются нарушения состава такого жизненно важного компонента человеческого организма, как кровь и нарушения функционирования системы кровообращения.
При ЦП выделяют два ведущих синдрома, характеризующих нарушения в системе крови: геморрагический и анемический.
Прежде чем мы рассмотрим причины и проявления этих синдромов, необходимо выяснить роль печени в осуществлении нормального процесса свертывания крови.
Роль печени в процессе свертывания крови
Процесс свертывания крови является одним из важнейших звеньев системы гемостаза. Система гемостаза выполняет следующие функции:
- Поддержание крови в жидком состоянии.
- «Ремонт» сосудов (тромбирование) при их повреждении.
- Растворение тромбов, которые выполнили свою роль.
Каким образом происходит остановка кровотечения?

После травмы сосуда происходит его рефлекторное сужение. К месту дефекта начинают «прилипать» специальные клетки крови – тромбоциты. Образуется так называемый первичный тромб.
Далее происходит активация многочисленных свертывающих факторов крови. Их участие запускает цепь достаточно сложных и многочисленных превращений и реакций, в результате которых происходит образование более плотного «вторичного» тромба.
После восстановления целостности сосуда активируется противосвертывающая система крови (фибринолиз) и происходит рассасывание тромба.
Какие факторы свертывания существуют?
На сегодняшний день известно 13 плазменных свертывающих факторов крови (содержащихся в плазме) и 22 – тромбоцитарных (находятся в тромбоцитах). Также свертывающие факторы крови находятся в эритроцитах, лейкоцитах и т. д.
Особый интерес представляют плазменные свертывающие факторы крови. По международной классификации их обозначают римскими цифрами. По структуре большая часть их является белками. И, самое важное – почти все они синтезируются в печени, за исключением двух: III и IV. Для синтеза многих из них необходимо наличие витамина K, поступающего с пищей.
Что еще делает печень?
В печени синтезируются многие фибринолитические белки, которые отвечают за процессы «разжижения» крови, рассасывания «ненужных» тромбов и т. д.
Следует также отметить, что большинство факторов как свертывающей системы, так и фибринолиза находятся в плазме крови в неактивном состоянии. Для того чтобы они выполнили свою функцию, должна произойти их активация путем некоторых биохимических реакций. После этого печень выполняет еще и утилизирующую функцию, удаляя из крови активированные факторы и комплексы и другие конечные продукты тромбообразования и тромболизиса.
Почему возникают нарушения свертывания крови при ЦП?

Механизмы развития геморрагического синдрома, как следствия нарушения свертывания крови при ЦП, очень разнообразны и сложны. Для удобства понимания этих процессов их можно разделить на три условные группы.
Уменьшение синтеза факторов свертывания крови
При декомпенсированной форме ЦП, в результате замещения большой площади функционирующих клеток печени (гепатоцитов) фиброзной тканью, происходит резкое нарушение всех ее функций. При этом страдает и синтетическая (производящая) функция печени.
Снижается концентрация всех факторов свертывания крови, синтезируемых печенью. Вначале происходит снижение уровня тех факторов, период «жизни» которых наименьший, например, фактора VII. Затем происходит уменьшение концентрации II, IX, X факторов. Далее, при тяжелой печеночной недостаточности уменьшается синтез факторов I, V и XIII.
Также необходимо отметить, что при ЦП часто наблюдаются нарушения механизмов желчевыделения.
Это, в свою очередь, вызывает нарушения процессов пищеварения и всасывания витаминов, микроэлементов и других питательных веществ из поступающей пищи. Такие изменения вызывают дефицит витамина K в организме и нарушение синтеза II, VII, IX и X факторов свертывания.
Увеличенное потребление факторов свертывания

Из поврежденных печеночных клеток в кровь выделяются особые тромбопластические вещества. При этом повышается фибринолитическая активность и появляется опасное состояние – диссеминированное внутрисосудистое свертывание крови (ДВС-синдром), приобретающее хроническое течение. При этом состоянии происходит массивное образование тромбоцитных тромбов в сосудах и активируется фибринолиз, что сопровождается повышенным потреблением факторов свертывания I, II, V, VII, IX — XI.
Уменьшение количества и изменение функциональных свойств тромбоцитов
При развитии ЦП, особенно, декомпенсированной его формы происходит снижение уровня тромбоцитов – тромбоцитопения. Наиболее частой причиной этого является диссеминированное внутрисосудистое свертывание крови (ДВС-синдром) и проявления гиперспленизма, при котором тромбоциты накапливаются в увеличенной селезенке.
При прогрессировании заболевания происходят и качественные изменения тромбоцитов, что влияет на способность их к агрегации (склеиванию) при образовании первичного тромба.
Отдельно следует отметить, что у лиц, злоупотребляющих алкоголем, также происходит снижение количества тромбоцитов в крови даже при отсутствии признаков декомпенсации ЦП.
Однако, при воздержании от употребления алкоголя в течение 1–2 недель, уровень тромбоцитов возвращается к нормальным значениям, чего не происходит при вышеописанных нарушениях.
Геморрагический синдром

Яркий пример нарушения согласованности процессов свертывания и фибринолиза при ЦП – геморрагический синдром (старое название – геморрагический диатез). Его проявления достаточно разнообразны, но доминирующим симптомом является кровотечение. Интенсивность кровотечения может быть различной – от микроскопического по размеру и абсолютно бессимптомного до обширного, массивного, угрожающего жизни больного.
Проявления геморрагического синдрома
Клиническая картина обусловлена повышенной кровоточивостью. Проявления этого могут быть очень разнообразными.
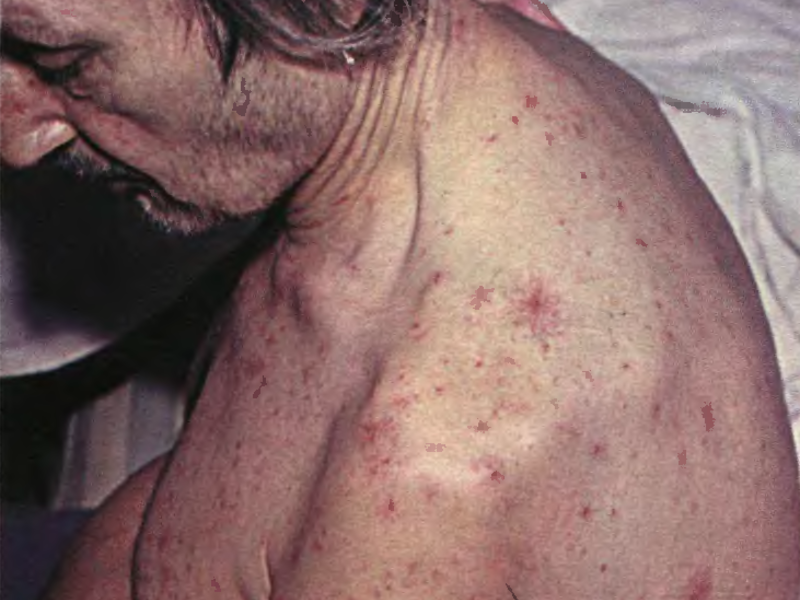
Сыпь
Такие кожные проявления геморрагического синдрома как сыпь, отличаются многообразием даже у одного и того же больного. Сыпь бывает мелкой, имеет вид петехий (пятен до 3 мм в диаметре). Также сыпь может быть в виде более крупных пятен – экхимозов или кровоподтеков (геморрагий или синяков). Кровоподтеки, в свою очередь, иногда могут приобретать достаточно большие размеры.
Чаще всего сыпь встречается в виде петехий и экхимозов, с размерами элементов до 1 см.
Цвет элементов сыпи может быть разный: пурпурно-красного, голубого, фиолетового и т. д. При надавливании сыпь не исчезает.
Другие проявления
Сыпь часто сопровождается болями в суставах и мышцах, животе, повышением температуры и другими проявлениями. Часто появление сыпи сопровождают видимые кровотечения в виде кровоточивости десен, носовые, маточные, из варикозно расширенных вен прямой кишки и пищевода и др.
Диагностика

Диагноз геморрагических осложнений течения цирроза печени устанавливается на основании характерных клинических проявлений и специфических изменений в анализах крови.
- При лабораторном исследовании выявляется снижение уровня тромбоцитов в крови.
- Исследуется также время свертывания крови (увеличивается) и длительность кровотечения (удлиняется).
- Обязательно исследование коагулограммы и определение основных факторов свертывания.
Иногда требуется повторное исследование коагулограммы в течение короткого промежутка времени: быстрое уменьшение количества факторов свертывания указывает на коагулопатию потребления, как одной из причин возникновения ДВС- и геморрагического синдромов.
А также по показаниям проводят другие тесты: тромбиновое и протромбиновое время, определение активности факторов свертывания, исследование функции тромбоцитов и т. д.
Анемический синдром

Анемия (малокровие) является достаточно частым симптомом хронических заболеваний печени и цирроза в том числе. Что такое анемия?
Анемией называют состояние, при котором происходит снижение уровня гемоглобина и/или эритроцитов (гематокрита) по сравнению с нормальным уровнем.
Гемоглобин – это железосодержащий белок, входящий в состав эритроцитов (красных кровяных шариков). Основная функция гемоглобина – перенос кислорода в ткани. При снижении его уровня, происходящего при развитии анемии, начинается гипоксия (кислородное голодание) тканей.
Проявления анемии
Клинические проявления анемии зависят от причины, ее вызвавшей. Однако, есть общие симптомы, которые встречаются при всех видах анемий:
- Бледность кожных покровов и слизистых.
- Повышенная утомляемость.
- Слабость.
- Обмороки, учащенное сердцебиение и т. д.
Для каждого вида анемий существуют и свои характерные признаки. При железодефицитной анемии наблюдается сухость кожи, ломкость и изменение формы ногтей. Гемолитическая анемия обычно сопровождается желтухой. При анемии, вызванной недостатком фолиевой кислоты, появляется стоматит (воспаление слизистой оболочки рта), глоссит (воспаление языка), ощущение покалывания в руках и ногах и т. д.
Диагностика

Диагноз устанавливается при исследовании периферической крови. Для этого часто достаточно сдать общий анализ крови (ОАК), а при необходимости проводятся и другие исследования.
Общий анализ крови
В ОАК выявляется, прежде всего, снижение уровня гемоглобина и эритроцитов. Определяется гематокрит – соотношение форменных элементов крови (эритроциты, лейкоциты и т. д.) к плазме. Рассчитывается цветной показатель (ЦП) – содержание гемоглобина в эритроците.
Также в ОАК возможно определить размеры эритроцитов – нормоциты, микроциты (уменьшение) или макроциты (увеличение). Иногда появляются качественные изменения эритроцитов:
- изменения величины (анизоцитоз);
- формы (пойкилоцитоз);
- степени окрашивания (анизохромия);
- появление «молодых» форм – ретикулоцитов и т. д.
Другие методы диагностики
Для более точного определения причины анемии возможно проведение специфических методов исследования: уровни сывороточного железа, фолиевой кислоты, B12, трансферрина, ферритина и т. д.
Иногда проводится биохимическое исследование крови – определение уровня билирубина, активности печеночных трансаминаз и др.
Причины анемии при ЦП

При циррозе печени анемия может развиваться вследствие действия нескольких причин. У больных ЦП эти причины могут сочетаться, и анемия приобретает черты полиэтиологического (многофакторного) заболевания. Все их объединяет, как уже указывалось выше, снижение уровней гемоглобина и эритроцитов. Рассмотрим основные факторы развития анемического синдрома и специфические критерии диагностики при каждом из них.
Анемия вследствие гиперволемии
Гиперволемия или увеличение объема циркулирующей плазмы – достаточно частое явление при циррозе печени. При этом развивается так называемая анемия разведения.
Если течение такой анемии не осложняется другими причинами, то при лабораторной диагностике дополнительно выявляется снижение только гематокрита.
Гемолитическая анемия
Этот вид анемии встречается достаточно часто при ЦП и иногда протекает бессимптомно. При обширном гемолизе (распадении эритроцитов) появляется гемолитическая желтуха. В анализах крови определяются ретикулоциты, повышается концентрация билирубина за счет непрямой его фракции и активность лактатдегидрогеназы (ЛДГ).
Гемолитическая анемия при ЦП практически всегда сочетается с увеличением селезенки и проявлениями гепатолиенального синдрома.
Микроцитарная анемия
Другие названия этого вида анемий – железодефицитная, гипохромная. Развивается вследствие острой или хронической кровопотери. У больных ЦП часто возникают кровотечения из варикозно расширенных вен пищевода или прямой кишки, как проявление портальной гипертензии. Длительные, но относительно небольшие кровопотери бывают при язвах желудочно-кишечного тракта, носовых кровотечениях и т. д.
В ОАК выявляется микроцитоз, анизоцитоз, пойкилоцитоз, снижение ЦП. Могут определяться ретикулоциты.
В биохимических исследованиях крови уменьшение содержания сывороточного железа, ферритина и другие признаки дефицита железа.
Макроцитарная анемия
Такой вид анемии при ЦП формируется вследствие нарушения обмена витамина B12 и/или фолиевой кислоты.
Недостаток фолиевой кислоты часто появляется у лиц, злоупотребляющих алкоголем. При отказе от алкоголя в течение нескольких месяцев проявления такой анемии исчезают.
В анализе крови выявляется макроцитоз, анизоцитоз, пойкилоцитоз, увеличение среднего объема эритроцитов и специфические изменения – гиперсегментация нейтрофилов (вид лейкоцитов). Также определяются мегалобласты – крупные клетки, являющиеся ранними предшественниками эритроцитов в процессе кроветворения. В тяжелых случаях выявляется уменьшение содержания всех форменных элементов крови – панцитопения.
В биохимических анализах выявляется уменьшение уровня фолиевой кислоты и/или витамина B12.
В заключение важно отметить, что оценивать результаты исследований и устанавливать диагноз должен только врач.
Источник
Цирро́з пе́чени (др.-греч. κίρρως — рыжий, янтарный) — хроническое заболевание печени, сопровождающееся необратимым замещением паренхиматозной ткани печени фиброзной соединительной тканью, или стромой. Цирротичная печень увеличена или уменьшена в размерах, необычно плотная, бугристая, шероховатая. Десятилетняя смертность от постановки диагноза составляет 34-66%, в зависимости от причин: алкогольный цирроз имеет худший прогноз, чем связанный с другими причинами. Первое известное описание заболевания было за авторством Гиппократа в 5-м веке до нашей эры[2]. Сам термин «цирроз» был изобретен в 1819 году из-за желтоватого цвета больной печени.[3]
Эпидемиология[править | править код]
Годы жизни, скорректированные по нетрудоспособности пациентов с циррозом печени на 100 000 населения в 2004 году.[4]
Нет данных Менее 50 50—100 100—200 200—300 300—400 400—500 500—600 600—700 700—800 800—900 900—1000 Более 1000
В экономически развитых странах цирроз входит в число шести основных причин смерти пациентов от 35 до 60 лет, составляя 14—30 случаев на 100 тыс. населения. Ежегодно в мире умирают 40 млн человек[5] от вирусного цирроза печени и гепатоцеллюлярной карциномы, развивающейся на фоне носительства вируса гепатита B. В странах СНГ цирроз встречается у 1 % населения.
Чаще наблюдается у мужчин: соотношение мужчин и женщин составляет в среднем 3:1. Заболевание может развиться во всех возрастных группах, но чаще после 40 лет[6].
Этиология[править | править код]
Чаще цирроз развивается при длительной интоксикации алкоголем (по разным данным, от 40—50 % до 70—80 %) и на фоне вирусных гепатитов B, С и D (30—40 %) и паразитарных инфекций. Более редкие причины цирроза — болезни желчевыводящих путей (внутри- и внепечёночных), застойная сердечная недостаточность, различные химические (гепатотоксины) и лекарственные интоксикации. Цирроз может развиваться и при наследственных нарушениях обмена веществ (гемохроматоз, гепатолентикулярная дегенерация, недостаточность α1-антитрипсина) и окклюзионными процессами в системе воротной вены (флебопортальный цирроз). Среди инфекционных факторов: хронические вирусные гепатиты, особенно B и C и паразитарные инфекции, особенно грибковые и трематодозные (шистосомоз, описторхоз, кандидоз, аспергиллёз). Первичный билиарный цирроз печени возникает первично без видимой причины. Приблизительно у 10—35 % больных этиология остаётся неясной[6].
Патогенез[править | править код]
За многие месяцы и годы меняется геном гепатоцитов и создаются клоны патологически изменённых клеток. Вследствие этого развивается иммуновоспалительный процесс.
Выделяют следующие этапы патогенеза цирроза[7]:
- Действие этиологических факторов: цитопатогенное действие вирусов, иммунные механизмы, влияние гепатотоксичных цитокинов, хемокинов, прооксидантов, эйкозоноидов, ацетальдегида, железа, продуктов перекисного окисления липидов
- Активизация функции клеток Ито, что приводит к избыточному разрастанию соединительной ткани в пространствах Диссе и перицеллюлярному фиброзу печени
- Нарушение кровоснабжения паренхимы печени за счёт капилляризации синусоидов и уменьшения сосудистого русла с развитием ишемических некрозов гепатоцитов
- Активация иммунных механизмов цитолиза гепатоцитов
При мостовидном некрозе гепатоцитов в зону поражения стягиваются Т-лимфоциты, которые активизируют клетки Ито, приобретающие фибробластоподобные свойства: синтезируют коллаген I типа, что и ведёт в итоге к фиброзу. Кроме того, микроскопически в печёночной паренхиме образуются ложные дольки, не имеющие центральной вены.
Алкогольный цирроз печени. Этапы: острый алкогольный гепатит и жировая дистрофия печени с фиброзом и мезенхимальной реакцией. Важнейший фактор — некроз гепатоцитов, обусловленный прямым токсическим действием алкоголя, а также аутоиммунными процессами.
Вирусный цирроз печени. Важным фактором является сенсибилизация иммуноцитов к собственным тканям организма. Основной мишенью аутоиммунной реакции является печёночный липопротеид.
Застойный цирроз печени. Некроз гепатоцитов связан с гипоксией и венозным застоем.
Развивается портальная гипертензия — повышение давления в системе портальной вены, обусловленное обструкцией внутри- или внепечёночных портальных сосудов. Это приводит к появлению портокавального шунтирования крови, спленомегалии и асцита. Со спленомегалией связаны тромбоцитопения (усиленное депонирование тромбоцитов в селезёнке), лейкопения, а также анемия вследствие повышенного гемолиза эритроцитов. Асцит приводит к ограничению подвижности диафрагмы, гастроэзофагальному рефлюксу с пептическими эрозиями, язвами и кровотечениями из варикозно-расширенных вен пищевода, брюшным грыжам, бактериальному перитониту, гепаторенальному синдрому. У больных циррозом печени часто наблюдаются гепатогенные энцефалопатии.
Первичный билиарный цирроз печени. Основное место принадлежит генетическим нарушениям иммунорегуляции. Вначале происходит разрушение билиарного эпителия с последующим некрозом сегментов канальцев, а позднее — их пролиферация, что сопровождается нарушениями экскреции жёлчи. Стадии процесса следующие:
- хронический негнойный деструктивный холангит
- дуктулярная пролиферация с деструкцией жёлчных канальцев
- рубцевание и уменьшение жёлчных канальцев
- крупноузловой цирроз с холестазом
Патологоанатомическая картина первичного билиарного цирроза включает инфильтрацию эпителия лимфоцитами, плазматическими клетками, макрофагами[6].
Лабораторными исследованиями выявляются антимитохондриальные антитела (АМА), наиболее специфичны — М2-АМА, направленные против Е2-субъединицы пируватдегидрогеназы, повышение IgM в сыворотке. Помимо этого выявляются иммуноопосредованные внепечёночные проявления — тиреоидит Хашимото, синдром Шегрена, фиброзирующий альвеолит, тубулоинтерстициальный нефрит, целиакия, а также сочетание с заболеваниями ревматического круга — системной склеродермией, ревматоидным артритом, системной красной волчанкой[8].
Симптомы[править | править код]
Большинство внепечёночных симптомов обусловлено повышением давления в синусоидах, что ведёт к возрастанию давления в системе воротной вены. Портальная гипертензия. Также характерным симптомом является «голова медузы» — перенаполнение вен передней брюшной стенки.
Для цирроза характерны общие симптомы: слабость, пониженная трудоспособность, неприятные ощущения в животе, диспепсические расстройства, повышение температуры тела, боли в суставах, также отмечаются метеоризм, боль и чувство тяжести в верхней половине живота, похудение, астения. При осмотре выявляется увеличение печени, уплотнение и деформация её поверхности, заострение края. Сначала отмечается равномерное умеренное увеличение обеих долей печени, позднее как правило преобладает увеличение левой доли. Портальная гипертензия проявляется умеренным увеличением селезёнки.
Развёрнутая клиническая картина проявляется синдромами печёночно-клеточной недостаточности и портальной гипертензии. Имеют место вздутие живота, плохая переносимость жирной пищи и алкоголя, тошнота, рвота, диарея, чувство тяжести или боль в животе (преимущественно в правом подреберье). В 70 % случаев обнаруживается гепатомегалия, печень уплотнена, край заострён. У 30 % больных при пальпации выявляется узловатая поверхность печени. Спленомегалия у 50 % больных.
Субфебрильная температура, возможно, связана с прохождением через печень кишечных бактериальных пирогенов, которые она не в состоянии обезвредить. Лихорадка резистентна к антибиотикам и проходит только при улучшении функции печени.
Могут быть внешние признаки — пальмарная или плантарная эритема, сосудистые звёздочки, скудный волосяной покров в подмышечной области и на лобке, белые ногти, гинекомастия у мужчин вследствие гиперэстрогенемии. В ряде случаев пальцы приобретают вид «барабанных палочек».
В терминальной стадии болезни в 25 % случаев отмечается уменьшение размеров печени. Также возникают желтуха, асцит, периферические отёки из-за гипергидратации (прежде всего отёки ног), внешние венозные коллатерали (варикозно-расширенные вены пищевода, желудка, кишечника). Кровотечение из вен часто заканчивается летальным исходом. Реже возникают геморроидальные кровотечения, они менее интенсивны.
Энцефалопатия может быть следствием как печёночно-клеточной, так и портально-печёночной недостаточности[6].
Осложнения[править | править код]
- печёночная кома
- кровотечение из варикозно-расширенных вен пищевода
- тромбоз в системе воротной вены
- гепаторенальный синдром
- формирование рака печени — гепатоцеллюлярной карциномы
- инфекционные осложнения — пневмонии, «спонтанный» перитонит при асците, сепсис
Диагностика[править | править код]
Цирроз печени с уменьшением объёма органа. Компьютерная томография брюшной полости.
Характерно повышение активности АЛТ, АСТ, щелочной фосфатазы, лейкоцитоз. При гепатолиенальном синдроме может развиваться гиперспленизм, проявляющийся лейкопенией, тромбоцитопенией, анемией и увеличением клеточных элементов в костном мозге.
Расширенные и извитые венозные коллатерали выявляются при ангиографии, компьютерной томографии, ультразвуковом исследовании или в ходе оперативного вмешательства.
Классификация[править | править код]
Морфологическая классификация[править | править код]
Предложена Всемирной ассоциацией гепатологов (Акапулько, 1974) и ВОЗ (1978)[6].
- мелкоузловой, или мелконодулярный цирроз (диаметр узлов от 1 до 3 мм)
- крупноузловой, или макронодулярный цирроз (диаметр узлов более 3 мм)
- неполная септальная форма
- смешанная (при которой наблюдаются различные размеры узлов) форма
Этиологическая классификация[править | править код]
Различают следующие формы цирроза[6]:
- вирусный
- алкогольный
- лекарственный
- вторичный билиарный
- врождённый, при следующих заболеваниях:
- гепатолентикулярная дегенерация
- гемохроматоз
- дефицит α1-антитрипсина
- тирозиноз
- галактоземия
- гликогенозы
- застойный (недостаточность кровообращения)
- болезнь и синдром Бадда-Киари
- обменно-алиментарный, при следующих состояниях:
- наложение обходного тонкокишечного анастомоза
- ожирение
- тяжёлые формы сахарного диабета
- цирроз печени неясной этиологии
- криптогенный
- первичный билиарный
- индийский детский
Шкала оценки тяжести печёночной недостаточности по Чайлду — Пью[править | править код]
Функция печёночных клеток при циррозе печени оценивается по Чайльду — Пью[9][10].
| Параметр | Баллы | ||
|---|---|---|---|
| 1 | 2 | 3 | |
| Асцит | Нет | Мягкий, легко поддаётся лечению | Напряжённый, плохо поддаётся лечению |
| Энцефалопатия | Нет | Лёгкая (I—II) | Тяжёлая (III—IV) |
| Билирубин, мкмоль/л(мг%) | менее 34 (2,0) | 34—51 (2,0—3,0) | более 51 (3,0) |
| Альбумин, г/л | более 35 | 28—35 | менее 28 |
| ПТВ, (сек) или ПТИ (%) | 1—4 (более 60) | 4—6 (40—60) | более 6 (менее 40) |
Класс цирроза выставляется в зависимости от суммы баллов по всем параметрам. Сумма баллов 5—6 соответствует классу A, при сумме 7—9 — классу B, а при сумме в 10—15 баллов — классу C[6].
Ожидаемая продолжительность жизни у больных класса А составляет 15—20 лет, послеоперационная летальность при полостном хирургическом вмешательстве — 10 %. Класс В является показанием для рассмотрения вопроса о пересадке печени; при этом послеоперационная летальность при полостном хирургическом вмешательстве достигает 30 %. У больных класса С ожидаемая продолжительность жизни достигает 1—3 года, а послеоперационная летальность при полостном вмешательстве — 82 %. На основании критериев Чайлда — Пью предложено оценивать необходимость в трансплантации печени: высокая необходимость у больных, относящихся к классу С, умеренная — у больных класса В и низкая — у больных класса А[11].
Система критериев SAPS[править | править код]
В последние годы для определения прогноза у пациентов в момент развития желудочно-кишечного кровотечения, комы, сепсиса и других осложнений используется система критериев SAPS (Simplified Acute Physiology Score), включающая основные физиологические параметры[12]. В стратификации имеют значение: возраст, ЧСС, ЧДД, систолическое артериальное давление, температура тела, диурез, гематокрит, лейкоциты крови, мочевина, калий, натрий, и бикарбонаты плазмы, а также стадия печёночной комы[6].
Критерии оценки по системе SAPS
Критерий | Баллы | |||||||
4 | 3 | 2 | 1 | 1 | 2 | 3 | 4 | |
Возраст, годы | ≤45 | 46-55 | 56-65 | 66-75 | >75 | |||
ЧСС в минуту | ≥180 | 140—179 | 110—139 | 70-109 | 55-69 | 40-54 | <40 | |
Систолическое артериальное давление, мм рт. ст. | ≥190 | 150—189 | 80-149 | 55-79 | <55 | |||
Температура тела, ºС | ≥41 | 39,0-40,9 | 38,5-38,9 | 36,0-38,4 | 34,0-35,9 | 32,0-33,9 | 30,0-31,9 | <30 |
Частота дыхательных движений в минуту | ≥50 | 35-49 | 25-34 | 12-24 | 10-11 | 6-9 | ИВЛ или ППДВ | <6 |
Количество мочи, л/сут | ≥5,00 | 3,50-4,99 | 0,70-3,49 | 0,50-0,69 | 0,20-0,49 | <0,2 | ||
Мочевина крови, ммоль/л | ≥55 | 36 −54,9 | 29 −35,9 | 7,5 −28,9 | 3,5 −7,4 | <3,5 | ||
Гематокрит, % | ≥60,0 | 50,0-59,9 | 46,0-49,9 | 30,0-45,9 | 20,0-29,9 | <20,0 | ||
Количество лейкоцитов, ×109/л | ≥40 | 20,0-39,9 | 15,0-19,9 | 3,0-14,9 | 1,0-2,9 | <1 | ||
Глюкоза крови, ммоль/л | ≥44,4 | 27,8-44,3 | 13,9-27,7 | 3,9-13,8 | 2,8-3,8 | 1,6-2,7 | <1,6 | |
Калий крови, мэкв/л | ≥7,0 | 6,0-6,9 | 5,5-5,9 | 3,5-5,4 | 3,0-3,4 | 2,5-2,9 | <2,5 | |
Натрий крови, мэкв/л | ≥180 | 161—179 | 156—160 | 151—155 | 130—150 | 120—129 | 110—119 | <110 |
НСО3, мэкв/л | ≥40 | 30,0-39,9 | 20,0-29,9 | 10,0-19,9 | 5,0-9,9 | <5,0 | ||
Шкала Глазго, баллы | 13-15 | 10-12 | 7-9 | 4-6 | 3 |
ППДВ — постоянное положительное давление воздуха.
Формулировка диагноза[править | править код]
Диагноз выставляется по следующей схеме:[источник не указан 3434 дня]
- Основной:
- Цирроз печени,
- морфология (если есть), этиология,
- активность, класс по шкале Чайлда-Пью, стадия компенсации.
- Осложнения:
- Портальная гипертензия.
- Присутствующие синдромы (асцит, варикозно-расширенные вены пищевода (степень расширения)),
- гиперспленизм (степень),
- энцефалопатия (этиология, степень, стадия …)
Лечение[править | править код]
Лечение цирроза печени заключается в употреблении лекарственных препаратов и строгом соблюдении диеты, однако сформировавшийся цирроз печени необратим: печень в таком состоянии вылечить невозможно, единственный способ спасти жизнь пациенту — трансплантация печени.
Профилактические мероприятия[править | править код]
- предупреждение заражения острым вирусным гепатитом
- отказ от алкоголя
- защита от гепатотоксических препаратов
Диета[править | править код]
Диета при ЦП должна быть полноценной, содержащей 70—100 г белка (1—1,5 г на 1 кг массы тела), 80—90 г жиров (из них 50 % — растительного происхождения), 400—500 г углеводов. Необходимо учитывать привычки больного, переносимость продуктов и сопутствующие заболевания органов пищеварения. Исключаются химические добавки, консерванты и токсические ингредиенты. Диета модифицируется при наличии осложнений портальной гипертензии (отечно-асцитический, гепаторенальный синдром, печёночная энцефалопатия и др.)[7].
Урсодезоксихолевая кислота[править | править код]
Для восполнения дефицита жёлчных кислот в кишечнике, вызванного билиарной недостаточностью, целесообразно применять урсодезоксихолевую кислоту (УДХК). Дозировка — 10-15 мг на 1 кг веса пациента 1 раз в день на ночь — способствует восстановлению процессов пищеварения. Действие УДХК включает следующие моменты[7]:
- увеличение поступления жёлчи и панкреатического сока в кишку за счёт стимуляции их продукции
- разрешение внутрипечёночного холестаза
- усиление сокращения жёлчного пузыря
- омыление жиров и повышения активности липазы
- повышение моторики кишечника, улучшающей смешивание ферментов с химусом
- нормализация иммунного ответа
Гепатопротекторы[править | править код]
- Семена расторопши пятнистой и другие желчегонные препараты запрещены к использованию при циррозе[13].
Клеточная терапия[править | править код]
Традиционное лечение в основном заключается в применении фармацевтических средств для защиты печёночных клеток от повреждения, стимуляции выделения жёлчи, коррекции нарушений обмена веществ. Без сомнения, это улучшает состояние больного, но не в силах остановить развитие заболевания. Если вышеуказанные методы лечения не помогают, проводят трансплантацию (пересадку) печени.
Цирроз печени у животных[править | править код]
Болезнь развивается постепенно. Проходят недели и даже месяцы до наступления длительного и постоянного расстройства функций пищеварения с явлением атонии преджелудков, гастрита и энтерита. У животных извращается аппетит и появляются диспепсические явления, что приводит к истощению и общей слабости организма. Характерны для цирроза умеренная анемия и лейкопения. Нарушение обмена при циррозе печени влечёт за собой кахексию и анемию. Прогноз обычно неблагоприятный[14].
Примечания[править | править код]
- ↑ Monarch Disease Ontology release 2018-06-29sonu — 2018-06-29 — 2018.
- ↑ Cohn, Stephen M. Cohn, Steven T. Brower. Surgery: Evidence-Based Practice. — PMPH-USA, 2012. — 1018 с. — ISBN 9781607951094.
- ↑ Ariel Roguin. Rene Theophile Hyacinthe Laënnec (1781–1826): The Man Behind the Stethoscope // Clinical Medicine and Research. — 2006-9. — Т. 4, вып. 3. — С. 230–235. — ISSN 1539-4182.
- ↑ WHO Disease and injury country estimates. World Health Organization (2009). Дата обращения 11 ноября 2009. Архивировано 19 августа 2011 года.
- ↑ Циррозы печени. Вопросы этиологии, патогенеза, клиники, д?

.jpg)