Экспресс диагностика гепатита в рнга
Оглавление темы «Вирусные гепатиты.»:
- Гепатит А. Болезнь Боткина. Вирус гепатита А. Эпидемиология гепатита А.
- Антигены вируса гепатита А. Патогенез гепатита А. Диагностика, лечение и профилактика гепатита А.
- Гепатит В. Вирус гепатита В. Эпидемиология гепатита В.
- Антигены вируса гепатита В. HBsAg. HBcAg. HBeAg. HBxAg.
- Патогенез гепатита В. Диагностика гепатита В. Лечение гепатита В.
- Профилактика гепатита В. Иммунопрофилактика гепатита В.
- Гепатит D. Вирус гепатита D. Свойства вируса гепатита D. Патогенез гепатита D.
- Диагностика гепатита D. Лечение гепатита D. Профилактика гепатита D.
- Гепатит С. Вирус гепатита С. Диагностика гепатита С. Лечение гепатита С. Профилактика гепатита С.
- Гепатит Е. Вирус гепатита Е. Диагностика гепатита Е. Лечение гепатита Е. Профилактика гепатита Е.
- Гепатит G. Вирус гепатита G. Диагностика гепатита G.
Патогенез гепатита В. Диагностика гепатита В. Лечение гепатита В.
Вирус гепатита В гематогенно заносится в печень и размножается в гепатоцитах. Во второй половине инкубационного периода (40-180 сут) вирус выделяют из крови, спермы, мочи, фекалий и секрета носоглотки.
В патогенезе гепатита В важную роль играют аутоиммунные гуморальные и клеточные реакции, что подтверждает связь между началом клинических*проявлений и появлением специфических AT. Патологический процесс начинается после распознавания вирусиндуцированных Аг на мембранах гепатоцитов иммунокомпетентными клетками.
Осложнения хронической формы гепатита В обусловлены хроническим воспалением и некротическими процессами в паренхиме печени; основные осложнения — цирроз и первичная карцинома печени. Цирроз обычно отмечают у страдающих острым хроническим гепатитом; ежегодно регистрируют более 10 000 летальных исходов, обусловленных вирусным гепатитом В.
Карцинома печени при гепатите В. Показана чёткая связь между злокачественной трансформацией гепатоцитов и перенесённым вирусным гепатитом В. В развитии опухолевого процесса принимают участие определённые кофакторы, многие из которых остаются неизвестными.
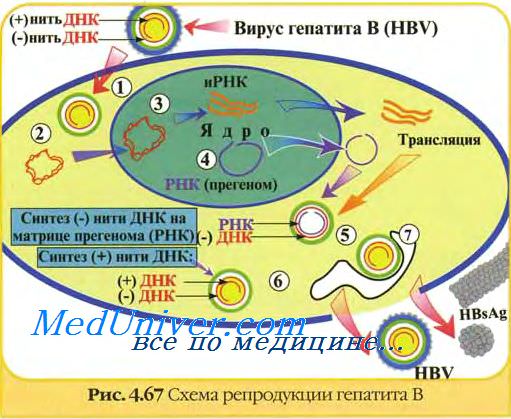
Принципы микробиологической диагностики гепатита В
Маркёры репликации вируса гепатита В — HBeAg, AT (IgM) к HBсAg, ДНК вируса и вирусная ДНК-полимераза, Для выявления HBsAg и HBeAg применяют ИФА и РНГА; исследования дополняют выявлением ДНК вируса гепатита В и вирусной ДНК-полимеразы. Вирусспецифические AT к HBsAg, HBeAg, HBeAg определяют в ИФА и РНГА. На наличие «свежей» инфекции указывают высокие титры HBsAg и IgM к HBsAg и HBeAg.
У пациентов с клинически проявляющимся гепатитом В титр HBsAg сначала растёт, а затем (по мере развития иммунных реакций) снижается. AT к HBsAg можно выявить только через несколько недель, что объясняют их активным связыванием в иммунные комплексы. В течение этого периода (так называемого «окна») можно обнаружить лишь AT к HBeAg.
AT к HBeAg. Важный диагностический маркер инфицирования, особенно при отрицательных результатах выявления HBsAg.
• IgM к HBcAg. Один из наиболее ранних сывороточных маркёров вирусного гепатита В. При хроническом гепатите маркируют репликацию вируса и активность процесса в печени. Их исчезновение является показателем либо санации организма от возбудителя, либо развития интегративной фазы инфекции.
• IgG к HBcAg. Сохраняются многие годы. Свидетельствуют об имеющейся или ранее перенесённой инфекции.
AT к HBeAg. Серологический маркёр интеграции вируса. В комплексе с IgG HBeAg и HBsAg свидетельствуют о полном завершении инфекционного процесса.
AT к HBsAg. Протективные AT; также образуются после вакцинации. Применительно к хроническому вирусному гепатиту, могут свидетельствовать о завершении вирусной инфекции.
AT к preS1— и preS2-фрагментам HBsAg. Свидетельствуют о развитии протективного иммунитета при завершении инфекционного процесса. AT к Pre-S выявляют одновременно с AT к HBcAg, a AT к Pre-S2.
Лечение гепатита В
Средства специфической терапии гепатита В отсутствуют, лечение в основном симптоматическое. Определённые перспективы имеет применение ингибиторов ДНК-полимеразы (например, ламивудина), а-ИФН и его индукторов. Несмотря на то что на терапию ИФН реагируют менее 50% пациентов, показаны достоверное исчезновение всех маркёров инфекции (ДНК вируса гепатита В, HBsAg и HBeAg) и увеличение титров AT к HBsAg
Видео лабораторная диагностика вирусных гепатитов
Посетите раздел других видео уроков по эпидемиологии.
— Также рекомендуем «Профилактика гепатита В. Иммунопрофилактика гепатита В.»
Источник
Современная диагностика гепатита В. Выявление HBsAg
Серологическая диагностика гепатита В в настоящее время строится на основании определения маркеров НВ-вирусной инфекции, как правило, с помощью имуноферментного анализа, то есть антигенов вируса гепатита В или антител к ним в биологических субстратах, главным образом, в сыворотке крови. В качестве основных маркеров гепатита В, имеющих самостоятельное значение для серологической диагностики, сегодня признаны:
HBsAg (поверхностный антиген вируса гепатита В) — основной маркер, свидетельствующий о наличии вируса гепатита В. При остром гепатите В HBsAg можно обнаружить еще в продромальном периоде, и длительность его персистенции при неосложненном течении составляет до 10 недель;
HBeAg — показатель высокой степени активности инфекционного процесса. Маркер репликации HBeAg определяется, как правило, при наличии HBsAg, однако циркулирует в крови менее продолжительное время — в среднем 4 недели;
anti-HBc класса IgM — показатель острого инфекционного процесса или, при хронических формах гепатита В, косвенный показатель активной репликации HBV. Возможна их длительная циркуляция;
anti-HBc (суммарные) — так называемые «анамнестические» антитела, образующиеся в результате перенесенного гепатита В, также присутствуют при хроническом гепатите В в комплексе с другими маркерами. В ряде случаев отмечена пожизненная циркуляция;
anti-HBs — свидетельство перенесенной ранее инфекции или поствакцинального иммунитета:
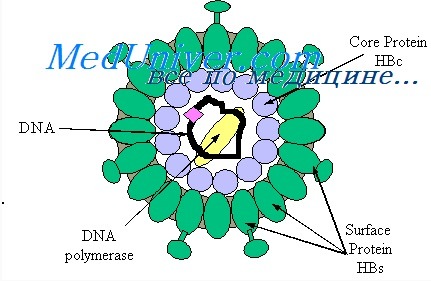
anti-HBe — не являются показателем, характеризующим какое-либо конкретное состояние при гепатите В. Эти антитела могут быть и в конце острого гепатита В и при хроническом гепатите и в случаях, так называемого здорового носительства HBsAg.
Хронический гепатит В: в фазу обострения наблюдается следующий профиль маркеров: HBsAg, HBeAg, DNA HBV, anti-HBc IgM и суммарные. В период стихания процесса обнаруживаются HBsAg, anti-HBc IgG (суммарные), возможна сероконверсия HBeAg на anti-HBe.
В основе всей серологигеской диагностики гепатита В: как острых, так и хронигеских форм—лежит определение HBsAg. Современные иммуноферментные тест-системы позволяют выявлять HBsAg в концентрациях до 0,1 нг/мл. Схема определения у разных тест-систем, как правило, одна и та же. В качестве иммуносорбента используются антитела к HBsAg. Как правило, применяются моноклональные антитела.
Именно они обеспечивают строгую специфичность применяемых в настоящее время диагностических наборов.
Сравнительные исследования чувствительности зарегистрированных во Франции иммуноферментных тест-систем различных производителей, проведенные Французским обществом переливания крови, позволили определить, что лучшие показатели могут быть достигнуты в результате длительной ночной инкубации при комнатной температуре.
Соблюдение таких условий постановки позволило определять HBsAg в концентрации 0,08 нг/мл («Wellcozyme HBsAg», производства «Murex»). Необходимо отметить, что наличие или отсутствие отдельных маркеров HBV может быть обусловлено не только особенностями иммунной системы человека, но и инфицированием мутантным штаммом HBV. Существует значительное количество мутаций вируса, при которых могут отсутствовать маркеры, обязательные при инфицировании дикими штаммами HBV.
ПЦР (полимеразная цепная реакция) в диагностике гепатита В
Метод полимеразной цепной реакции используют для подтверждения НВ-вирусной инфекции, наличия репликации вируса при остром и хроническом гепатите В, а также определения эффективности курса лечения. Наибольшей чувствительностью обладает двойной нестед-метод, который предполагает использование двух пар праймеров. Чувствительность нестедметода весьма высока и позволяет выявлять несколько копий DNA HBV в образце, что существенно превосходит возможности ИФА.
Сегодня разработаны соответствующие технологии производства отечественные тест-системы для детекции DNA HBV с помощью ПЦР, которые активно применяются в практическом здравоохранении. Высокая чувствительность ПЦР-диагностики при гепатите В расширила возможности раннего определения вируса гепатита В при острой инфекции. Длительность инкубационного периода при гепатите В достигает 6 месяцев, а в ряде случаев и больше. В это время вирус попадает в кровь, проникает в клетки печени, запускается механизм репликации, и в результате размножение приобретает устойчивый характер.
Эти процессы не затрагивают в значительной степени жизнедеятельность печени и других органов в течение длительного времени. В этот период эффекторные реакции иммунной системы организма не задействованы. Число вирусных частиц резко возрастает к концу инкубационного периода и становятся максимальными. В этот период методом ПЦР можно обнаружить в крови вирус гепатита В, тогда как остальные маркеры НВ-вирусной инфекции, главным образом серологические, ещё отсутствуют. Таким образом, с помощью полимеразной цепной реакции стала возможной более ранняя диагностика острого гепатита В.
Видео лабораторная диагностика вирусных гепатитов
Посетите раздел других видео уроков по эпидемиологии.
— Также рекомендуем «Вирус гепатита С и его геном»
Оглавление темы «Диагностика вирусных гепатитов»:
- Подтверждение или исключение гепатита D и гепатита С у детей
- ИФА в диагностике вирусных гепатитов. Возможности иммуноферментного анализа
- Вирус гепатита В и его антигены
- Мутации вируса гепатита В. Генетическая изменчивость ВГВ
- Заражение гепатитом В после прививки. Иммунитет к вирусу гепатита В
- Варианты HBsAg гепатита В и их распространение
- Современная диагностика гепатита В. Выявление HBsAg
- Вирус гепатита С и его геном
- Белки и антигены вируса гепатита С. Диагностика ВГС
- Современная диагностика вирусного гепатита А. Антигены HAV
Источник
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ
Тема: «Методы микробиологической диагностики вирусных инфекций. Профилактика вирусной инфекции»
Студент должен знать:
-морфологию, экологию, физиологию вирусов, методы их изучения;
-основы эпидемиологии вирусных инфекций (типы инфекций);
-основы химиотерапии и химиопрофилактики вирусной инфекции;
-факторы иммунитета при вирусных инфекциях.
Студент должен уметь:
-проводить профилактику вирусных инфекций;
-составлять алгоритмы действия в условиях эпидемии.
Вопросы для фронтального обсуждения:
1.Дайте понятие вирусам. Охарактеризуйте особенности строения и жизни вирусной частицы.
2.Какими факторами осуществляется защита организма человека от вируса.
3.Назовите группу и механизм действия препаратов на вирусы. Приведите примеры препаратов.
4.Назовите типы инфекции, вызываемые вирусами.
5. Назовите представителей кишечных, кровяных, респираторных вирусных инфекций, инфекций кожных покровов и слизистых.
6.Дайте понятие «Эпидемическому процессу», опишите структуру распространения инфекции среди населения.
7.Назовите, как называются мероприятия, ликвидирующие эпидемический процесс.
Самостоятельная работа студентов:
Запишите определения методов исследования вирусных инфекций.
Зарисйте в атлас внутриклеточные включения при натуральной оспе (тельца Гварниери), при бешенстве (тельца Бабеша-Негри).
3.Составьте план противоэпидемических мероприятий на вирусную инфекцию (инфекцию определяет преподаватель).
Краткие теоретические положения
Введение
Расширение возможностей в лечении и профилактике вирусных болезней с использованием противовирусных препаратов, иммуномодуляторов и вакцин с различным механизмом действия нуждается в быстрой и точной лабораторной диагностике. Узкая специфичность некоторых противовирусных препаратов также требует быстрой и высокоспецифичной диагностики инфицирующего агента. Появилась необходимость в количественных методах определения вирусов для мониторинга противовирусной терапии. Помимо установления этиологии заболевания лабораторная диагностика имеет важное значение в организации противоэпидемических мероприятий.
Ранняя диагностика первых случаев эпидемических инфекций позволяет своевременно провести противоэпидемические мероприятия – карантин, госпитализацию, вакцинацию и пр. Реализация программ по ликвидации инфекционных заболеваний, например натуральной оспы, показала, что по мере их выполнения возрастает роль лабораторной диагностики. Существенную роль играет лабораторная диагностика в службе крови и акушерской практике, например, выявление доноров, инфицированных вирусом иммунодефицита человека (ВИЧ), вирусом гепатита В (HBV), диагностика краснухи и цитомегаловирусной инфекции у беременных.
Методы диагностики вирусных инфекций
Для успешного выделения вирусов клинический материал должен быть взят в соответствии с патогенезом предполагаемого заболевания и в наиболее ранние сроки.
Как правило, берутся:
– при респираторных инфекциях – носоглоточный смыв;
– при энтеровирусных инфекциях – смыв и фекалии (рео-, энтеровирусы);
– при поражениях кожи и слизистых оболочек – соскобы, содержимое пузырьков (герпес, ветряная оспа);
– при экзантемных инфекциях – смывы (корь, краснуха);
– при арбовирусных инфекциях – кровь, спинномозговая жидкость.
1.Быстрые (экспресс-методы) — прямое обнаружение вируса или его компонентов (антигенов, НК), включений непосредственно в клиническом материале.
А. Вирусоскопический метод заключается в обнаружении вируса в исследуемом материале под микроскопом. Чаще всего используют электронный микроскоп. Световая микроскопия из-за ничтожно малых размеров вирусов практически не применяется. При данном методе можно определить тип НК, размеры вириона, форму вириона, а также выявить внутриклеточные включения, которые образуются в пораженных клетках при некоторых инфекциях.
II. Вирусологический метод основан на:
культивировании вирусов в чувствительных биологических системах (клеточных культурах, курином эмбрионе, организмах лабораторных животных),их индикации по цитопатогенному действию на биологическую систему (рис.1), идентификации по ингибиции действия вирусов соответствующими противовирусными антителами (рис.2).
Рис. 1. Цитопатическое действие вирусов на клетку: А-нормальный рост, Б-ЦПД вирусов на клетку
Рис.2 Ингибиция вируса антителами
Вирусологическое исследование — это «золотой стандарт» вирусологии и должно проводится в специализированной вирусологической лаборатории. В настоящее время оно используется практически только в условиях возникновения эпидемической вспышки того или иного вирусного инфекционного заболевания.
III. Серологический метод — определение противовирусных антител (оптимально — IgM) и/или определение динамики нарастания их титров за определенный период заболевания в парных сыворотках. Диагностически значимым считают нарастание титра антител в 4 и более раз.
Метод парных сывороток:осуществляем сбор венозной крови в количестве 10 мл в начале болезни и в конце, приготавливаем сыворотку, определяем количество антител в первой и второй сыворотке.
При этом четырехкратное нарастание титра антител во второй сыворотке в большинстве случаев служит показателем протекающей или свежеперенесенной инфекции. При исследовании одной сыворотки, взятой в острой стадии болезни, диагностическое значение имеет обнаружение антител класса Ig М, свидетельствующее об острой инфекции.
Современные методы диагностики:
1.ПЦР-выявляют персистирующие вирусы по НК, находящиеся в клиническом материале, с трудом обнаруживаемые или не обнаруживаемые другими методами.
2.Радиоизотопный иммунный анализ (РИА)-метод основан на метке антител радиоизотопами, что обеспечивало высокую чувствительность в определении вирусного антигена. Широкое распространение метод получил в 80-е годы, особенно для определения маркеров HBV и других некультивируемых вирусов. К недостаткам метода относится необходимость работать с радиоактивными веществами и использования дорогостоящего оборудования (гамма-счетчиков).
3.Иммуноферментный анализ (ИФА) – Иммуноферментные методы определения вирусных антигенов в принципе сходны с РИФ, но основываются на мечении антител ферментами, а не красителями. Наиболее широко используется пероксидаза хрена и щелочная фосфатаза, применяют также b-галактозидазу и b-лактамазы. Меченые антитела связываются с антигеном, и такой комплекс обнаруживается при добавлении субстрата для фермента, с которым конъюгированы антитела. Конечный продукт реакции может быть в виде нерастворимого осадка, и тогда учет проводится с помощью обычного светового микроскопа, или в виде растворимого продукта, который обычно окрашен (или может флюоресцировать или люминесцировать) и регистрируется инструментально.
Поскольку с помощью ИФА можно измерять растворимые антигены, то не требуется наличия интактных клеток в образце и таким образом могут использоваться различные виды клинического материала.
Другое важное преимущество метода ИФА – возможность количественного определения антигенов, что позволяет применять его для оценки клинического течения болезни и эффективности химиотерапии. ИФА, как и РИФ, может применяться как в прямом, так и в непрямом варианте.
Твердофазный ИФА, дающий растворимый окрашеный продукт реакции, нашел наибольшее распространение. ИФА может быть использован как для определения антигена (тогда на твердую фазу – дно лунки полистиролового планшета – наносятся антитела), так и для определения антител (тогда на твердую фазу наносятся антигены).
4.Реакция иммунофлюоресценции (РИФ) – Метод основан на использовании антител, связанных с красителем, например флюоресцеинизотиоцианатом. РИФ широко применяется для выявления вирусных антигенов в материале больных и для быстрой диагностики.
В практике применяются два варианта РИФ: прямой и непрямой. В первом случае применяются меченные красителем антитела к вирусам, которые наносятся на инфицированные клетки (мазок, культура клеток). Таким образом, реакция протекает одноэтапно. Неудобством метода является необходимость иметь большой набор конъюгированных специфических сывороток ко многим вирусам.
При непрямом варианте РИФ на исследуемый материал наносится специфическая сыворотка, антитела которой связываются с вирусным антигеном, находящимся в материале, а затем наслаивается антивидовая сыворотка к гамма-глобулинам животного, в котором готовилась специфическая иммунная сыворотка, например антикроличья, антилошадиная и т. п. Преимущество непрямого варианта РИФ состоит в потребности лишь одного вида меченых антител.
Метод РИФ широко применяется для быстрой расшифровки этиологии острых респираторных вирусных инфекций при анализе мазков-отпечатков со слизистой оболочки верхних дыхательных путей. Успешное применение РИФ для прямой детекции вируса в клиническом материале возможно лишь в случае содержания в нем достаточно большого числа инфицированных клеток и незначительной контаминации микроорганизмами, которые могут давать неспецифическое свечение.
5.Другие методы диагностики –
РТГА используется для диагностики заболеваний, вызванных гемагглютинирующими вирусами. Она основана на связывании антителами сыворотки больного добавленного стандартного вируса. Индикатором реакции являются эритроциты, агглютинирующиеся вирусом (формирование характерного «зонтика») при отсутствии специфических антител и оседающие на дно неагглютинированными при их наличии.
РСК является одной из традиционных серологических реакций и используется для диагностики многих вирусных инфекций. В реакции принимают участие две системы: антитела сыворотки больного + стандартный вирус и эритроциты барана + антитела к ним, а также оттитрованный комплемент. При соответствии антител и вируса этот комплекс связывает комплемент и лизиса бараньих эритроцитов не происходит (положительная реакция). При отрицательной РСК комплемент способствует лизису эритроцитов. Недостатком метода является его недостаточно высокая чувствительность и трудность стандартизации реагентов.
Для учета значимости РСК также, как и РТГА, необходимо титрование парных сывороток, то есть взятых в начале заболевания и в период реконвалесценции.
РПГА – агглютинация сенсибилизированных вирусными антигенами эритроцитов (или полистироловых шариков) в присутствии антител. На эритроцитах могут быть сорбированы любые вирусы, независимо от наличия или отсутствия у них гемагглютинирующей активности. В связи с наличием неспецифических реакций сыворотки исследуются в разведении 1:10 и более.
РНГА – агглютинация эритроцитов, сенсибилизированных специфическими антителами в присутствии вирусных антигенов. Наибольшее распространение РОПГА получила при выявлении HBs-антигена как у больных, так и у доноров крови.
Не нашли то, что искали? Воспользуйтесь поиском:
Источник: studopedia.ru
Источник


