Опн при кишечной инфекции
Острая почечная недостаточность при кишечных инфекциях. Диагностика ОПН при инфекцияхПри острых кишечных инфекциях, прежде всего при сальмонеллезе, может развиться патология почек. Степень нарушения функции почек зависит от тяжести течения болезни, в том числе от выраженности и длительности нарушений гемодинамики, а также от преморбидного состояния почек. По данным О.С.Буханцевой (1971), при пищевых токсикоинфекциях и сальмонеллезах в остром периоде выявлялись олигурия (77,8 %), патологические изменения мочевого осадка (47 %). Последние характеризовались протеинурией, микрогематурией, лейкоцитурией и цилиндрурией. Отмечалось снижение клубочковой фильтрации у 68,4 % обследованных лиц. При тяжелом течении пищевых токсикоинфекций и сальмонеллезов величина клубочковой фильтрации снижалась до 45,6 мл/мин, а при среднетяжелом — до 74,3 мл/мин. Вместе с тем выявлялось повышение канальцевой реабсорбции воды и концентрационного индекса креатинина у 87,7 % обследованных. Коэффициент очищения мочевины в остром периоде болезни был ниже нормы у 63,9 % больных. Сходные результаты были получены А.И.Ляшук (1973). По данным Ю.Ю.Черниковой (1984), при среднетяжелом течении пищевых токсикоинфекций нарушаются реабсорбционная, азотовыделительная и ионрегулирующая функции почек, уменьшается объем внутриклеточной жидкости, снижается абсолютное содержание натрия в циркулирующей крови, а также концентрация калия и хлора. Автором были выявлены три типа нарушений кислотовыделительной функции почек, из которых наиболее неблагоприятными для регуляции КОС являлись парадоксальная ацидурия и тубулярный ацидоз. Аккомодационная способность почек, выявленная с помощью нагрузки бикарбонатом натрия, снижалась. Однако у части больных с острыми кишечными инфекциями патологические изменения в почках достигают Уровня ОПН. Последняя справедливо расценивается как осложнение острых кишечных инфекций. При пищевых токсикоинфекциях и сальмонеллезах острая почечная недостаточность нами была выявлена у 246 больных (0,8 %). Различались преренальная и ренальная форма ОПН. Преренальная форма ОПН отмечалась у 76,4 % из них и была связана с резкими нарушениями почечного кровотока при расстройствах гемодинамики.
Снижение систолического давления ниже 70 мм ртст резко ограничивало фильтрационный процесс в почках Как правило, преренальная форма ОПН наблюдалась при тяжелом течении пищевых токсикоинфекций с обезвоживанием II —III степени и нестабильной гемодинамикой Нарушения мочевыделения сопровождались снижением очистительной способности почек и приводили к повышению концентрации креатинина и мочевины в крови. По нашим наблюдениям, выявлялась достоверно низкая концентрация ионов натрия, калия и хлора, что в сочетании с повышенной реабсорбцией их в канальцах приводило к уменьшению выведения с мочой Суточная экскреция ионов натрия, калия и хлора снижалась. Уменьшение фильтрации и усиление реабсорбции носили компенсаторный характер, направленный на сохранение электролитного гомеостаза. Выраженность преренальной формы ОПН может быть различной — от клинически латентной до значительной. У некоторых больных преренальная форма ОПН возникала при ИТШ, преимущественно с выраженным обезвоживанием. При этом кровоток в почках уменьшался не только в связи с общей циркуляторной недостаточностью, но и в результате селективной вазоконстрикции почечных сосудов. Эта компенсаторная реакция, направленная на «централизацию кровообращения», сопровождалась нарушением функционального состояния почек, особенно коркового слоя, на долю которого приходится до 90 % почечного кровотока. Развивались олигурия и азотемия. Эта начальная стадия преренальной формы ОПН обратима, но при сохраняющейся циркуляторной недостаточности может трансформироваться в ренальную форму ОПН — «ишемическую». Эта форма проявляется усугублением олигурии, достигающей стадии анурии, а также нарастанием азотемии, протекающих в условиях коррекции гемодинамики. Тщательный учет диуреза помогает выявлять олигурию (диурез менее 500 мл/сут). При этом наблюдается стойкое снижение относительной плотности мочи (до 1003—1010), что свидетельствует о нарушении концентрационной функции почек. В мочевом осадке выявляются эритроциты, зернистые цилиндры и повышенное количество лейкоцитов. Диагностика ОПН должна быть ранней, и этому способствует исследование почасового диуреза. Снижение его ниже 35—45 мл/ч является признаком олигурии. Однако обычные анализы мочи информативны лишь у 2/3 больных. Наиболее информативны показатели концентрации креатинина в сыворотке крови (норма до 0,06—0,07 ммоль/л), несколько менее информативны показатели концентрации мочевины (норма до 8,3 ммоль/л). Азотемия во многих случаях предшествует снижению диуреза. Для клинической картины ОПН характерны тошнота, повторная рвота, икота, анорексия, усталость, вялость, головная боль, заторможенность, сонливость, снижение диуреза. У некоторых больных возможно развитие анемии и изменений в свертывающей системе. Таким образом, ОПН свойственны олигурия (у 80 % пациентов), метаболический ацидоз (чаще декомпенсированный), гиперкалиемия, гиперазотемия, угроза гипергидратации. Необходимо иметь в виду, что критическими показателями при ОПН являются концентрация креатинина 0,6 ммоль/л, концентрация мочевины 30 ммоль/л, концентрация калия 6 ммоль/л. Ренальная форма ОПН, по нашим наблюдениям, отмечалась у 23,6 % больных. Она была следствием поражения нефрона и канальцевого эпителия. Чаще всего эта форма ОПН наблюдалась при ИТШ, протекавшем без выраженного обезвоживания. Синдром «шоковой почки» наиболее часто развивался в фазе гиперкоагуляции ДВС. При этом микротромбы локализовались почти всегда в почечных клубочках, что определяло олигурию и снижение скорости фильтрации. Распространенный гломерулотромбоз создавал условия для возникновения кортикального некроза канальцев и рассматривался как морфологический маркер синдрома «шоковой почки». — Также рекомендуем «Стадии почечной недостаточности. Водно-электролитный гомеостаз при кишечных инфекциях» Оглавление темы «Осложнения кишечной инфекции»: |
Источник
Принципы лечения.
Острая печеночная недостаточность (ОПечН) — клинико-патогенетический синдром, обусловленный цитолизом, острым нарушением дезинтоксикационной и синтетической функции печени, в результате чего развиваются геморрагические осложнения и энцефалопатия. Эндогенная печеночная недостаточность чаще всего развивается при вирусном гепатите В, С, D, желтой лихорадке, некоторых других инфекциях и отравлениях грибами.
Развитие ОПечН проходит следующие стадии:
1 стадия — уменьшение размеров печени, нарушения сна (бессонница ночью и сонливость днем), немотивированное поведение (поиск несуществующих предметов), появление «мушек» перед глазами, адинамия или эйфория, брадикардия, сменяющаяся тахикардией;
2 стадия — нарушение ориентации в пространстве и времени, двигательное возбуждение, психические нарушения, тремор верхних конечностей:
3 стадия — периодически нарушается сознание, возникают галлюцинации, возможны менингеальные знаки, «печеночный запах» изо рта, тахикардия, геморрагический синдром, значительное снижение протромбина.
4 стадия (печеночная кома) — сознание, болевая чувствительность, рефлексы отсутствуют, зрачки расширены, нарастает уровень свободной (непрямой) фракции билирубина крови, снижается активность АлАТ (вследствие массивного гепатонекроза), в крови — лейкоцитоз, увеличенная СОЭ.
Интенсивная терапия больных с ОПечН заключается в проведении активной неспецифической дезинтоксикации, которая включает как экстракорпоральные методы, так и инфузионную терапию. Применяют также антигипоксанты, средства, уменьшающие кишечную аутоинтоксикацию (энтеросорбенты), коррекцию нарушений КОС, системы свертывания крови, всех видов обмена веществ. Обязательно назначают кортикостероиды (3-5 мг/кг массы из расчета на преднизолон) в комплексе с дегидратационными средствами для предупреждения или уменьшения отека мозга (маннитол, фуросемид). При психомоторном возбуждении вводят натрия оксибутират 20%, диазепам (сибазон, седуксен). Для угнетения процессов аутолиза назначают ингибиторы протеиназ (контрикал, трасилол, гордокс). Для выведения церебротоксичных веществ применяют гемосорбцию, плазмаферез, экстракорпоральную перфузию крови через гетеро — или гомопечень. Для угнетения кишечной флоры назначают внутрь лактулозу, антибиотики (неомицин). С целью уменьшения аутоинтоксикации назначают безбелковую диету, очищают желудок и кишечник сифонными промываниями 2% раствором гидрокарбоната натрия.
Острая почечная недостаточность (ОПН) — нарушение выделительной функции почек с задержкой в крови азотистых продуктов метаболизма, калия, магния и воды с развитием метаболического ацидоза.
Преренальная ОПН является следствием критических состояний, сопровождающихся глубоким расстройством кровообращения и перфузии почек при инфекционно-токсическом, дегидратационном или анафилактическом шоке и снижении АД ниже 70 мм рт. ст. Длительная (более 8 ч) гипотензия ведет к гипоксии, ацидозу и необратимым изменениям почек.
Ренальная ОПН — следствие первичного поражения нефронов, эндотелия почечных канальцев при лептоспирозе и геморрагической лихорадке с почечным синдромом.
Начальная стадия ОПН не имеет специфических симптомов. Заподозрить ее развитие помогает систематический учет диуреза, снижающегося до 0,5 мл/кг массы в час. Одновременно уменьшается концентрационная способность почек — снижается удельный вес мочи, в ее осадке появляются эритроциты, цилиндры, клетки эпителия, в крови нарастают мочевина, креатинин, калий.
В течение нескольких дней наступает олигоанурия. Наряду с уменьшением количества мочи (при олигурии менее 500 мл/сут, при анурии менее 50 мл/сут), снижается и удельный вес мочи (до 1005-1008). В крови значительно повышаются мочевина, креатинин, калий, возникает гипергидратация (даже при ограничении поступления жидкости в организм, в связи с образованием эндогенной воды). Нарастает концентрация в крови электролитов и неорганических кислот. Развивается метаболический ацидоз. Уремия сопровождается поражением ЦНС, возникают интенсивная головная боль, сухость слизистых полости рта, языка и губ, рвота, поносы, одышка, тахикардия, снижается АД, прогрессируют нарушения сознания вплоть до сопора, нарушается ритм дыхания (типа Чейн-Стокса, Куссмауля). При отсутствии интенсивной терапии может развиться отек легких или остановка сердца в связи с гиперкалиемией.
Лечение инфекционных больных в начальной стадии ОПН должно быть направлено на ликвидацию факторов, вызывающих нарушение функции почек. В первую очередь необходимо восстановление системной гемодинамики и микроциркуляции в почках (при ИТШ), регидратация (при ДС), устранение гиповолемии, артериальной гипотензии. Одновременно проводят коррекцию КОС (устранение метаболического ацидоза) в/в введением 200-400 мл 4% раствора гидрокарбоната натрия. С целью стимуляции выделительной функции почек в/в вводят маннитол, реоглюман или фуросемид.
В олигоанурической стадии ОПН проводится комплексная интенсивная терапия, первоочередной задачей которой является борьба с гипергидратацией. Прежде всего, следует строго соблюдать водный баланс, который должен соответствовать объему выделенной за сутки мочи, перспирации воды через легкие и кожные покровы и объему испражнений и рвотных масс. Для уменьшения азотемии назначают безбелковую диету, белкового катаболизма — анаболические гормоны (ретаболил, неробол) и концентрированные растворы глюкозы. Путем повторных промываний желудка и толстого кишечника 2% раствором натрия гидрокарбоната удаляют азотистые шлаки. Назначают также энтеросорбенты (энтеросгель, полисорб и др). При стабилизации гемодинамики и ликвидации ацидоза проводят стимуляцию диуреза 1% раствором фуросемида, 2,4% раствором эуфиллина. В случае отсутствия эффекта от проведенных лечебных мероприятий, продолжающейся анурии, повышении содержания мочевины более 33,3 ммоль/л, креатинина более 0,884 ммоль/л и калия более 7 ммоль/л проводит экстракорпоральный гемодиализ.
Стадия полиурии также относится к критическим состояниям. Повышенный диурез способствует дегидратации и нарушению водно-электролитного баланса, развитию гипокалиемии. В этот период следует тщательно контролировать и корригировать водно-электролитный баланс. Снижение азотемии начинается к концу первой недели интенсивной терапии, а нормализация наступает в течение двух недель.
Источник
Кишечные инфекции – это острые состояния, которые возникают вследствие инвазии патогенных микроорганизмов в кишечник человека. Поражение пищеварительной системы может быть вызвано множеством возбудителей. Объединяет данные состояния общность клинической картины – выраженный диарейный синдром и интоксикация пациента.
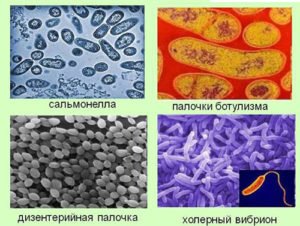
Возбудители кишечных инфекций
В зависимости от происхождения все кишечные инфекции можно разделить на:
- бактериальные;
- вирусные;
- протозойные.
Значительно реже заболевание ассоциировано с патогенными грибками.
| Бактериальные инфекции | Вирусные инфекции | Протозойные инфекции |
|
|
|
Симптомы
Общие симптомы
- Болевой синдром. В зависимости от уровня поражения кишечника боли могут локализоваться в области верхних или нижних отделов живота.
- Диарейный синдром. Для большинства кишечных инфекций характерно учащение дефекации, которое часто сопровождается появлением ложных позывов – тенезмов.
- Запоры. В тяжелых случаях заболевания возможно развитие пареза кишечника, который внешне характеризуется стойким запором, сохраняющимся на протяжении нескольких суток.
- Изменение характера стула. В большинстве случаев стул становится жидким, водянистым, меняется его цвет. В составе кала могут обнаруживаться остатки непереваренной пищи, слизь или кровь.
- Общая интоксикация организма. Кишечная инфекция обязательно сопровождается ухудшением общего состояния пациента, которое проявляется возникновением лихорадки, общей слабости, головных болей, снижения массы тела, отсутствием аппетита.
- Тошнота и рвота. В зависимости от тяжести течения заболевания рвота может быть однократной или многократной, приносить пациенту облегчение или, наоборот, ухудшать его состояние.

Специфические симптомы
| Кишечная инфекция | Специфические симптомы |
| Ботулизм |
|
| Сальмонеллез |
|
| Дизентерия |
|
| Эшерихиоз |
|
| Брюшной тиф |
|
| Паратифозные инфекции |
|
| Ротавирусная инфекция |
|
| Аденовирусная инфекция |
|
| Энтеровирусная инфекция |
|
Пути передачи кишечных инфекций
-
 Алиментарный путь. Заражение происходит через употребляемую пищу. Такой механизм передачи наиболее характерен для кишечных инфекций.
Алиментарный путь. Заражение происходит через употребляемую пищу. Такой механизм передачи наиболее характерен для кишечных инфекций. - Водный путь. Попадание микроорганизмов в тело человека осуществляется при употреблении воды из непроверенных источников.
- Контактно-бытовой путь. Распространение бактерий происходит через предметы обихода.
- Воздушно-капельный путь. Наиболее редко микроорганизмы проникают в тело человека после вдыхания воздуха, в который попали частички мокроты инфицированного пациента. Для кишечных инфекций практически не характерен аэрозольный путь передачи, однако в исключительных случаев возможно и такое заражение.
Диагностика
При подозрении на кишечную инфекцию пациент должен обратиться к своему терапевту. После обследования врач сможет предположить конкретный диагноз и назначит лечение. При тяжелом течении заболевания или при подозрении на специфическую инфекцию (например, дизентерию) больной направляется в специализированный инфекционный стационар для проведения профильной терапии и обеспечения необходимой изоляции.
Для подтверждения диагноза кишечной инфекции используются следующие методики диагностики:
-
 Исследование кала. Копрограмма дает возможность исследовать кал, обнаружить возможные примеси крови, иммунных клеток, выделить бактерии и отправить их на посев.
Исследование кала. Копрограмма дает возможность исследовать кал, обнаружить возможные примеси крови, иммунных клеток, выделить бактерии и отправить их на посев. - Бактериологическое исследование кала. Посев полученного от пациента биоматериала – основной способ определения возбудителя заболевания. Бактерии культивируются на специальных питательных средах и тщательно исследуются, что позволяет установить вид патогенной бактерии. Кроме того, после определения возбудителя проводится его тестирование на чувствительность к антибиотикам, что позволяет точно подобрать эффективную терапию для пациента.
- Серологические исследования. Дополнительным способом диагностики являются исследование на антитела в крови пациента. Они выделяются в ответ на воздействие бактерий через 4-5 дней. Антитела имеют высокую специфичность по отношению к определенной бактерии, благодаря чему можно установить разновидность микроорганизма.
Лечение
Лечение кишечной инфекции зависит от того, каким возбудителем она вызвана, однако можно выделить ряд общих правил, которые относятся ко всем поражениям пищеварительной системы.
Диета
 При легкой форме патологии пациенту назначается щадящая диета. Уменьшается общий объем пищи, исключаются вредные для кишечника продукты, назначается максимально щадящее питание. При среднетяжелом и тяжелом течении заболевания общий суточный калораж сокращается примерно на 40-50%. Рекомендуется увеличить частоту приемов пищи до 6-8 раз в день. В период восстановления, когда диарейный синдром исчезает, рекомендуется назначить пациенту пребиотики как в виде пищевых продуктов, так и отдельно, в таблетках.
При легкой форме патологии пациенту назначается щадящая диета. Уменьшается общий объем пищи, исключаются вредные для кишечника продукты, назначается максимально щадящее питание. При среднетяжелом и тяжелом течении заболевания общий суточный калораж сокращается примерно на 40-50%. Рекомендуется увеличить частоту приемов пищи до 6-8 раз в день. В период восстановления, когда диарейный синдром исчезает, рекомендуется назначить пациенту пребиотики как в виде пищевых продуктов, так и отдельно, в таблетках.
| Рекомендуемые продукты | Нерекомендуемые продукты |
|
|
Препараты
Для лечения тяжелых бактериальных инфекций применяются антибиотики. Средства подбираются в зависимости от возбудителя.
Определение схемы терапии и дозировки лекарства проводится только лечащим врачом пациента.
При более легких формах заболевания антибактериальные препараты обычно не назначаются, проводится симптоматическая терапия. В нее входят:
-
 Введение солевых растворов (Трисоль, Регидрон). При легких формах заболевания жидкость назначается внутрь, при тяжелом течении – вводится парентерально.
Введение солевых растворов (Трисоль, Регидрон). При легких формах заболевания жидкость назначается внутрь, при тяжелом течении – вводится парентерально. - Жаропонижающие средства. Для снижения температуры и интоксикации назначаются нестероидные противовоспалительные средства (Ибупрофен, Нимесулид), а также Парацетамол.
- Сорбенты (Энтеросгель, Полисорб, Смекта). Препараты из данной группы обезвреживают токсические вещества, которые содержатся в пораженном кишечнике, и выводят их из организма. Благодаря этому снижается выраженности интоксикации организма.
- Пробиотики и пребиотики. Кишечные инфекции обычно сопровождаются симптомами дисбактериоза, поэтому пациентам назначаются средства для восстановления нормальной микрофлоры пищеварительной системы. Лекарства применяются исключительно в реабилитационном периоде, когда исчезает диарейный синдром, так как до этого их использование практически неэффективно.
При подозрении на кишечную инфекцию пациент должен оценить свое состояние и принять решение о тактике лечения. Если это легкое пищевое отравление, которое не сопровождается выраженным подъемом температуры и внекишечными симптомами, то заболевание можно лечить дома. Для этого рекомендуется голод и покой, обильное питье, использование сорбентов. При тяжелом состоянии больного, выраженной лихорадке, присоединении внекишечных проявлений обязательно нужно обратиться к врачу. Возможно, пациенту потребуется госпитализация в гастроэнтерологическое отделение или инфекционную больницу.
Прогноз для пациента будет зависеть от возбудителя кишечной инфекции. В большинстве случаев болезнь легко устраняется, однако при некоторых специфических заболеваниях болезнь сопровождается осложнениями и может даже привести к летальному исходу. Залогом благоприятного разрешения заболевания является раннее обращение к врачу и соблюдение его инструкций.
Возможные осложнения
- инфекционно-токсический шок;
- вторичное распространение очагов инфекции, поражение других органов;
- острая почечная недостаточность;
- дисбактериоз.
Профилактика
- регулярно мыть руки перед приемом пищи;
- употреблять мясные и молочные продукты из проверенных источников;
- не пить воду из природных водоемов, не купаться на неофициальных пляжах;
- тщательно мыть фрукты и овощи, даже перед термической обработкой;
- соблюдать правила личной гигиены, не пользоваться чужими личными вещами (например, полотенцами);
- по возможности ограничить контакты с людьми, имеющими признаки кишечных инфекций.
Источник