Первичный билиарный цирроз формулировка диагноза
Справочник болезней
«Медицина заставляет нас умирать продолжительнее и мучительнее» Плутарх
ОПРЕДЕЛЕНИЕ
Диффузный процесс в печени, характеризующийся фиброзом и образованием узлов.
Морфология цирроза печени
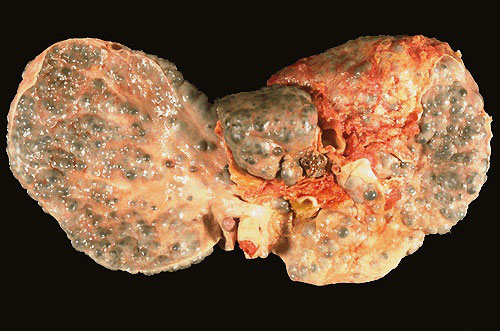
Макронодулярный (крупноузловой) цирроз печени.
ЭТИОЛОГИЯ ЦИРРОЗА ПЕЧЕНИ
• Вирусный гепатит (В, С).
• Алкогольный стеатогепатит.
• Неалкогольный стеатогепатит
• Метаболические нарушения (гемохроматоз, болезнь Вильсона).
• Холестаз внутри- или внепеченочный.
• Нарушение венозного оттока (синдром Бадда-Киари).
• Лекарства (амиодарон, метотрексат).
Морфология цирроза печени
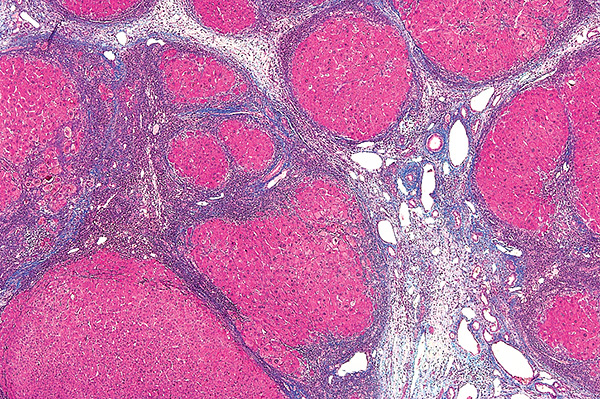
Фиброзные перегородки, отделяющие узлы регенерирующих гепатоцитов.
КЛИНИЧЕСКАЯ КАРТИНА
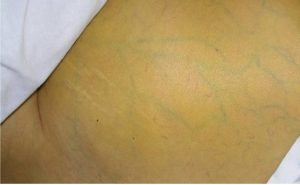
• Портальная гипертензия: отеки, асцит, расширение вен пищевода, кровотечения из пищевода, расширение подкожных вен.
• Печеночная недостаточность: гипопротеинемические отеки, коагулопатия (> протромбинового времени, МНО), гинекомастия.
• Бактериальный перитонит: лихорадка, боли в животе, напряжение брюшной стенки отеки, >250 полиморфноядерных лейкоцитов в мм3 асцитической жидкости.
• Гепатокарцинома.
• Гепаторенальный синдром.
Прогрессирование цирроза печени
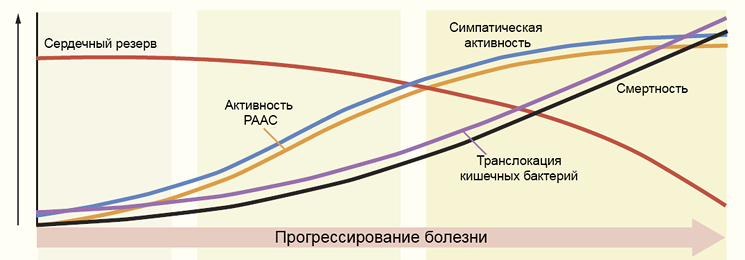
РААС — ренин-ангиотензин-альдостероновая система. Ge P, Runyon B. N Engl J Med. 2016;375:767–77.
ДИАГНОСТИКА
• Общий анализ крови с тромбоцитами.
• Биохимический анализ крови: АСТ, АЛТ, ЩФ, ГГТП, протеинограмма, коагулограмма, альфа–фетопротеин, креатинин.
• Шкала APRI: неинвазивная оценка цирроза печени.
• Сонография: узлы, неравномерная плотность, асцит, v.portae >13 мм. Повторять через 2–3 года.
• Эзофагогастроскопия (обычная, ультратонкая ≤6 мм): варикоз вен пищевода, желудка.
• Эластография печени.
• Вирусы гепатита В (HBsAg, анти-HBc, анти-HBs, HCV DNA, HBeAg), С (анти-HCV, HCV RNA, HCVcAg).
По показаниям
• Компьютерная томография: гепатокарцинома.
• Биопсия: узлы, гепатокарцинома.
• Парацентез: анализ и посев асцитической жидкости.
• Биохимический анализ крови: церулоплазмин, железо сыворотки, ферритин, насыщение трансферрина железом.
Цирроз печени и легочная эмболия
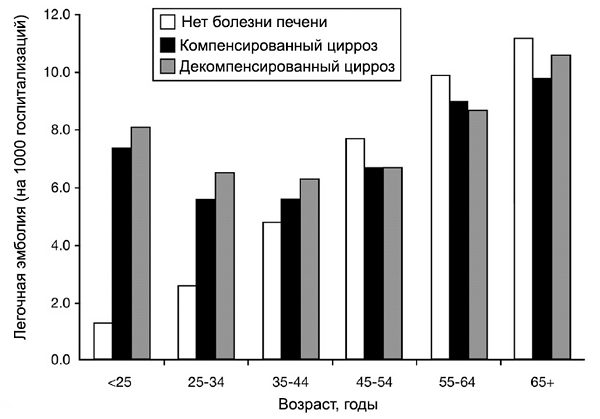
Wu H, Nguyen G. Clin Gastroenterol Hepatol. 2010;8:800–5.
КРИТЕРИИ Baveno VI
Критерии низкой вероятности варикоза вен пищевода и нецелесообразности эндоскопии:
• Тромобоциты >150•109/л.
• Плотность печени при эластографии <20 кПа.
КЛАССИФИКАЦИЯ ЦИРРОЗА ПЕЧЕНИ
• Этиология: вирусы гепатита В или С, алкоголь…
• Тяжесть: шкалы MELDNa, Child-Turcotte-Pugh.
• Варикоз пищевода, желудка: малый (<5 мм), большой (>5 мм).
• Морфология: крупноузловой, мелкоузловой, смешанный.
Спонтанный бактериальный перитонит
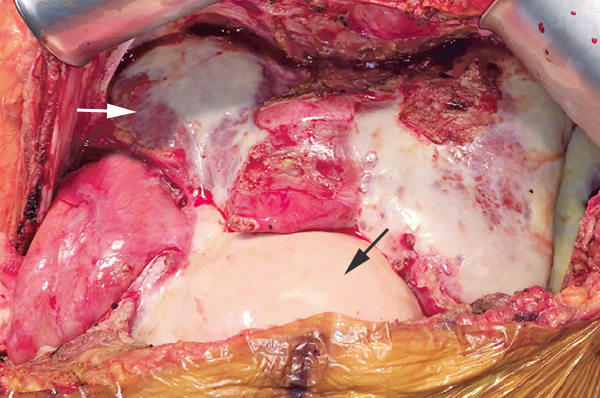
Правая доля при терминальной болезни печени (светлая стрелка), фибриновый налет на кишечнике (темная стрелка). Lancet. 2017;389.
ФОРМУЛИРОВКА ДИАГНОЗА
Ds: Цирроз печени вирусный (HCV), класс В, портальная гипертензия (большой варикоз пищевода, асцит), печеночная энцефалопатия 2 степени, кардиомиопатия. [K70.3]
Осложнение: Рецидивирующее пищеводное кровотечение. Бактериальный перитонит.
Ds: Цирроз печени алкогольный, класс А, портальная гипертензия (малый варикоз пищевода). [K70.3]
Ds: Цирроз печени неуточненный, декомпенсация печеночной недостаточности. [K74.6]
Асцит при циррозе печени
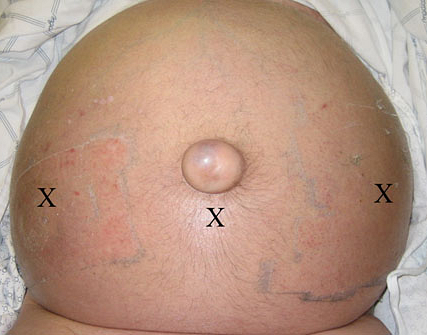
ПОКАЗАНИЯ К ПАРАЦЕНТЕЗУ (AASLD, BGS, WGO)
• Для уточнения причины ухудшения (спонтанный перитонит).
• Напряженный асцит с дыхательной недостаточностью, дискомфортом, рвотой при стабильной гемодинамике.
• Выраженный или рефрактерный к диуретической терапии асцит.
• Невысокий риск геморрагий: протромбиновый индекс >40%, МНО <2–3, тромбоциты >25–40•109/л.
• Отсутствие острого живота.
Асцит при сонографии
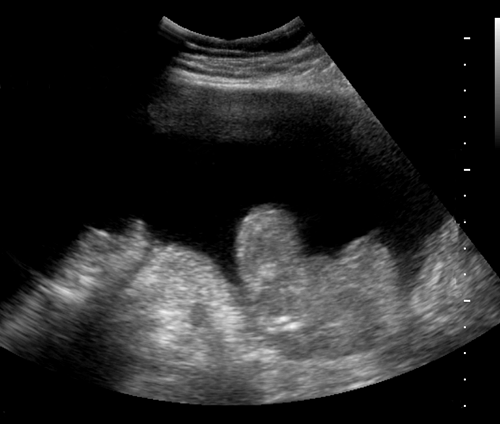
Парацентез
• Однократно 5–10 л.
• Можно 10 л за 1 час с введением 6 г бессолевого альбумина (хуже 150 мл декстрана) на 1 л удаляемой жидкости.
• Не более 6 л, если креатинин >265 мкмоль/л, билирубин >170 мкмоль/л, альбумин <30 мг/л.
Лечение портальной гипертензии
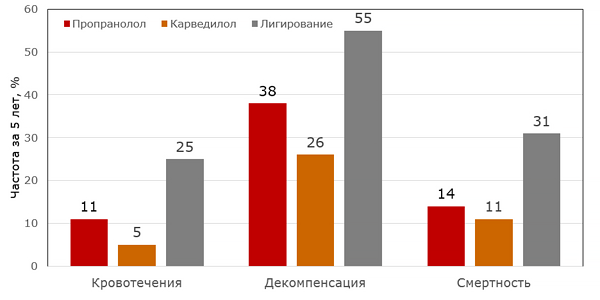
Reiberger T, et al. Gut 2013;62:1634–41.
ЛЕЧЕНИЕ ЦИРРОЗА ПЕЧЕНИ (AASLD, BSG)
• Лечение причины: противовирусная терапия, отказ от алкоголя и лечение зависимости.
• Асцит: ограничение соли (Na 2 г/сут), неселективные бета–блокаторы, спиронлактон 200–400 мг/сут, фуросемид <160 мг/сут, альбумин человеческий (ANSWER), парацентезы, перитонеовенозный шунт.
• Профилактика кровотечений: бета–блокаторы (титровать пропранолол 20–160 мг 2 раза, карведилол 6.25–25 мг 2 раза), лигирование узлов, склеротерапия.
• Лечение кровотечений: переливание эритроцитов, свежезамороженная плазма, тромбомасса (<50•109/л), антифибринолитики (ε-аминокапроновая или транексамовая кислота), вазопрессоры (октреотид, терлипрессин), лигирование узлов, баллонная тампонада.
• Тромбоцитопения: кортикостероиды, спленэктомия, стимуляторы гемопоэза (элтромбопаг, ромиплостим).
• Гепаторенальный синдром (b тип): инфузия альбумина, октреотид, мидодрин, норадреналин.
• Профилактика бактериального перитонита: норфлоксацин 400 мг, рифаксимин 1200 мг однократно, постоянно.
• Бактериальный перитонит: в/в ципрофлоксацин 400 мг 2 раза, цефотаксим 2 г 3 раза, цефтриаксон 1 г 1 раз, офлоксацин 400 мг 2 раза per os.
• Печеночная недостаточность: ограничение белка (1 г/кг/сут), лактулоза 15–30 мл 3 раза, сифонные клизмы.
• Трансплантация печени: ≥15 по MELD.
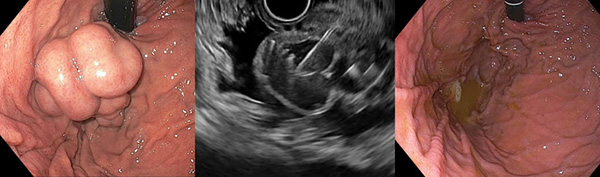
Лигирование венозных узлов в пищеводе
ПОКАЗАНИЯ К ПРОФИЛАКТИКЕ БАКТЕРИАЛЬНОГО ПЕРИТОНИТА (AASLD, EASL)
• Острое гастроинтестинальное кровотечение (7 сут).
• Низкий уровень белка в асцитической жидкости (<1.5 г/дл) + дисфункция почек (креатинин ≥106 мкмоль/л, Na ≤130 мкмоль/л) или печеночная недостаточность (шкала Чайлд ≥9 и билирубин ≥154 мкмоль/л).
• Бактериальный перитонит в анамнезе.
Динамика смертности при трансплантации печени
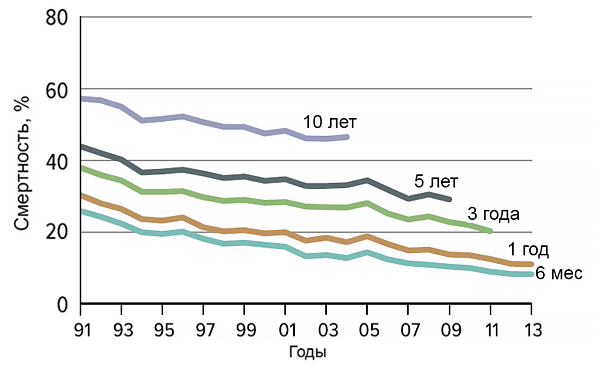
Fayek S, et al. Am J Transplant. 2016;16:3093–104.
СКРИНИНГ ГЕПАТОКАРЦИНОМЫ И ВАРИКОЗА ВЕН ПИЩЕВОДА
• Фиброэзофагогастроскопия: каждые 2–3 года (компенсированный цирроз и нет варикоза), каждые 1–2 года (малый варикоз), ежегодно (декомпенсированный цирроз).
• Альфа-фетопротеин, сонография печени: каждые 6 мес.
• Компьютерная томография, магнитно-резонансная томография.
• Биопсия печени.
ПОКАЗАНИЯ ДЛЯ ТРАНСПЛАНТАЦИИ ПЕЧЕНИ (AASLD)
• Острая печеночная недостаточность.
• Осложнения цирроза печени: асцит, хроническая желудочно-кишечная кровопотеря вследствие портальной гипертензивной гастропатии, энцефалопатия, рак печени, рефрактерные варикозные кровотечения, дисфункция синтеза.
• Печеночные метаболические нарушения с системными проявлениями: дефицит a1-антитрипсина, семейный амилоидоз, болезнь накопления гликогена, гемохроматоз, первичная оксалурия, болезнь Вильсона.
• Системные осложнения хронической болезни печени: гепатопульмональный синдром, портопульмональная гипертензия.
Источник
Е.Н. Широкова
Эпидемиология. Заболевание встречается с частотой 19-151 на 1.000.000 населения. Ежегодно регистрируется 4-15 новых случаев заболевания на 1.000.000. В структуре мировой смертности от всех циррозов печени доля первичного билиарного цирроза (ПБЦ) составляет почти 2%.
ПБЦ болеют люди всех рас. Среди больных 90-95% составляют женщины. Заболевание обычно начинается в возрасте 30-70 лет.
Генетика. Генетические факторы, очевидно, играют определенную роль в возникновении ПБЦ, хотя заболевание не наследуется по доминантному или рецессивному типу. Описаны семейные случаи заболеваемости ПБЦ. Вероятность заболевания в семьях, где имеется больной ПБЦ, в 1000 раз больше, чем в общей популяции.
Данные об отсутствии развития ПБЦ у одного из близнецов, если второй болен, позволяют предположить необходимость запускающего фактора у генетически восприимчивого индивидуума. Имеется слабая связь между ПБЦ и антигенами гистосовместимости HLA DR8 и геном DQB1.
Иммунологические нарушения. Большое число иммунных нарушений у больных ПБЦ указывает на то, что заболевание вызвано некоторыми нарушениями иммунной регуляции. Однако прямого подтверждения этой гипотезы нет.
Антимитохондриальные антитела (АМА) обнаруживаются у 95% больных ПБЦ. Они не оказывают влияния на течение заболевания и не являются специфичными для ПБЦ, т.к. встречаются у некоторых больных с аутоиммунным и лекарственным гепатитом.
АМА — это семейство антител, которое взаимодействует с различными антигенами митохондрий. Специфичными для ПБЦ считаются анти-М2. Они направлены непосредственно против дигидролипоилацетилтрансферазы (Е2) пируватдегидрогеназного комплекса внутренней мембраны митохондрий (рис. 14.1).

Рис. 14.1. Схема пируват — дегидрогеназного комплекса
У больных ПБЦ также определяли другие АМА: анти-М4, анти-М8 и анти-М9. Однако недавно проведенные исследования с использованием в качестве антигенов высоко очищенных клонированных человеческих белков митохондрий не подтвердили существование этих антител. Они могут быть артефактами ранее используемых технологий.
Связь между АМА и иммунным повреждением желчных протоков остается неясной. Е2 антигены пируватдегидрогеназного комплекса стимулируют продукцию интерлейкина 2 мононуклеарами периферической крови и Т-клетками, клонированными из биопсийного материала печени больных ПБЦ. Молекула с некоторыми антигенными признаками Е2 компонента пируватдегидрогеназного комплекса аберрантно экспрессируется на поверхности эпителия желчных протоков больных ПБЦ, но не обнаруживается в контрольной группе или у пациентов с первичным склерозирующим холангитом (ПСХ). Пируватдегидрогеназный Е2 компонент начинает экспрессироваться эпителиальными клетками желчных протоков до экспрессии двух других антигенов, которые необходимы для цитотоксичности Т-лимфоцитов: антигенов HLA II-го класса и фактора ВВ1/В7.
Митохондриальные антигены не являются специфичными для определенного типа ткани. Не установлено корреляции между титром АМА и тяжестью течения ПБЦ. Высокие титры АМА могут быть воспроизведены у экспериментальных животных путем иммунизации чистой человеческой пируватдегидрогеназой. Однако у этих животных не развивается заболевание печени.
У больных ПБЦ обнаруживают и другие циркулирующие антитела: антинуклеарные, антитиреоидные, лимфоцитотоксичные, к ацетилхолиновым рецепторам, к тромбоцитам, к антирибонуклеопротеиновому антигену Ro, антигистоновые, антицентромерные.
Определяются высокие уровни сывороточного иммуноглобулина М (IgM), отличающегося высокой иммунной реактивностью и криопреципитацией. Тесты на иммунные комплексы могут быть ложноположительными из-за высоких уровней иммуноглобулинов сыворотки.
ПБЦ может сочетаться с другими аутоиммунными заболеваниями: с тиреоидитом, гипотиреозом, ревматоидным артритом, CREST синдромом (C — кальциноз, R — синдром Рейно, E — нарушение моторики пищевода, S — склеродактилия, T — телеангиоэктазии), синдромом Шегрена, склеродермией.
У больных имеются изменения клеточного иммунитета: нарушение Т-клеточной регуляции, уменьшение циркулирующих Т-лимфоцитов, секвестрация Т-лимфоцитов внутри печеночных портальных триад, отрицательные кожные пробы гиперчувствительности замедленного типа.
Патогенез. По-видимому, существуют два взаимосвязанных процесса, вызывающих повреждение печени и проявляющихся клиническими признаками ПБЦ (схема 14.1).
Первый процесс — это хроническая деструкция мелких желчных протоков, очевидно, вызываемая активированными лимфоцитами. Вероятно, начальное повреждение обусловлено цитотоксическими Т-лимфоцитами. Клетки желчных протоков у больных ПБЦ экспрессируют повышенное количество антигенов I-го класса комплекса гистосовместимости HLA-A, HLA-B, HLA-C и антигенов II-го класса HLA-DR, по сравнению с нормальными клетками желчных протоков. Повреждения желчных протоков сходны с нарушениями, вызываемыми цитотоксическими Т-лимфоцитами, такими как болезнь трансплантат против хозяина и реакция отторжения аллогенного трансплантата.
Второй процесс— химическое повреждение гепатоцитов в тех областях печени, где дренирование желчи нарушено вследствие повреждения мелких желчных протоков и проявляется уменьшением их числа. Происходит задержка желчных кислот, билирубина, меди и других веществ, которые в норме секретируются или экскретируются в желчь. Увеличенная концентрация некоторых из них, таких как желчные кислоты, может вызвать дальнейшее повреждение клеток печени.
Симптомы ПБЦ обусловлены длительно существующим холестазом. Разрушение желчных протоков, в конечном счете, ведет к портальному воспалению, фиброзу, и в итоге к циррозу и печеночной недостаточности.
Морфология. Макроскопически печень по мере нарастания холестаза приобретает зеленоватую окраску, на стадии цирроза становится мелкобугристой, окрашенной в темно-зеленый цвет.
ПБЦ – длительно текущее заболевание, которое характеризуется деструкцией внутрипеченочных желчных протоков с уменьшением их числа, пролиферацией холангиол (как попытка компенсации утраты желчных протоков), воспалительной клеточной инфильтрацией портальных трактов и долек печени, образованием гранулем, а в дальнейшем развитием холестаза, деструкции печеночной ткани, нарастанием фиброзных изменений с формированием мелкоузлового цирроза в финале.
Выделяют четыре морфологические стадии ПБЦ:
- I – хронического негнойного деструктивного холангита (дуктальная стадия),
- II – пролиферация холангиол и перидуктального фиброза (дуктулярная стадия),
- III – фиброза стромы при наличии воспалительной инфильтрации паренхимы печени,
- IV – цирроза печени.
В I стадию происходит разрушение междольковых желчных протоков в зоне гранелематозного воспаления. Разрушающиеся желчные протоки в виде муфт окружены клетками воспалительного инфильтрата, преимущественно лимфоцитами, портальные тракты густо инфильтрированы лимфоцитами, плазмоцитами, макрофагами, в небольшом количестве эозинофилами (рис. 14.2).

Рис. 14.2. Первичный билиардный цирроз печени (биоптат печени, окраска г/э, х400). Деструктивный холангит. Рядом с протоком — гранулема, лимфоидный инфильтрат
Во II стадию продолжающаяся деструкция желчных протоков приводит к уменьшению их числа, появляются портальные тракты без желчных протоков (“пустой” портальный тракт), вокруг сохранившихся протоков разрастается волокнистая соединительная ткань. Уменьшение числа желчных протоков в портальных трактах – важный диагностический признак ПБЦ. Происходит также пролиферация холангиол. Возникают признаки холестаза. Развитие портальной гипертензии в этот сравнительно ранний период (I – II стадии ПБЦ) объясняют фиброзом и клеточной инфильтрацией портальных трактов (рис. 14.3).

Рис. 14.3. Первичный билиардный цирроз печени (биоптат печени, окраска г/э, х100). Фиброзные изменения и воспалительная клеточная инфильтрация, желчные протоки не выявляются (дуктопения)
В III стадии усиливается химическое повреждение, некроз гепатоцитов вследствие нарушения внутрипеченочного оттока желчи и воспалительная клеточная инфильтрация долек, появляются порто-портальные и порто-центральные септы, которые окружают формирующиеся ложные дольки.
IV стадия, которая может наступить спустя много лет от начала заболевания, выявляется сформированный мелкоузловой цирроз печени.
- 14.1. Клинические проявления
- 14.2. Лечение
Источник