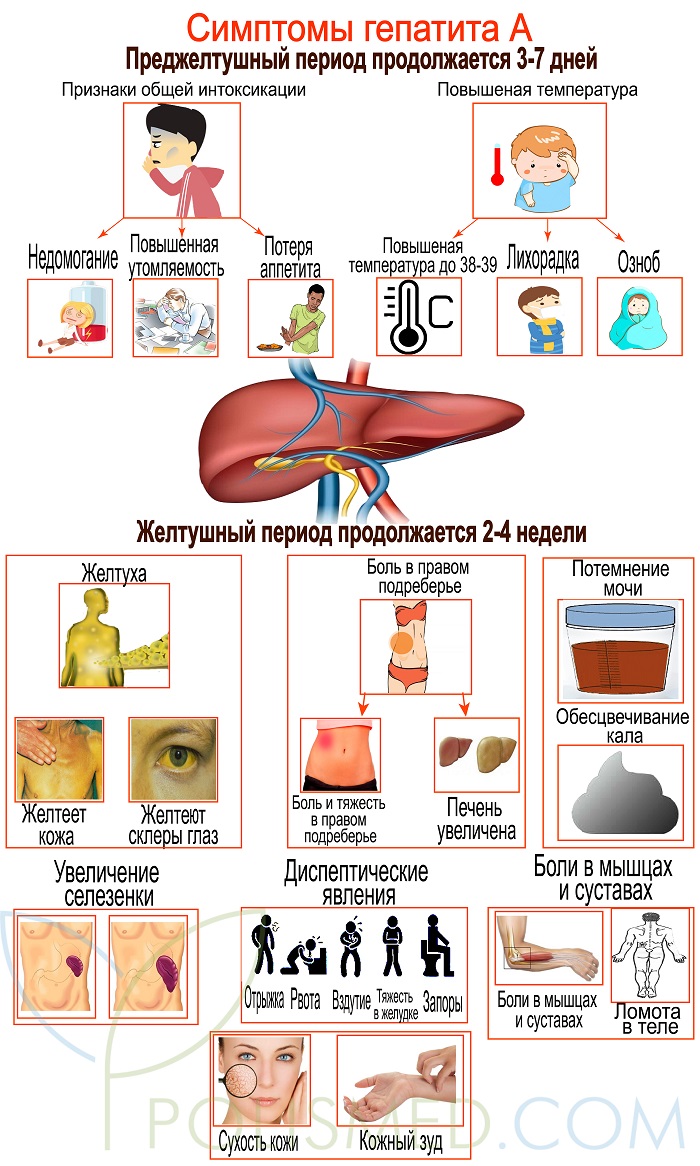
Порядок проведения обследования на гепатиты
Об организации обследования населения на ВИЧ-инфекцию, вирусные гепатиты B и С
(с изменениями на 10 октября 2008 года)
________________________________
Документ с изменениями, внесенными:
Приказом министерства здравоохранения Хабаровского края от 21 апреля 2006 года N 124
Приказом министерства здравоохранения Хабаровского края от 10 октября 2008 года N 319
________________________________
Во исполнение Федерального закона от 30.03.1995 N 38-ФЗ (в ред. от 22.08.2004) «О предупреждении распространения в Российской Федерации заболевания, вызываемого вирусом иммунодефицита человека (ВИЧ-инфекции)», Постановления Правительства РФ от 31.12.2005 N 870 «Об обеспечении государственных и муниципальных учреждений здравоохранения за счет средств федерального бюджета диагностическими препаратами в целях профилактики, выявления и лечения лиц, инфицированных вирусами иммунодефицита человека и гепатитов B и С, оборудованием и расходными материалами для неонатального скрининга», Закона Хабаровского края от 29 декабря 2004 г. N 235 «О краевой целевой программе «Основные направления по предупреждению распространения в Хабаровском крае заболевания, вызываемого вирусом иммунодефицита человека (ВИЧ-инфекции), на 2005 — 2009 годы» и с целью установки региональных стандартов проведения лабораторной диагностики ВИЧ-инфекции, вирусных гепатитов B и С в учреждениях здравоохранения края утвердить:
Перечень учреждений здравоохранения, имеющих право проведения лабораторных исследований на ВИЧ-инфекцию и вирусные гепатиты B и С в рамках финансирования из федерального, краевого и муниципального бюджетов на территории Хабаровского края (приложение 1).
2. Руководителям учреждений здравоохранения Хабаровского края:*
________________
*Нумерация пунктов дана в соответствии с официальным текстом. — Примечание “КОДЕКС”.
2.1. Организовать проведение диагностики ВИЧ-инфекции и вирусных гепатитов B и С в строгом соответствии с требованиями нормативных правовых документов, определяющих стандарт обследования и порядок проведения соответствующих лабораторных исследований (приложение 2).
3. Главному врачу ГУЗ «Центр по профилактике и борьбе со СПИД и инфекционными заболеваниями» министерства здравоохранения Хабаровского края Жердевой А.И. обеспечить:
3.1. формирование сводной заявки на диагностикумы для выявления ВИЧ-инфекции, вирусных гепатитов B и С с учетом потребности учреждений здравоохранения Хабаровского края, утвержденных приложением 1 настоящего приказа;
3.2. учреждения здравоохранения Хабаровского края, оказывающие экстренную медицинскую помощь, — тест-системами для экспресс-диагностики ВИЧ-инфекции;
3.3. действенный контроль за соблюдением в учреждениях здравоохранения Хабаровского края требований нормативных правовых актов, инструкций, регулирующих порядок проведения обследования населения с целью диагностики ВИЧ-инфекции и вирусных гепатитов B и С.
4. Заместителю министра здравоохранения — начальнику управления экономики, финансирования и технического контроля министерства здравоохранения Хабаровского края Новиковой Н.А. предусмотреть финансирование краевых учреждений здравоохранения согласно приложению 2, в пределах лимита средств, предусмотренных годовым бюджетом на эти цели.
5. Рекомендовать руководителям органов управления здравоохранением муниципальных образований Хабаровского края принять к руководству настоящий приказ и обеспечить его исполнение в подведомственных учреждениях здравоохранения.
6. Информацию о ходе выполнения приказа представлять в министерство здравоохранения Хабаровского края к 01.06. и 01.12. ежегодно.
7. Контроль за исполнением приказа возложить на заместителя министра здравоохранения Деркача А.Я.
Министр
Н.Д. Халилов
Приложение 1. Перечень учреждений здравоохранения, имеющих право проведения лабораторных исследований на вич-инфекцию и вирусные гепатиты B и C в рамках финансирования из федерального, краевого и муниципального бюджетов на территории Хабаровского края
Наименование учреждений здравоохранения | Виды исследований | ||
Первичная лабораторная диагностика | Арбитражные исследования | Мониторинг | |
1 | 2 | 3 | 4 |
ГУЗ «Центр по борьбе и профилактике со СПИД и инфекционными заболеваниями» министерства здравоохранения Хабаровского края | + | + | + |
ГУЗ «Краевая клиническая больница N 1» министерства здравоохранения Хабаровского края | + | ||
ГУЗ «Хабаровская краевая станция переливания крови» министерства здравоохранения Хабаровского края | + | ||
ГУЗ «Амурский центр организации специализированных видов медицинской помощи» министерства здравоохранения Хабаровского края | + | ||
ГУЗ «Верхнебуреинский центр организации специализированных видов медицинской помощи» министерства здравоохранения Хабаровского края | + | ||
ГУЗ «Вяземский центр организации специализированных видов медицинской помощи» министерства здравоохранения Хабаровского края | + | ||
МУЗ «Станция переливания крови» отдела здравоохранения администрации г. Комсомольска-на-Амуре | + | + | |
МУЗ «Центральная районная больница» муниципального района им. Лазо | + | ||
МУЗ «Троицкая центральная районная больница» администрации Нанайского района | + | ||
МУЗ «Центральная районная больница» администрации Николаевского-на-Амуре района | + | + | |
МУЗ «Центральная районная больница» администрации Охотского района | + | ||
МУЗ «Районная больница» Совгаванского муниципального района | + | ||
МУЗ «Центральная районная больница N 1» с. Богородское | + | ||
МУЗ «Центральная районная больница Ванинского района» | + | ||
Лаборатория управления федеральной службы исполнения наказаний | + | ||
Государственное учреждение здравоохранения «Перинатальный центр» министерства здравоохранения Хабаровского края | |||
ГУЗ «Территориальный консультативно-диагностический центр» министерства здравоохранения Хабаровского края | + | — | + |
Заместитель министра
А.Я. Деркач
Приложение 2. Перечень нормативно-правовых актов, регламентирующих порядок проведения обследования населения с целью диагностики ВИЧ-инфекции и вирусных гепатитов B и C, и санитарных правил
Приложение 2
к приказу
Министерства здравоохранения
Хабаровского края
от 07 марта 2006 года N 68
1. Федеральный закон от 30.03.1995 N 38-ФЗ (в ред. от 22.08.2004) «О предупреждении распространения в Российской Федерации заболевания, вызываемого вирусом иммунодефицита человека (ВИЧ-инфекции)».
2. Постановление Правительства РФ от 31.12.2005 N 870 «Об обеспечении государственных и муниципальных учреждений здравоохранения за счет средств федерального бюджета диагностическими препаратами в целях профилактики, выявления и лечения лиц, инфицированных вирусами иммунодефицита человека и гепатитов B и С, оборудованием и расходными материалами для неонатального скрининга».
3. Закон Хабаровского края от 29.12.2004 N 235 «О краевой целевой программе «Основные направления по предупреждению распространения в Хабаровском крае заболевания, вызываемого вирусом иммунодефицита человека (ВИЧ-инфекции), на 2005 — 2009 годы».
4. Постановление Губернатора Хабаровского края от 30.03.2005 N 71 «О реализации Закона Хабаровского края от 29 декабря 2004 г. N 235 «О краевой целевой программе «Основные направления по предупреждению распространения в Хабаровском крае заболевания, вызываемого вирусом иммунодефицита человека (ВИЧ-инфекции), на 2005 — 2009 годы».
5. Санитарные правила СП 1.2.731-99 «Безопасность работы с микроорганизмами 3 — 4 групп патогенности и гельминтами», 1999 г.
6. Санитарно-эпидемиологические правила СП 3.1.958-99 «Профилактика вирусных гепатитов. Общие требования к эпидемиологическому надзору за вирусными гепатитами», 2000 г.*
_______________
*Вероятно, ошибка оригинала. Следует читать » СП 3.1.958-00″. — Примечание «КОДЕКС».
7. Санитарно-эпидемиологические правила СП 3.3.2.1248-03 «Условия транспортирования и хранения медицинских иммунобиологических препаратов», 2003 г.
8. Отчетная форма федерального статистического наблюдения N 4 «Сведения о результатах обследования крови на антитела к ВИЧ», утвержденная Постановлением Госкомстата России 05.05.1999 N 30.
9. Приказ МЗ СССР от 12.07.1989 N 408 «О мерах по снижению заболеваемости вирусными гепатитами в стране».
10. Приказ Минздравмедпрома РФ от 16.08.1994 N 170 «О мерах по совершенствованию профилактики и лечения ВИЧ-инфекции в Российской Федерации».
11. Приказ Минздравмедпрома РФ от 30.10.1995 N 295 «О введении в действие правил проведения обязательного медицинского освидетельствования на ВИЧ и перечня работников отдельных профессий, производств, предприятий и организаций, которые проходят обязательное медицинское освидетельствование на ВИЧ».
12. Приказ МЗ РФ от 07.08.2000 N 312 «О совершенствовании организационной структуры и деятельности учреждений по профилактике и борьбе со СПИД».
13. Приказ МЗ РФ от 30.07.2001 N 292 «Об использовании иммуноферментных тест-систем для выявления антител к ВИЧ в сыворотке крови человека».
14. Приказ МЗ РФ от 21.10.2002 N 322 «О применении в практике здравоохранения иммуноферментных тест-систем для выявления поверхностного антигена вируса гепатита B (HBsAg) и антител к вирусу гепатита С (анти-ВГС) в сыворотке крови человека».
15. Приказ МЗ РФ от 19.12.2003 N 606 «Об утверждении инструкции по профилактике передачи ВИЧ-инфекции от матери ребенку и образца информированного согласия на проведение химиопрофилактики ВИЧ».
16. Приказ МЗ и социального развития РФ от 13.08.2004 N 77 «Об утверждении стандарта медицинской помощи больным ВИЧ-инфекцией».
17. Приказ МЗ и социального развития РФ от 23.11.2004 N 260 «Об утверждении стандарта медицинской помощи больным хроническим гепатитом B, хроническим гепатитом С».
18. Приказ МЗ и социального развития РФ от 30.05.2005 N 374 «Об утверждения стандарта медицинской помощи детям, больным ВИЧ-инфекцией».
19. Приказ МЗ и социального развития РФ от 30.05.2005 N 375 «Об утверждении стандарта профилактики передачи ВИЧ-инфекции от матери ребенку».
20. Приказ МЗ и СР от 05.12.2005 N 757 «О неотложных мерах по организации обеспечения лекарственными препаратами больных ВИЧ-инфекцией».
21. Приказ МЗ ХК от 16.12.2005 N 366 «О совершенствовании мероприятий по предупреждению распространения ВИЧ-инфекции в крае на 2005 — 2009 годы».
22. Приказ МЗ ХК от 08.02.2006 N 32 «О мерах по организации обеспечения лекарственными средствами и тест-системами для диагностики, профилактики, лечения лиц, инфицированных вирусами иммунодефицита человека и гепатитов B и С».
Заместитель министра
А.Я. Деркач
Текст документа сверен по:
Официальная рассылка
Редакция документа
подготовлена «Софтинформбюро»
Источник
Медицинский персонал обследуется при приеме на работу и далее 1 раз в год, дополнительно — по клиническим и эпидемиологическим показаниям.
Документ «МУ 3.1.3342-16. 3.1. Профилактика инфекционных болезней. Эпидемиологический надзор за ВИЧ-инфекцией. Методические указания» (утв. Главным государственным санитарным врачом РФ 26.02.2016) в Приложении № 1 определяет контингент лиц, подлежащих обязательному медицинскому освидетельствованию на ВИЧ-инфекцию.
↯
Больше статей в журнале
«Главная медицинская сестра»
Активировать доступ
Медицинские работники проходят обследование при поступлении на работу и в дальнейшем 1 раз в год.
Врачи, средний и младший медицинский персонал лабораторий, которые осуществляют обследование населения на ВИЧ-инфекцию и исследование крови и биологических материалов, полученных от лиц, инфицированных вирусом иммунодефицита человека — при поступлении на работу и при периодических медицинских осмотрах.
Аналогично Постановление Главного государственного санитарного врача РФ от 28.02.2008 № 14 «Об утверждении санитарно-эпидемиологических правил СП 3.1.1.2341-08» устанавливает в Приложении, что медицинский персонал обследуется при приеме на работу и далее 1 раз в год, дополнительно — по клиническим и эпидемиологическим показаниям.
Также Постановление Главного государственного санитарного врача РФ от 22.10.2013 № 58 «Об утверждении санитарно-эпидемиологических правил СП 3.1.3112-13 «Профилактика вирусного гепатита C» в Приложении № 1 содержит контингенты, подлежащие обязательному обследованию.
Персонал медицинских организаций — при приеме на работу и далее 1 раз в год, дополнительно — по показаниям.
Дополнительно сообщаем, что периодичность осмотров, участие врачей-специалистов, лабораторные и функциональные исследования для разных работников (должностей) зависят от воздействия конкретных вредных и (или) опасных производственных факторов.
Установить их можно исключительно по результатам проведения СОУТ.
Медицинские работники должны проходить медицинский осмотр 1 раз в год как медицинский персонал ЛПУ в соответствии с п. 17 Приложения № 2 Приказа Минздравсоцразвития России от 12.04.2011 № 302н.
Пункт 16 раздела 3 Приложения № 3 к Приказу № 302н определяет, что периодические осмотры проводятся не реже чем в сроки, указанные в Перечне факторов и Перечне работ.
То есть годичный срок является для медицинских работников предельным в отношении действительности результатов медосмотра.
Нельзя проходить осмотр реже одного раза в год, чаще не запрещено.
Материал проверен экспертами Актион Медицина

Журнал регистрации и контроля ультрафиолетовой бактерицидной установки
посмотреть/скачать>>
Читайте бесплатно в системе
Главная медсестра:

Внедрите требования Росздравнадзора по внутреннему контролю качества
Журнал учета отходов классов Б и В в подразделении
Составьте идеальный график уборок для каждого помещения
Медизделия для противошоковой укладки: памятка для медсестер
9 обязательных разделов программы производственного контроля
К какому классу опасности отнести отходы
Источник
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
ПРИКАЗ
от 30 октября 2000 г. N 384
О ПРИМЕНЕНИИ В ПРАКТИКЕ ЗДРАВООХРАНЕНИЯ ИММУНОФЕРМЕНТНЫХ ТЕСТ — СИСТЕМ ДЛЯ ВЫЯВЛЕНИЯ ПОВЕРХНОСТНОГО АНТИГЕНА ВИРУСА ГЕПАТИТА В (HBsAg) И АНТИТЕЛ К ВИРУСУ ГЕПАТИТА С (анти-ВГС) В СЫВОРОТКЕ КРОВИ ЧЕЛОВЕКА
В целях принятия дополнительных мер по предотвращению распространения гепатитов В и С и улучшению качества иммунобиологических препаратов, предназначенных для лабораторной диагностики вирусных гепатитов В и С с 28 марта по 1 июня 2000 года были проведены сравнительные испытания диагностических иммуноферментных тест — систем для выявления поверхностного антигена вируса гепатита В (HBsAg) и антител к вирусу гепатита С (анти-ВГС) в сыворотке крови человека.
По результатам испытаний установлено, что за период прошедший со времени проведения предыдущих сравнительных испытаний, качество отечественных диагностических тест систем значительно улучшилось, их чувствительность повысилась в 2 раза. Более того, анализ результатов испытаний выявил потенциальные возможности отечественных производителей на современном этапе развития технологии производства тест — систем для диагностики HBsAg и анти-ВГС обеспечить их еще более высокую чувствительность и специфичность.
Эпидемическая обстановка, сложившаяся в Российской Федерации по вирусным парентеральным гепатитам, диктует необходимость дальнейшего повышения чувствительности и специфичности таких диагностических тест — систем.
На основании заключения комиссии по организации и проведению сравнительных испытаний тест — систем для выявления поверхностного антигена вируса гепатита В (HBsAg) и антител к вирусу гепатита С (анти-ВГС) в сыворотке крови человека, в целях принятия дополнительных мер по предотвращению распространения вируса гепатита В и С при переливании крови и ее компонентов, трансплантации органов и тканей, а также повышения качества лабораторной диагностики вирусных гепатитов В и С. приказываю:
1. Руководителям органов управления здравоохранением субъектов Российской Федерации:
1.1. Обеспечить проведение обследования доноров крови, органов и тканей человека, больных острыми и хроническими гепатитами на наличие HBsAg и анти-ВГС с помощью тест — систем, указанных в приложениях 1 и 4. При выборе тест — систем для выявления HBsAg отдавать преимущество диагностическим препаратам с более высокой заявляемой чувствительностью.
1.2. Запретить с 1 января 2002 года применение тест — систем для выявления HBsAg, с чувствительностью ниже 0,25 нг/мл.
1.3. В случае установления фактов поставки тест — систем для выявления HBsAg и анти-ВГС неудовлетворительного качества, а также несоблюдения условий их транспортировки и хранения, направлять информацию в Департамент госсанэпиднадзора Минздрава России и ГИСК им. Л.А. Тарасевича.
1.4. Использовать для проведения анализа по подтверждению наличия HBsAg и анти-ВГС конфирматорные тест — системы (приложения 3 и 5). Постановка окончательного лабораторного диагноза без подтверждения в одном из конфирматорных тестов запрещается.
1.5. Исключить использование диагностических иммуноферментных тест — систем для выявления HBsAg и анти-ВГС, не имеющих разрешение Минздрава России на применение.
2. Главным врачам Центров госсанэпиднадзора в субъектах Российской Федерации:
2.1. Обеспечить действенный контроль за использованием на местах тест — систем для выявления HBsAg и анти-ВГС в соответствии с настоящим приказом.
2.2. В случае использования для диагностики HBsAg и анти-ВГС тест — систем, не разрешенных Минздравом России, принимать срочные меры по их запрещению. О каждом выявленном случае немедленно информировать Департамент госсанэпиднадзора Минздрава России.
2.3. Обеспечить постоянный контроль за транспортировкой и хранением тест — систем для диагностики HBsAg и анти-ВГС в соответствии с инструкциями по применению и требованиями санитарных правил СП 3.3.2.028-95 «Условия транспортировки и хранения медицинских иммунобиологических препаратов».
3. Департаменту госсанэпиднадзора Минздрава России организовать и провести следующие сравнительные испытания в 1 квартале 2002 года.
4. Государственному НИИ стандартизации и контроля медицинских иммунобиологических препаратов им. Л.А. Тарасевича:
4.1. Завершить в первом квартале 2001 года подготовку и аттестацию панелей сывороток крови, содержащих HBsAg в различных концентрациях с учетом его субтиповой принадлежности (субтип «ad» и «аy»). При подготовке и аттестации новых серий панелей сывороток крови, содержащих антитела к ВГС, руководствоваться результатами генотипирования сывороток и данными о распространенности различных генотипов ВГС на территории Российской Федерации.
4.2. Обеспечить проведение выборочного предреализационного контроля тест — систем для диагностики вирусных гепатитов В и С.
4.3. Внедрить в лабораторную практику для оценки чувствительности тест — систем по выявлению HBsAg Отраслевой стандартный образец HBsAg вируса гепатита В — ОСО 42-28-311-00.
5. Контроль за выполнением настоящего приказа возложить на Первого заместителя Министра Г.Г.Онищенко.
Министр
Ю.Л.ШЕВЧЕНКО
Приложение N 1
к приказу Министерства
здравоохранения
Российской Федерации
от 30.10.2000 г. N 384
ПЕРЕЧЕНЬ
ДИАГНОСТИЧЕСКИХ ПРЕПАРАТОВ ДЛЯ ВЫЯВЛЕНИЯ АНТИТЕЛ К ВИРУСУ ГЕПАТИТА С В ИММУНОФЕРМЕНТНОМ МЕТОДЕ, РАЗРЕШЕННЫХ ДЛЯ ОБСЛЕДОВАНИЯ ДОНОРОВ КРОВИ, ОРГАНОВ И ТКАНЕЙ ЧЕЛОВЕКА, БОЛЬНЫХ ОСТРЫМИ И ХРОНИЧЕСКИМИ ГЕПАТИТАМИ И СКРИНИНГА НАСЕЛЕНИЯ
| N пп | Производитель | Название диагностикума |
| 1. | НПО «Диагностические системы» г. Н. Новгород | «ИФА-АНТИ-HCV» (субстратные системы ОФД и ТМБ). |
| 2. | Фирма «ИмБио» г. Н. Новгород | «ИФА-АНТИ-ВГС» (субстратные системы ОФД и ТМБ). |
| 3. | НПП «АКВАПАСТ» г. С. — Петербург | «Аквагеп-С-Ат-2» (субстратные системы ОФД и ТМБ) |
| 4. | «ПКБ им. И.И.Мечникова» г. Москва | «ГепаСкан» |
| 5. | «ПКБ им. И.И.Мечникова» г. Москва | «ГепаСкрин» |
| 6. | ЗАО БК «Биосервис» | «ГепаСкан» |
| 7. | ЗАО БК «Биосервис» | «ГепаСкрин» |
| 8. | ГП НИИ им. Пастера г. С. — Петербург | «ИФА для выявления антител к ВГС» |
| 9. | ЗАО «МБС» г. Новосибирск | «ВГС-ДСМ» (субстратные системы ОФД и ТМБ) |
| 10. | Институт им. Пастера г. С. — Петербург | «ИФА-АНТИ-ВГС» (субстратные системы ОФД и ТМБ) |
| 11. | ЗАО «Вектор — Бест» г. Новосибирск | «РекомбиБест-анти ВГС» (субстратные системы ОФД и ТМБ) |
| 12. | ЗАО «Вектор — Бест» г. Новосибирск | «РекомбиБест-анти ВГС стрип» (субстратные системы ОФД и ТМБ) |
| 13. | Предприятие «ЭКОлаб» г. Электрогорск | «ЭКОлаб-ВГС» |
| 14. | ДГУ ЭПП «Вектор — Биальгам» г. Новосибирск | тм «ГепаСкрин » |
| 15. | ООО МЦ «Авиценна» г. Москва | «ВГС-ИФА-Авиценна» |
| 16. | BIO-RAD | «Monolisa R anti-HCV PLUS» |
| 17. | ABBOTT-Murex | «Murex anti-HCV» (version 4.0) |
Руководитель Департамента
госсанэпиднадзора
С.И.ИВАНОВ
Приложение N 2
к приказу Министерства
здравоохранения
Российской Федерации
от 30.10.2000 г. N 384
ПЕРЕЧЕНЬ
ДИАГНОСТИЧЕСКИХ ПРЕПАРАТОВ ДЛЯ ВЫЯВЛЕНИЯ АНТИТЕЛ К ВИРУСУ ГЕПАТИТА С В ИММУНОФЕРМЕНТНОМ МЕТОДЕ, РАЗРЕШЕННЫХ ДЛЯ ОБСЛЕДОВАНИЯ БОЛЬНЫХ ОСТРЫМИ И ХРОНИЧЕСКИМИ ГЕПАТИТАМИ И СКРИНИНГА НАСЕЛЕНИЯ
| N пп | Производитель | Название диагностикума |
| 1. | ЗАО «ДИАплюс» | «Анти-HCV ИФА» «ДИАплюс» |
| 2. | «ROCHE» | Cobas R Core Anti-HCV EIA |
| 3. | R АВВОТТ IM system x | НСV version 3.0 |
| 4. | R АВВОТТ AxSYM system | HCV version 3.0 |
| 5.<*> | ЗАО «Биоград» | «Иммунокомб II HCV» |
<*> Диагностический препарат «Иммунокомб II HCV» производства ЗАО «Биоград» может использоваться для обследования доноров крови, органов и тканей человека в ургентных ситуациях или при отсутствии лабораторного оборудования, когда невозможно использование для этих целей препаратов указанных в приложении 1.
Руководитель Департамента
госсанэпиднадзора
С.И.ИВАНОВ
Приложение N 3
к приказу Министерства
здравоохранения
Российской Федерации
от 30.10.2000 г. N 384
ПЕРЕЧЕНЬ
ДИАГНОСТИЧЕСКИХ ПРЕПАРАТОВ, ПРЕДНАЗНАЧЕННЫХ ДЛЯ ОПРЕДЕЛЕНИЯ СПЕКТРА АНТИТЕЛ К СТРУКТУРНЫМ И НЕСТРУКТУРНЫМ БЕЛКАМ ВИРУСА ГЕПАТИТА С (ПОДТВЕРЖДАЮЩИЕ ТЕСТЫ)
| N пп | Производитель | Название диагностикума |
| 1. | НПО «Диагностические системы» г. Н. Новгород | «ИФА-АНТИ-HCV-СПЕКТР» |
| 2.<*> | Фирма «ИмБио» г. Н. Новгород | Тест — система иммуноферментная для подтверждения положительных результатов на антитела к вирусу гепатита С (СПЕКТР- 4) |
| 3.<*> | ЗАО «Вектор — Бест» г. Новосибирск | «РекомбиБест анти-ВГС подтверждающий тест» |
| 4. | ЗАО «Вектор — Бест» г. Новосибирск | «РекомбиБест анти-ВГС- спектр» |
| 5.<*> | ЗАО «МБС» г. Новосибирск | «ВГС-ДСМ-подтверждающий тест» |
| 6. | «ORGANON TEKNIKA» | «LiaTek HCV-III» |
<*> После получения сертификата ГИСК.
Руководитель Департамента
госсанэпиднадзора
С.И.ИВАНОВ
Приложение N 4
к приказу Министерства
здравоохранения
Российской Федерации
от 30.10.2000 г. N 384
ПЕРЕЧЕНЬ
ДИАГНОСТИЧЕСКИХ ПРЕПАРАТОВ ДЛЯ ВЫЯВЛЕНИЯ ПОВЕРХНОСТНОГО АНТИГЕНА ВИРУСА ГЕПАТИТА В (HBsAg) В ИММУНОФЕРМЕНТНОМ МЕТОДЕ, РАЗРЕШЕННЫХ ДЛЯ ОБСЛЕДОВАНИЯ ДОНОРОВ КРОВИ, ОРГАНОВ И ТКАНЕЙ ЧЕЛОВЕКА, БОЛЬНЫХ ОСТРЫМИ И ХРОНИЧЕСКИМИ ГЕПАТИТАМИ, СКРИНИНГА НАСЕЛЕНИЯ
| N | Производитель | Название диагностикума | Чувствительность |
| 1. | НПО «Диагностические системы» г. Н. Новгород | «ИФА-HBsAg/м» (субстратная система ТМБ) | 0.1 нг/мл |
| 2. | ЗАО БК «Биосервис» | тм «Гепаскан HBsAg » | 0.1 нг/мл |
| 3. | ПКБ им. И. И. Мечникова г. Москва | тм «Гепаскан HBsAg » | 0.1 нг/мл |
| 4. | ЗАО «Вектор — Бест» г. Новосибирск | «Вектогеп B-HBs-антиген — стрип» (комплектация 2) | 0.1 нг/мл |
| 5. | ЗАО «Вектор — Бест» г. Новосибирск | «Вектогеп B-HBs-антиген» (комплектация 2) | 0.1 нг/мл |
| 6. | Предприятие «ЭКОлаб» г. Электрогорск | «Рекоматгеп В стрип» | 0.1 нг/мл |
| 7. | «НИАРМЕДИК ПЛЮС» | «ГепаСтрип» (субстратные системы ОФД и ТМБ) | 0.1 нг/мл |
| 8. | ЗАО «ДИАплюс» | «HBsAg ИФА»ДИАплюс»» | 0.1 нг/мл |
| 9. | BIO-RAD | R «Monolisa Ag HBs Plus» | 0.1 нг/мл |
| 10. | «ORGANON TEKNIKA» | «Hepanostika HBsAg UNI-FORM II» | 0.1 нг/мл |
| 11. | «ROCHE» | R Cobas Core HBsAg II EIA | 0.1 нг/мл |
| 12. | «ROCHE» | «ELECSYS HBsAg — immunoaassay»(aвтомат.) | 0.1 нг/мл |
| 13. | АВВОТТ R AxSYM system | HBsAg (V2) | 0.1 нг/мл |
| 14. | АВВОТТ R IМ system х | HBsAg (V2) | 0.1 нг/мл |
| 15. | НПО «Диагностические системы» г. Н. Новгород | «ИФА-HBsAg/м» (субстратная система ОФД) | 0.25 нг/мл |
| 16. | НПП «АКВАПАСТ» г. С. — Петербург» | «Аквагеп-В-Аг-1» (субстратная система ТМБ) | 0.25 нг/мл |
| 17. | Институт им. Пастера г. С. — Петербург | «ИФА-HBsAg» (субстратные системы ОФД и ТМБ) | 0.25 нг/мл |
| 18. | ГП НИИ им. Пастера г. С. — Петербург | «ИФА для выявления HBsAg» | 0.25 нг/мл |
| 19. | ЗАО «Вектор — Бест» г. Новосибирск | «Рекоматгеп В» | 0.25 нг/мл |
| 20. | ЗАО «Вектор — Бест» г. Новосибирск | «Вектогеп B-HBs-антиген — стрип» | 0.25 нг/мл |
| 21. | «АВВОТТ Murex» | «Murex HBsAg» | 0.25 нг/мл |
| 22. | Фирма «ИмБио» г. Н. Новгород | «ИФА-HBsAg» (субстратные системы ОФД и ТМБ) | 0.5 нг/мл |
| 23. | НПП «АКВАПАСТ» г. С. — Петербург | «Аквагеп-В-Аг-1» (субстратная система ОФД) | 0.5 нг/мл |
| 24. | ЗАО «Вектор — Бест» г. Новосибирск | «Вектогеп B-HBs-антиген» | 0.5 нг/мл |
| 25. | ДГУ ЭПП «Вектор — Биальгам» г. Новосибирск | «Рекоматгеп В» | 0.5 нг/мл |
| 26. | ДГУ ЭПП «Вектор — Биальгам» г. Новосибирск | «HBs антиген ИФА» | 0.5 нг/мл |
| 27. | ЗАО «МБС» г. Новосибирск | «HBsAg-ДС» (комплект N 1) | 0.5 нг/мл |
| 28. | ООО БМФ «Мультитест» | «HBsAg-ИФА-М» | 0.5 нг/мл |
| 29. | ЗАО «Биоград» | «Иммунокомб II HBsAg» | 0.5 нг/мл |
| 30. | HUMAN | «HBsAg ELISA» | 0.5 нг/мл |
Руководитель Департамента
госсанэпиднадзора
С.И.ИВАНОВ
Приложение N 5
к приказу Министерства
здравоохранения
Российской Федерации
от 30.10.2000 г. N 384
ПЕРЕЧЕНЬ
ДИАГНОСТИЧЕСКИХ ТЕСТ — СИСТЕМ, ПРЕДНАЗНАЧЕННЫХ ДЛЯ ПОДТВЕРЖДЕНИЯ НАЛИЧИЯ HBsAg
| N пп | Фирма — производитель | Название тест — системы |
| 1. | НПО «Диагностические системы» г. Н. Новгород | «ИФA-HBsAg-подтверждающий тест» |
| 2. | НПП «Аквапаст» г. С. — Петербург | «Гепатаг-В-N 3» |
| 3. | ЗАО «Вектор — Бест» г. Новосибирск | «Рекоматгеп В-подтвержд. тест — стрип» |
| 4. | ЗАО «Вектор — Бест» г. Новосибирск | «Вектогеп B-HBs-антиген — подтвержд.- стрип» |
| 5. | ДГУ ЭПП «Вектор — Биальгам» г. Новосибирск | «Рекоматгеп В» |
| 6. | НИАРМЕДИК ПЛЮС | «Гепаблок» |
| 7. | Фирма «ИмБио» г. Н. Новгород | «ИФА-HBsAg» |
| 8. | Предприятие «ЭКОлаб» г. Электрогорск | «Рекоматгеп В-стрип» |
| 9. | BIO-RAD | R «Monolisa HBs Ag CONFIRMATION» |
| 10. | «ORGANON TEKNIKA» | «Hepanostika HBsAg UNI-FORM II» CONFIRMATION |
| 11. | ROCHE | «ELECSYS HBsAg confirmatory test» (автомат.) |
Руководитель Департамента
госсанэпиднадзора
С.И.ИВАНОВ
Источник