Стеатоз печени при хроническом гепатите с
Жировые отложения в клетках печени — стеатоз при гепатите С изменяют структуру и жизнедеятельность органа, негативно воздействуя на обменные процессы в организме. Для лечения такой патологии применяется противовирусная и гепатопротекторная терапия. При успешном воздействии на вирус жировые отложения уменьшаются и функции печени восстанавливаются.
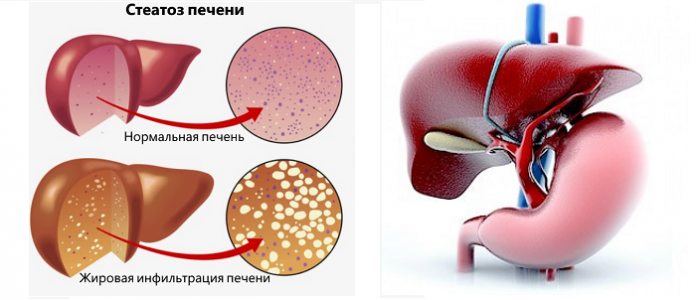
Что такое стеатоз?
Стеатоз возникает в результате накопления жировых отложений в клетках печени.
При прогрессировании заболевания нарушается метаболизм, жиры вытесняют здоровые ткани. В дальнейшем разрушается структура клеток печени и отложения накапливаются в межклеточном пространстве. Вирус гепатита С нередко провоцирует стеатоз, нарушая обмен липопротеинов в организме — компонентов жиров и жироподобных веществ.
Вернуться к оглавлению
Причины патологии
Основными причинами развития стеатоза при вирусном поражении гепатитом С являются гормональные изменения организма и нарушение обмена веществ. Течение заболевания ухудшается при негативном влиянии вредных привычек и образа жизни пациента. Основные причины стеатоза при вирусном гепатите С:
 Нарушение обмена веществ может стать причиной онкологического заболевания.
Нарушение обмена веществ может стать причиной онкологического заболевания.
- дислипидемия — нарушение жирового и белкового обмена;
- наследственные нарушения метаболизма;
- синдром избыточного бактериального роста — сбой переваривания жиров;
- сахарный диабет II типа;
- синдром мальабсорбции — хроническое нарушение усвоения и всасывания питательных веществ;
- хронические заболевания органов ЖКТ;
- гипоксия тканей — недостаток поступления кислорода;
- патологии эндокринной системы с нарушением гормонального фона;
- сердечная недостаточность;
- болезни дыхательной системы.
Факторы, способствующие развитию поражений печени:
- нездоровое питание с преобладанием жирной и калорийной пищи;
- алкогольная интоксикация, алкоголизм;
- ожирение;
- резкое похудение;
- прием лекарственных препаратов;
- длительное парентеральное питание — введение питательных веществ капельно;
- вредное производство — интоксикация токсическими веществами;
- возрастные изменения и старение организма.
Вернуться к оглавлению
Симптомы стеатоза на фоне гепатита С
 Патологические процессы провоцируют болевые ощущения.
Патологические процессы провоцируют болевые ощущения.
Начальные изменения печеночных клеток проявляются нарушениями деятельности желудочно-кишечного тракта. В дальнейшем интоксикация организма провоцирует осложнения со стороны сердечно-сосудистой и нервной систем, головного мозга. При стеатозе, развивающемся на фоне гепатита С, нарушения печеночной деятельности выражаются следующей симптоматикой:
- болевые ощущения в области правого подреберья;
- снижение либо отсутствие аппетита;
- отрыжка;
- горечь во рту;
- тошнота, рвота;
- вздутие живота, метеоризм;
- расстройство стула (понос или запор);
- слабость, повышенная утомляемость;
- налет на языке и неприятный запах изо рта.
В дальнейшем проявляются следующие осложнения:
 Затяжные психоэмоциональные расстройства вводят в глубокую депрессию.
Затяжные психоэмоциональные расстройства вводят в глубокую депрессию.
- усиление болевых ощущений;
- кровоточивость десен;
- высыпания на коже, зуд;
- нарушение сна, бессонница;
- депрессивное психоэмоциональное состояние;
- пожелтение склер и кожного покрова;
- повышение температурных показателей;
- сбои ритма сердца;
- нарушение концентрации внимания, забывчивость;
- головокружение;
- отечность конечностей;
- выпадение волос.
Вернуться к оглавлению
Диагностика
Для определения изменений печени и развития вирусного процесса проводится комплексное обследование организма. Основные лабораторные методы диагностики:
- Биохимический анализ крови. Показывает состояние внутренних органов, нарушения обмена веществ, количество ферментов печени.
- Коагулограмма. Определение свертываемости крови.
 Исследование на клеточном уровне установит природу поражения.
Исследование на клеточном уровне установит природу поражения.
Инструментальные исследования печени:
- Ультразвуковая диагностика (УЗИ). Определение размеров и распространения патологических процессов.
- Компьютерная томография (КТ). Посрезное сканирование органа с визуализацией изменений структуры.
- Магнитно-резонансная томография (МРТ). Подробное изучение состояния печеночных тканей и функционирования желчевыводящих путей.
- Перитонеоскопия. Малоинвазивный метод определения состояния органов брюшной полости через вводимый эндоскоп и выведение получаемой информации на монитор.
- Биопсия. Исследование фрагмента печени с определением изменений на клеточном уровне.
Вернуться к оглавлению
Лечение стеатоза при гепатите С
Для подавления жировых изменений в печени необходимо соблюдение принципов лечебного питания, устранение провоцирующих факторов и применение медикаментозных средств. Курс терапии подбирается индивидуально для каждого пациента, учитывая степень повреждения органов, активности вирусного процесса и проявляющейся симптоматики. Лечебное питание способствует:
- нормализации обменных процессов в организме;
- стимулированию расщепления жиров за счет усиленной выработки желчных кислот;
- восстановлению пищеварительной деятельности ЖКТ;
- регенерации клеток печени.
 Вредную пищу рекомендовано исключить из рациона полностью.
Вредную пищу рекомендовано исключить из рациона полностью.
Диетические рекомендации:
- применять дробное питание небольшими порциями;
- уменьшить или исключить употребление поваренной соли;
- соблюдать режим питья;
- приготавливать пищу методом варки, тушения, запекания в духовке либо на пару.
Медикаментозные средства направлены на улучшение жирового обмена, подавление вирусной активности и восстановление клеток печени. Основные лекарства описаны в таблице:
| Группа препаратов | Действие |
| Статины | Подавляют воспаление |
| Уменьшают холестерин | |
| Фибраты | Улучшают обменные процессы |
| Восстанавливают кровообращение | |
| Тиазолиндионы | Уменьшают поражение клеток печени |
| Усиливают распад жиров | |
| Противовирусные | Снижают инфекционную нагрузку |
| Подавляют воспаление | |
| Альфа-липоевая кислота | Улучшает жировой обмен |
| Гепатопротекторы | Защищают и восстанавливают клетки печени |
Для улучшения самочувствия и поддержания организма рекомендовано избавиться от всех вредных привычек, увеличить пребывание на свежем воздухе и двигательную активность, поддерживать стабильное психоэмоциональное состояние. При стеатозе на фоне гепатита С необходимо регулярное наблюдение лечащего врача и выполнение медицинских рекомендаций.
Источник
Стеатоз печени часто встречается у больных с HCV-инфекцией и может сочетаться с метаболическим синдромом. Мы изучали стеатоз печени у больных, получавших пэгинтерферон-α-2a и рибавирин. Исходно стеатоз (>5%) выявили у 45 (22%) из 207 пациентов. У больных стеатозом печени были выше частота генотипа 3 HCV (51% и 14%; р<0,0001), вирусная нагрузка (р=0,0045), масса тела (р=0,0176), индекс массы тела (ИМТ; р=0,0352) и сывороточные уровни триглицеридов (ТГ; р=0,0364), частота гипертриглицеридемии (р=0,0009), артериальной гипертонии (р=0,0229) и ниже уровень холестерина (р=0,0009).
Предикторами выраженного стеатоза были генотип 3 (относительный риск [ОР] 9,04, 95% ДИ 3,85-21,21, р<0,0001), уровень HCV RNA (ОР 2,96, 1,49-5,88, р=0,0019) и концентрация триглицеридов (ОР 1,06, 1,02-1,11, р=0,0071). У больных с генотипом 3 единственным достоверным предиктором стеатоза была вирусная нагрузка (ОР 11,15, 2,60-47,81, р=0,0012), а у пациентов с другими генотипами — гипертриглицеридемия (ОР 1,07, 1,02-1,12, р=0,0041). У 134 (65%) из 207 пациентов был достигнут стойкий вирусологический ответ на лечение пэгинтерфероном-a-2a и рибавирином. У больных с генотипом 3, ответивших на лечение, частота стеатоза уменьшилась с 48% до 13%, в то время как у пациентов с другими генотипами частота стеатоза существенно не изменилась, несмотря на стойкий вирусологический ответ. Результаты анализа международного исследования подтвердили, что стеатоз печени развивается примерно у 1/5 больных хроническим гепатитом С. У большинства пациентов стеатоз сочетался с другими проявлениями метаболического синдрома. Стеатоз значительно чаще встречается у больных с генотипом 3. Стойкий вирусологический ответ у таких пациентов сопровождается уменьшением стеатоза.
Стеатоз печени — это характерное проявление многих заболеваний, включая неалкогольный стеатогепатит и хронический гепатит С. При HCV-инфекции стеатоз может быть проявлением метаболического синдрома, в частности у пациентов, инфицированных не генотипом 3, или следствием специфического действия вируса, как у больных с генотипом 3. Частота стеатоза печени у больных с HCV-инфекцией повышена примерно в 2,5 раза. Это свидетельствует о том, что HCV способствует развитию жировой инфильтрации печени. В нескольких исследованиях наличие стеатоза печени ассоциировалось с более тяжелым фиброзом у больных хроническим гепатитом С. Однако когда были учтены другие факторы, ассоциирующиеся со стеатозом, связь между ним и фиброзом утратила достоверность. В целом эти данные свидетельствуют о том, что стеатоз служит кофактором, а не первичной причиной ускоренного прогрессирования фиброза.
У больных хроническим гепатитом С стеатоз печени ассоциировался с генотипом 3 HCV, повышенным индексом массы тела (ИМТ) и возрастом. У пациентов с генотипом 3 вируса стеатоз коррелировал с внутрипеченочным уровнем HCV RNA. Элиминация генотипа 3 вируса сопровождалась уменьшением стеатоза. У больных с генотипом 1 и стеатозом печени было отмечено снижение частоты раннего вирусологического ответа и стойкого вирусологического ответа. Ниже приведены результаты ретроспективного анализа части пациентов, включенных в рандомизированное международное исследование влияния стеатоза на частоту стойкого вирусологического ответа и влияние противовирусной терапии на жировую инфильтрацию печени.
Настоящий анализ основывался на результатах международного исследования III фазы, в котором первичным больным хроническим гепатитом С проводили комбинированную терапию пэгинтерфероном a-2a (Пегасис, «Roche») в дозе 180 мкг/нед и рибавирином в низкой (800 мг/сут) или стандартной (1000 или1200 мг/сут в зависимости от массы тела) дозах (Копегус, «Roche») в течение 24 или 48 недель. Критериями включения в исследование были наличие HCV RNA в сыворотке (COBAS AMPLICOR HCV MONITOR Test, v2.0, Roche Diagnostics, чувствительность 2000 копий/мл, или 600 МЕ/мл), повышенная сывороточная активность АЛТ и гистологические признаки хронического гепатита при биопсии печени, выполненной в течение предыдущих 15 месяцев. Критериями исключения служили ВИЧ-инфекция, декомпенсация заболевания печени или серьезные сопутствующие заболевания. Критерии включения и исключения и основные результаты исследования были опубликованы ранее. В начале исследования всем центрам предлагали выполнить биопсию печени в конце периода наблюдения, т.е. через 24 недели после завершения лечения. Соответственно, парная биопсия печени была выполнена у части больных. В парных биоптатах печени оценивали выраженность стеатоза, а также воспалительную активность и фиброз, которые анализировали с помощью модифицированного индекса Кноделля. Биоптат изучал один независимый патологоанатом слепым методом. Стеатоз классифицировали на основании доли гепатоцитов, содержавших включения жира: <=5%, >5-33%, 34-66%, >66%. Критерием наличия стеатоза печени считали наличие >5% гепатоцитов, инфильтрированных жиром.
В начале исследования всем центрам предлагали выполнить биопсию печени в конце периода наблюдения, т.е. через 24 недели после завершения лечения. Соответственно, парная биопсия печени была выполнена у части больных. В парных биоптатах печени оценивали выраженность стеатоза, а также воспалительную активность и фиброз, которые анализировали с помощью модифицированного индекса Кноделля. Биоптат изучал один независимый патологоанатом слепым методом. Стеатоз классифицировали на основании доли гепатоцитов, содержавших включения жира: <=5%, >5-33%, 34-66%, >66%. Критерием наличия стеатоза печени считали наличие >5% гепатоцитов, инфильтрированных жиром. Критерием стойкого вирусологического ответа был отрицательный результат качественной ПЦР на HCV RNA (COBAS AMPLICOR HCV MONITOR Test, v2.0, Roche Diagnostics, чувствительность 100 копий/мл, мере на 2 log10 через 12 недель (COBAS AMPLICOR HCV MONITOR Test, v2.0, Roche Diagnostics) или клиренса HCV RNA (COBAS AMPLICOR HCV MONITOR Test, v2.0, Roche Diagnostics). В анализ включали пациентов, у которых была выполнена парная биопсия печени исходно и в конце периода наблюдения. Для выделения независимых предикторов стеатоза печени проводили множественный логистический регрессионный анализ. Для оценки связи между исходными показателями и стеатозом печени использовали критерий хи-квадрат Вальда. Переменную включали в модель, если скорректированное значение хи-квадрат было статистически значимым. Анализировали следующие исходные факторы хозяина и вируса: возраст, пол, масса тела, ИМТ, степень повышения активности АЛТ по сравнению с верхней границей нормы, сахарный диабет, гипертриглицеридемия и/или гиперхолестеринемия, цирроз печени, индекс некровоспалительных изменений, индекс фиброза, генотип HCV и сывороточный уровень HCV RNA, а также ранний вирусологический ответ. Сахарный диабет диагностировали при наличии анамнеза диабета и/или повышенного уровня глюкозы. Критериями диагностики артериальной гипертонии были анамнез гипертонии или исходное систолическое и/или диастолическое АД >130/85 мм рт. ст. Гипертриглицеридемию диагностировали, если сывороточный уровень триглицеридов превышал 150 мг/дл. Критерием диагностики гиперхолестеринемии был исходный уровень холестерина >200 мг/дл. Изменения доли больных стеатозом анализировали с помощью теста Мак-Немара. Все статистические методы были двусторонними при уровне значимости 0,05. Спонсором исследования была компания Roche (Швейцария), которая отвечала за сбор и статистический анализ данных. Главный исследователь имел неограниченный доступ к данным и интерпретировал результаты. Публикации не ограничивались. Первый автор принимал окончательное решение по поводу всех аспектов публикации, а все перечисленные авторы принимали участие в интерпретации результатов и написании статьи.
В исследовании приняли участие 36 из 99 центров. Парные биопсии печени были выполнены у 207 из 1311 больных. Исходно стеатоз печени выявили у 45 (22%) из 207 больных. Исходные показатели пациентов с учетом выраженности стеатоза приведены в табл.1.
Примечание: * критерий хи-квадратгенотипом 3 встречалась значительно чаще, чем у больных с другими генотипами (51% и 14%, соответственно; р<0,0001). Кроме того, у больных стеатозом печени были выше уровни HCV RNA (р=0,0045), масса тела (р=0,0176) и сывороточные уровни триглицеридов (р=0,0364), чаще встречались ИМТ>25 кг/м2 (р=0,0352), гипертриглицеридемия >150 мг/дл (р=0,0009), а также повышенное АД или гипертония в анамнезе (р=0,0229), в то время как исходные уровни холестерина были ниже (р=0,0009), чем у пациентов без стеатоза (табл. 1).
Таблица 1. Исходная характеристика пациентов в зависимости от выраженности стеатоза
| Показатели | Выраженность стеатоза в исходном биоптате печени ≤5% | Выраженность стеатоза в исходном биоптате печени >5% | Значение р* |
| n (%) | 162 (78) | 45 (22) | |
| Женщины/мужчины (% мужчин) | 51 /111 (69) | 14/31 (69) | нд |
| Возраст (лет) | 42,6±9,3 | 42,1±10,7 | нд |
| Масса тела (кг) | 74,8±14,2 | 80,6±13,7 | 0,0176 |
| HCV RNA (log10 копий/мл) | 6,4±0,7 | 6,7±0,5 | 0,0045 |
| Генотип HCV | |||
| Не 3 (%) | 139 (85,8) | 22 (48,9) | <0,0001 |
| 3 (%) | 23 (14,2) | 23 (51,1) | |
| ИМТ, кг/м2 | |||
| 20-25, норма (%) | 79 (48,8) | 12 (26,7) | 0,0352 |
| 25-30, избыточная масса тела (%) | 60 (37,0) | 24 (53,3) | |
| >30, ожирение (%) | 23 (14,2) | 9 (20,0) | |
| Артериальная гипертония (%) | 63/159 (39,6) | 26/44 (59,1) | 0,0229 |
| Гипертриглицеридемия (%) | 24/155 (15,5) | 17/43 (39,5) | 0,0009 |
| Цирроз (%) | 43 (26,5) | 11 (24,4) | нд |
| Холестерин (мг/дл) | 179,2±35,5 | 156,7±43,3 | 0,0009 |
| Триглицериды (мг/дл) | 113,8±71,9 | 168,9±210,6 | 0,0364 |
| Глюкоза (мг/дл) | 93,9±17,3 | 100,1±23,5 | нд |
| Сахарный диабет (%) | 36/158 (23) | 11/43 (26) | нд |
| Индекс Кноделля | |||
| Воспаление ≥9 (%) | 18/161 (11) | 5/44 (11) | нд |
| Фиброз>2 (%) | 45/161 (28) | 10/45 (22) | нд |
Рис. 1. Независимые предикторы стеатоза печени (>5%)
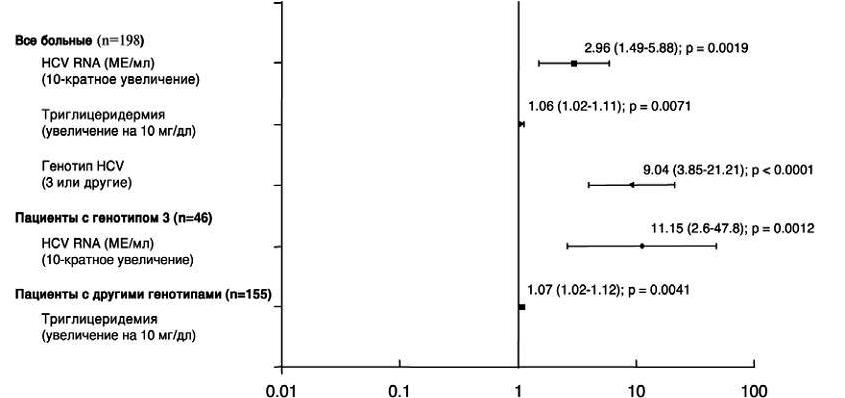
По данным множественного регрессионного логистического анализа, три исходных фактора были независимыми предикторами стеатоза печени: генотип 3 HCV, высокая вирусная нагрузка и гипертриглицеридемия (рис. 1). Следует отметить, что вероятность наличия стеатоза печени у больных с генотипом 3 вируса была значительно выше, чем у пациентов с другими генотипами (р<0,0001). У больных с генотипом 3 HCV единственным предиктором стеатоза печени был исходный уровень HCV RNA (рис. 1), а у пациентов с другими генотипами вируса — уровень триглицеридов (рис. 1). Стойкий вирусологический ответ на лечение пэгинтерфероном a-2a и рибавирином был достигнут у 134 (65%) из 207 пациентов. К концу периода наблюдения доля пациентов со стеатозом печени снизилась с 22% до 12% (р=0,0004). У больных, достигших стойкого вирусологического ответа, этот эффект был более выраженным (с 22% до 9%), чем у пациентов, не ответивших на лечение (с 22% до 17%; табл. 2). У пациентов, инфицированных не генотипом 3 HCV, наличие стойкого вирусологического ответа не ассоциировалось со значительными изменениями доли больных со стеатозом печени (рис. 2). Она снизилась на 4% у пациентов, ответивших на лечение (с 11% до 7%), и на 3% у больных, у которых не был достигнут стойкий вирусологический ответ (с 18% до 15%) (рис. 2). Напротив, среди больных с генотипом 3, ответивших на противовирусную терапию, доля пациентов со стеатозом печени снизилась с 48% до 13%. Число больных с генотипом 3, у которых отсутствовал стойкий вирусологический ответ, было небольшим (6), что не позволяло надежно оценить динамику стеатоза печени. Связи между исходными показателями и изменениями стеатоза печени приведены в табл. 2. Частота стеатоза печени значительно снизилась после лечения независимо от пола, возраста и наличия гипертриглицеридемии или артериальной гипертонии. Среди больных без цирроза частота стеатоза печени значительно снизилась по сравнению с исходной у пациентов с генотипом 3 и высокой вирусной нагрузкой (>600000 МЕ/мл). У пациентов с нормальным ИМТ и избыточной массой тела частота стеатоза печени также значительно снизилась, в то время как у больных с ожирением она не изменилась. Значительное уменьшение частоты стеатоза печени было выявлено у больных с гистологическим индексом активности <9 и индексом фиброза <2.
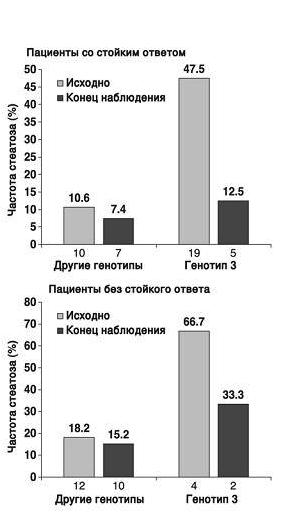
Рис. 2. Зависимость изменений частоты стеатоза печени
в зависимости от наличия стойкого вирусологического ответа
на лечение пэгинтерфероном-α-2a и рибавирином·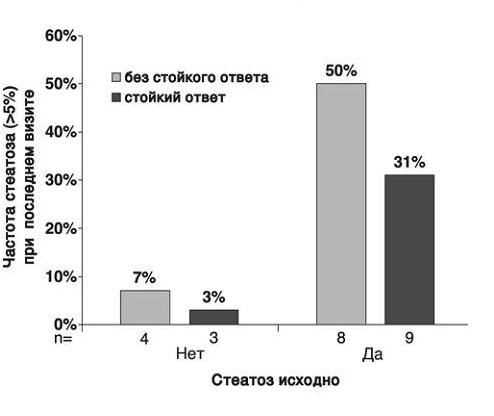
Рис.3. Изменения частоты стеатоза печени у пациентов,
ответивших и не ответивших на лечение
пэгинтерфероном -a-2a и рибавирином
(объединены все 4 группы)
Таблица 2. Факторы, оказывавшие влияние наизменения частоты стеатоза печени после лечения
| Всего | Пациенты со стеатозом | Пациенты со стеатозом | |
| Исходно | После лечения | ||
| n (%) | 206 | 45 (22) | 24 (12)*** |
| Пол, n (%) | |||
| Женщины | 65 | 14 (22) | 5 (8)* |
| Мужчины 141 31 (22) 19 (14)* | 141 | 31 (22) | 19 (14)* |
| Возраст | |||
| <43 лет | 102 | 22 (22) | 13 (13)* |
| ≥43 лет | 104 | 23 (22) | 11 (11)** |
| Генотип HCV | |||
| 1 | 117 | 17 (15) | 14 (12) |
| 2 | 30 | 3 (10) | 1 (3) |
| 3 | 46 | 23 (50) | 7 (15)*** |
| ИМТ | |||
| Норма | 90 | 12 (13) | 4 (4)* |
| Избыточная масса тела | 84 | 24 (29) | 11 (13)** |
| Ожирение | 32 | 9 (28) | 9 (28) |
| Гистологический диагноз | |||
| Цирроз | 54 | 11 (20) | 7 (13) |
| Без цирроза | 152 | 34 (22) | 17 (11)** |
| Индекс активности | |||
| <9 | 181 | 39 (22) | 21 (12)*** |
| ≥9 | 23 | 5 (22) | 3 (13) |
| Индекс фиброза | |||
| ≤2 | 150 | 35 (23) | 20 (13)** |
| >2 | 55 | 10 (18) | 4 (7) |
| Уровень HCV RNA | |||
| Низкий (≤600000 МЕ/мл) | 64 | 8 (12) | 7 (11) |
| Высокий (>600000 МЕ/мл) | 129 | 34 (26) | 16 (12)*** |
| Сахарный диабет | |||
| Нет | 153 | 32 (21) | 18 (12)** |
| Да | 47 | 11 (23) | 5 (11) |
| Гиперхолестеринемия (>5,18 ммоль/л) | |||
| Нет | 143 | 36 (25) | 13 (9)**** |
| Да | 41 | 17 (41) | 11 (27)* |
| Артериальная гипертония | |||
| Нет | 114 | 18 (16) | 8 (7)* |
| Да | 88 | 26 (30 | 15 (17)** |
| Ранний вирусологический ответ | |||
| Нет | 22 | 4 (18) | 5 (23) |
| Да | 184 | 41 (22 | 19 (10)**** |
| Стойкий вирусологический ответ | |||
| Нет | 72 | 16 (22 | 12 (17) |
| Да | 134 | 29 (22) | 12 (9)*** |
Были проанализировали изменения стеатоза печени в зависимости от стойкого вирусологического ответа. В конце периода наблюдения стеатоз сохранялся у 50% пациентов, не ответивших на лечение, и 31% больных, у которых был достигнут стойкий вирусологический ответ (рис. 3). Выявлена статистически значимая связь (р>0,001) между стойким вирусологическим ответом и уменьшением доли пациентов со стеатозом печени (табл. 2). Ранний вирусологический ответ (через 12 недель) также ассоциировался (р>0,001) с уменьшением числа больных со стеатозом печени (табл. 2). По данным множественного регрессионного логистического анализа, нормальный ИМТ или избыточная масса тела и ранний вирусологический ответ были независимыми предикторами отсутствия стеатоза печени после завершения лечения (рис. 4).
Частота стеатоза печени в когорте из 207 больных, которым была проведена парная биопсия печени, составила 22%. Этот показатель ниже такового в крупном мета-анализе (50%) и других исследованиях, в которых стеатоз печени диагностировали в 40% и 65% случаев. Эти различия могут отражать особенности пациентов и критериев включения/исключения, критериев диагностики ожирения и избыточной массы тела, классификации стеатоза. Например, в исследовании, в котором частота стеатоза составила 40%, его диагностировали, если жиром были инфильтрированы более 3% гепатоцитов (в нашем исследовании — >5%), что могло способствовать более частому выявлению стеатоза. Связь между фиброзом и стеатозом остается неясной. В некоторых исследованиях была выявлена ассоциация между ними, в то время как в других она отсутствовала.
Мы не выявили связи между двумя факторами, когда была сопоставлена степень фиброза у пациентов со стеатозом печени <5% и >5%. Более информативным было бы сравнение степени фиброза у больных с любым стеатозом и пациентов, у которых гистологические признаки стеатоза отсутствовали. Однако объем выборки нашего исследования был недостаточным для такого сравнения. Результаты нашего исследования продемонстрировали тесную связь стеатоза с генотипом 3 HCV, высокой вирусной нагрузкой, повышенными массой тела и ИМТ, гипертриглицеридемией и низким сывороточным уровнем холестерина. У пациентов с генотипом 3 вероятность наличия стеатоза была значительно выше, чем у больных с другими генотипами вируса. Этот факт согласуется с результатами других исследований, в которых изучался стеатоз у больных хроническим гепатитом С.
Некоторые исследователи отметили статистически значимую связь между повышением ИМТ и частотой стеатоза печени; однако другие авторы не выявили ассоциацию между стеатозом и ИМТ у больных с генотипом 3. Кроме того, у больных хроническим гепатитом С наблюдали связь между стеатозом и висцеральным ожирением, которое оценивали на основании окружности талии. Другие авторы, как и мы, выявили связь между увеличением вирусной нагрузки и стеатозом печени, особенно у больных с генотипом 3 HCV. У многих пациентов со стеатозом печени имелись признаки метаболического синдрома, включая повышенный ИМТ, гипертриглицеридемию и артериальную гипертонию. Мы не обнаружили связь между уровнями глюкозы или наличием сахарного диабета в анамнезе и стеатозом, однако мы не оценивали инсулинорезистентность, которая может наблюдаться при отсутствии явного сахарного диабета. Ранее была отмечена ассоциация между проявлениями метаболического синдрома и HCV-инфекцией. У больных хроническим гепатитом С выявлена достоверная корреляция между сахарным диабетом 2 типа, ИМТ и стеатозом, а также между инсулинорезистентностью или высокой гликемией и выраженностью фиброза печени . Следует отметить, что в одном исследовании генотип 3 ассоциировался со значительно более низкой инсулинорезистентностью, чем другие генотипы HCV. Этот факт согласуется с более высокой частотой сахарного диабета у больных, инфицированных генотипами 1 и 2 вируса. Низкий уровень сывороточного холестерина у больных стеатозом соответствует результатам предыдущих исследований. Сывороточные концентрации холестерина и аполипопротеина В значительно повышались у больных с генотипом 3, достигших стойкого вирусологического ответа, и не менялись у пациентов, у которых сохранялась HCV RNA после лечения. Эти наблюдения свидетельствуют о том, что у больных хроническим гепатитом С и стеатозом могут быть нарушены синтез и/или транспорт холестерина. Элиминация HCV с генотипом 3 после лечения пэгинтерфероном-α-2a и рибавирином сопровождалась уменьшением стеатоза. Напротив, у пациентов с другими генотипами вируса частота стеатоза существенно не менялась после противовирусной терапии. Уменьшение стеатоза на фоне стойкого вирусологического ответа у больных с генотипом 3 HCV, наблюдавшееся во многих исследованиях, подтверждает гипотезу о том, что этот генотип вируса является причиной жировой инфильтрации печени. Напротив, у пациентов с другими генотипами элиминация вируса не оказывала влияние на степень стеатоза. Однако у больных с генотипом 1, не ответивших на лечение, стеатоз был более выраженным, чем у пациентов, достигших стойкого вирусологического ответа. Связь между стеатозом и пониженной частотой вирусологического ответа у больных с генотипом 1 имеет значение для выбора метода лечения при наличии метаболического синдрома у таких пациентов. Перед назначением противовирусной терапии желательно добиться уменьшения метаболического синдрома, например, путем снижения массы тела. Оно приводило к значительному снижению распространенности стеатоза и выраженности фиброза у больных хроническим гепатитом С как с генотипом 3, так и другими генотипами вируса, хотя польза подобного подхода окончательно не установлена . Недостаток нашего исследования заключается в том, что мы не определяли инсулинорезистентность на основании индекса HOMA. Однако она не имела отношения к первичной конечной точке нашего исследования. Кроме того, парная биопсия печени была выполнена не всем пациентам. Однако в исследовании приняли участие больные из 36 центров. Мы полагаем, что они были репрезентативными по отношению к выборке всего исследования. Таким образом, результаты крупного рандомизированного международного исследования III фазы подтвердили, что стеатоз печени у пациентов с генотипом 3 встречается чаще, чем у пациентов с другими генотипами, а элиминация вируса с генотипом 3 при лечении пэгинтерфероном-α-2a и рибавирином сопровождается уменьшением стеатоза. Стеатоз печени ассоциируется с признаками метаболического синдрома, в том числе высоким ИМТ, гипертриглицеридемией и повышенным АД. Соответственно, лечение метаболического синдрома может привести к уменьшению тяжести стеатоза и задержать прогрессирование фиброза, а у больных с генотипом 1 может улучшить результаты противовирусной терапии.
Клиническая гепатология, 2008, 4
Источник


