Гепатит патогенез на клеточном уровне
В патогенезе гепатита В можно выделить несколько ведущих звеньев патогенетической цепи:
- внедрение возбудителя — заражение;
- фиксация на гепатоците и проникновение внутрь клетки;
- размножение вируса и «выталкивание» его на поверхность гепатоцита, а также в кровь;
- включение иммунологических реакции, направленных на элиминацию возбудителя;
- иммунокомплексное поражение органов и систем;
- формирование иммунитета, освобождение от возбудителя, выздоровление.
Поскольку заражение при гепатите В всегда происходит парентеральным путем, можно считать, что момент инфицирования практически равнозначен проникновению вируса в кровь. Попытки некоторых исследователей выделять при гепатите В энтеральную и региональную фазу малообоснованы. Больше оснований считать, что с током крови вирус сразу попадает в печень.
Тропизм вируса гепатита В к ткани печени предопределен наличием в составе НВsАg специального рецептора — полипептида с молекулярной массой 31 000 Да (РЗ1), обладающего альбумин связывающей активностью. Аналогичная зона альбумина находится и на мембране гепатоцитов печени человека и шимпанзе, чем по существу и определяется тропизм НВV к печени человека и шимпанзе.
При проникновении вируса внутрь гепатоцита происходит высвобождение вирусной ДНК, которая, попадая в ядро гепатоцита и исполняя роль матрицы для синтеза нуклеиновых кислот, запускает ряд последовательных биологических реакций, чьим итогом становится сборка нуклеокапсида вируса. Нуклеокапсид мигрирует через ядерную мембрану в цитоплазму где и происходит окончательная сборка частиц Дейна — полного вируса гепатита В.
Следует, однако, отметить, что при заражении гепатоцита процесс может пойти двумя путями — репликативным и интегративным. В первом случае развивается картина острого или хронического гепатита, а во втором — вирусоносительство.
Причины, предопределяющие два вида взаимодействия вирусной ДНК и гепатоцита, точно не установлены. Вероятнее всего, тип реагирования генетически детерминирован.
Итогом репликативного взаимодействия становятся сборка структур коровского антигена (в ядре) и сборка полного вируса (в цитоплазме) с последующей презентацией полного вируса или его антигенов на мембране или в структуре мембраны гепатоцитов.
Принято считать, что репликация вируса не приводит к поражению клетки на уровне гепатоцита, поскольку вирус гепатита В не обладает цитопатическим действием. Это положение нельзя считать бесспорным, так как оно основывается на экспериментальных данных, которые, хотя и свидетельствуют об отсутствии цитопатического действия вируса гепатита В, но получены на культурах тканей и поэтому не могут быть полностью экстраполированы на вирусный гепатит В у человека. Во всяком случае, вопрос об отсутствии поражения гепатоцитов в ходе репликативной фазы нуждается в дополнительном изучении.
Однако, независимо от характера взаимодействия вируса с клеткой, в дальнейшем печень обязательно включается в иммунопатологический процесс. При этом поражение гепатоцитов связано с тем, что в результате экспрессии вирусных антигенов на мембране гепатоцитов и выхода вирусных антигенов в свободную циркуляцию происходит включение цепи последовательных клеточных и гуморальных иммунных реакций, направленных в конечном итоге на удаление вируса ил организма. Этот процесс осуществляется в полном соответствии с общими закономерностями иммунного ответа при вирусных инфекциях. Для элиминации возбудителя включаются клеточные цитотоксические реакции, опосредованные различными классами клеток-эффекторов: К-клеток, Т-клеток, естественных киллеров, макрофагов. В ходе этих реакций происходит разрушение инфицированных гепатоцитов, что сопровождается высвобождением вирусных антигенов (НВсАg, НВeАg, НВsАg), запускающих систему антителогенеза, вследствие чего в крови накапливаются специфические антитела, прежде всего к коровому — анти-НВс и е-антигену — анти-НВЕ. Следовательно, освобождение печеночной клетки от вируса происходит в процессе ее гибели за счет реакций клеточного цитолиза.
Одновременно с этим накапливающиеся в крови специфические антитела связывают антигены вируса, образуя иммунные комплексы, фагоцитируемые макрофагами и выделяющиеся почками. При этом могут возникать различные иммунокомплексные поражения в виде гломерулонефрита, артериита, артралгий, кожных высыпаний и др. С участием специфических антител происходит очищение организма от возбудителя и наступает полное выздоровление.
В соответствии с изложенной концепцией патогенеза гепатита В все многообразие клинических вариантов течения болезни принято объяснять особенностями взаимодействия вируса и кооперацией иммунокомпетентных клеток, иначе говоря, силой иммунного ответа на присутствие вирусных антигенов. По современным представлениям, сила иммунного ответа генетически детерминирована и сцеплена с антигенами гистосовместимости локуса НLA первого класса.
Принято считать, что в условиях адекватного иммунного ответа на антигены вируса клинически развивается острый гепатит с циклическим течением и полным выздоровлением. На фоне снижения иммунного ответа к антигенам вируса иммуноопосредованный цитолиз выражен незначительно, поэтому не происходит эффективной элиминации инфицированных клеток печени, что приводит к слабовыраженным клиническим проявлениям с длительной персистенцией вируса и, возможно, развитию хронического гепатита. При этом, наоборот, в случае генетически детерминированною сильного иммунного ответа и массивности инфицирования (гемотрансфузии) возникают обширные зоны поражения печеночных клеток, чему клинически соответствуют тяжелые и злокачественные формы болезни.
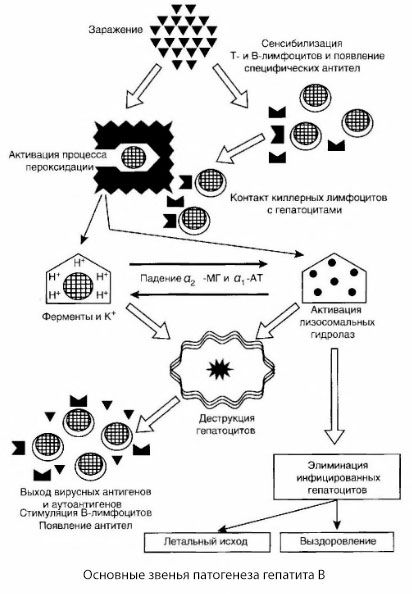
Представленная схема патогенеза гепатита В отличается стройностью, тем не менее в ней имеется ряд спорных и малоисследованных моментов.
Если следовать концепции гепатита В как иммунопатологического заболевания, можно было бы ожидать усиления реакций клеточной цитотоксичности с нарастанием тяжести заболевания. Однако, при тяжелых формах показатели клеточного звена иммунитета резко снижены, в том числе отмечается многократное падение, по сравнению с таковыми у здоровых детей, и показателя К-клеточной цитотоксичности. При злокачественной форме в периоде развития массивного некроза печени и особенно печеночной комы отмечается полная неспособность лимфоцитов к бластной трансформации под влиянием фитогематтлютинина, стафилококкового эндотоксина и НВsAg. Кроме того, отсутствует способность лейкоцитов к миграции по данным реакции торможения миграции лейкоцитов (РТМЛ), и выявляется резкое увеличение проницаемости мембран лимфоцитов по результатам исследований их с помощью флюоресцентного зонда тетрациклина.
Так, если показатели флюоресценции лимфоцитов здоровых людей составляют 9,9±2%, а при типичном гепатите В с доброкачественным течением они повышаются до 22,3±2,7%, то при злокачественных формах число флюоресцирующих лимфоцитов достигает в среднем 63,5±5,8%. Поскольку повышение проницаемости клеточных мембран однозначно оценивается в литературе как достоверный показатель их функциональной неполноценности, можно заключить, что при гепатите В, особенно при злокачественной форме, возникает грубое повреждение лимфоцитов. Об этом же свидетельствуют и показатели К-клеточной цитотоксичносги. При тяжелой форме на 1-2-й неделе заболевания цитотоксичность составляет 15,5±8,8%, а при злокачественной форме на 1-й неделе — 6.0±2,6, на 2-й — 22.0±6,3% при норме 44,8±2,6%.
Представленные данные однозначно свидетельствуют о выраженных нарушениях в клеточном звене иммунитета у больных с тяжелыми формами гепатита В. Очевидно также, что эти изменения возникают вторично, в результате поражения иммунокомпетентных клеток токсическими метаболитами и, возможно, циркулирующими иммунными комплексами.
Как показали исследования, у больных с тяжелыми формами гепатита В, особенно в случае развития массивного некроза печени, в сыворотке крови происходит падение титра HВsАg и НВeАg и одновременно начинают обнаруживаться в высоких титрах антитела к поверхностному антигену, что совершенно нехарактерно для доброкачественных форм болезни, при которых анти-НВV появляются лишь на 3-5-м месяцев болезни.
Быстрое исчезновение антигенов вируса гепатита В при одновременном появлении высоких титров противовирусных антител позволяет предполагать интенсивное образование иммунных комплексов и возможное их участие в патогенезе развития массивного некроза печени.
Таким образом, фактические материалы не позволяют однозначно трактовать гепатит В только с позиций иммунопатологической агрессии. И дело не только в том, что при этом не обнаруживается связи между глубиной и распространенностью морфологических изменений в печени, с одной стороны, и выраженностью клеточных факторов иммунитета — с другой. Теоретически это обстоятельство можно было бы объяснить поздними сроками исследования показателей клеточного иммунитета, когда иммунокомпетентные клетки подверглись мощному токсическому воздействию в связи с нарастающей функциональной недостаточностью печени. Можно, конечно, допустить, что иммунный цитолиз гепатоцитов происходит на самых ранних этапах инфекционного процесса, возможно, еще до появления клинических симптомов тяжелого поражения печени. Однако такое предположение маловероятно, поскольку у больных с острейшим (молниеносным) течением болезни выявлялись аналогичные показатели клеточного иммунитета и, кроме того, при морфологическом исследовании ткани печени не обнаруживалось массивной лимфоцитарной инфильтрации, в то же время выявлялись сплошные поля некротизированного эпителия без явлений резорбции и лимфоцитарной агрессии.
Объяснить морфологическую картину при остром гепатите только с позиций иммунного клеточного цитолиза весьма сложно, поэтому в ранних работах не исключали цитотоксическое действие вируса гепатита В.
В настоящее время это предположение нашло частичное подтверждение благодаря открытию вируса гепатита В. Как показали исследования, частота обнаружения маркеров гепатита D находится в прямой зависимости от тяжести заболевания: при легкой форме они обнаруживаются у 14%, среднетяжелой — у 18, тяжелой — 30, злокачественной — у 52% больных. Учитывая, что вирус гепатита D обладает некрозогенным цитопатическим эффектом, можно считать установленным, что в развитии фульминантных форм гепатита В большое значение имеет коинфекция вирусами гепатита В и D.
Патогенез гепатита В можно представить следующим образом. После проникновения вируса гепатита В в гепатоциты индуцируется иммунологическая атака на инфицированные гепатоциты Т-киллеров, выделяющих лимфотоксины в направлении печеночных клеток.
Интимные механизмы поражения гепатоцигов при гепатите В до настоящего времени не установлены. Ведущую роль играют активированные процессы перекисного окисления липидов и лизосомальные гидролазы. Пусковым моментом могут быть лимфотоксины, высвобождающиеся из эффекторных клеток при их контакте с гепатоцитами, но не исключено, что инициатором процессов переоксидации может выступать и сам вирус. В дальнейшем патологический процесс вероятнее всего развивается в следующей последовательности.
- Взаимодействие фактора агрессии (лимфотоксины или вирус) с биологическими макромолекулами (возможно, с компонентами мембран эндоплазматической сети, способными принимать участие в процессах детоксикации, по аналогии с другими повреждающими агентами, как это было показано по отношению к четыреххлористому углероду).
- Образование свободных радикалов, активация процессов перекисного окисления липидов и повышение проницаемости всех гепатоцеллюлярных мембран (синдром цитолиза).
- Движение биологически активных веществ по градиенту концентрации — потеря ферментов различной внутриклеточной локализации, донаторов энергии, калия и др. Накопление в клетках натрия, кальция, сдвиг pH в сторону внутриклеточного ацидоза.
- Активация и выход лизосомальных гидролаз (РНК-аза, ДНК-аза, катепсины и др.) с распадом печеночной клетки и высвобождением аутоантигенов.
- Стимуляция Т- и В-систем иммунитета с формированием специфической сенсибилизации Т-лимфоцитов к печеночному липопротеину, а также образование противопеченочных гуморальных аутоантител.
В предложенной схеме патогенеза гепатита В в качестве пускового фактора выступают вирусные антигены, чья интенсивная продукция наблюдается на самых ранних этапах заболевания и весь острый период, за исключением злокачественных форм, при которых продукция вирусных антигенов практически прекращается в момент развития массивного некроза печени, что и предопределяет быстрое снижение репликации вируса.
Очевидно также, что вирусные антигены активируют Т- и В-системы иммунитета. В ходе этого процесса возникает характерное перераспределение субпопуляций Т-лимфоцитов, направленное на организацию адекватного иммунного ответа, элиминацию инфицированных гепатоцитов, нейтрализацию вирусных антигенов, саногенез и выздоровление
При взаимодействии иммунокомпетентных клеток с вирусными антигенами на мембранах гепатоцитов или в ходе репродукции вируса внутри гепатоцита, возникают условия для активации процессов перекисного окисления липидов, управляющий как известно, проницаемостью всех клеточных и субклеточных мембран,
С этих позиций становится понятным столь закономерное и в высшей степени характерное для вирусных гепатитов возникновение синдрома цитолиза — повышенной проницаемости клеточных мембран
Конечным исходом синдрома цитолиза может быть полное разобщение окислительного фосфорилирования, истечение материала клетки, гибель печеночной паренхимы.
Однако в подавляющем большинстве случаев эти процессы не приобретают столь фатального развития. Только при злокачественных формах болезни патологический процесс протекает лавинообразно и необратимо, поскольку возникают массивное заражение, выраженный иммунный процесс, чрезмерная активация процессов переоксидации и лизосомальных гидродаз, явления аутоиммунной агрессии.
Эти же механизмы наблюдаются и при благоприятном течении гепатита В, с той лишь особенностью, что все они реализуются на качественно ином уровне. В отличие от случаев массивного некроза печени, при благоприятном течении болезни количество инфицированных гепатоцитов, а следовательно, зона иммунопатологического цитолиза меньше, процессы перекисного окисления липидов усиливаются не столь значительно, активация же кислых гидролаз приводит лишь к ограниченному аутолизу с несущественным высвобождением аутоантигенов, а следовательно, без массивной аутоагрессии, то есть все этапы патогенеза при благоприятном течении осуществляются в рамках сохраняющейся структурной организации паренхимы печени и сдерживаются защитными системами (антиоксиданты, ингибиторы и др.) и поэтому не имеют столь разрушительного действия.
Причины возникновения симптомов интоксикации при вирусных гепатитах исследованы не до конца. Предложение различать так называемую первичную, или вирусную, интоксикацию и вторичную (обменную, или метаболическую) можно считать позитивным, хотя это не раскрывает интимного механизма возникновения общетоксического синдрома. Во-первых, вирусы гепатитов не обладают токсическими свойствами, а, во-вторых, концентрация многих метаболитов далеко не всегда коррелирует с тяжестью заболевания и степенью выраженности симптомов токсикоза. Известно также, что и концентрация вирусных антигенов строго не коррелирует с тяжестью интоксикации. наоборот, с увеличением тяжести заболевания, а следовательно, нарастания степени токсикоза, концентрация НВsАg снижается и бывает самой низкой при злокачественных формах в момент возникновения глубокой печеночной комы. Вместе с тем частота обнаружения и титры специфических противовирусных антител прямо зависят от тяжести заболевания.
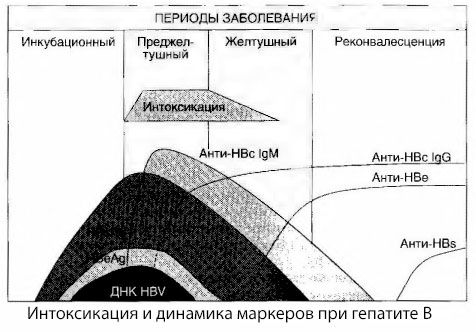
Интоксикация появляется не в момент регистрации вирусных антигенов, а в периоде циркуляции в крови противовирусных антител класса IgМ к коровскому антигену и антигену системы E. Более того, при тяжелых и особенно злокачественных формах у значительной части больных в крови появляются даже анти-НВs, чего обычно никогда не наблюдается при легких и среднетяжелых формах болезни.
Представленные данные дозволяют заключить, что синдром токсикоза при вирусных гепатитах, и гепатите В в частности, не возникает в результате появления в крови вирусных антигенов, а становится следствием взаимодействия вирусных антигенов с противовирусными антителами класса IgМ. Результат такого взаимодействия, как известно, — образование иммунных комплексов и, возможно, активных токсичных веществ.
Симптомы интоксикации возникают в момент появления в свободной циркуляции иммунных комплексов, но в дальнейшем такой корреляции не прослеживается.
Частичное объяснение этому можно найти при исследовании состава иммунных комплексов. У больных с тяжелыми формами в крови циркулируют преимущественно комплексы среднего размера, а в их составе на высоте токсического синдрома преобладают антитела класса тогда как в периоде спада клинических проявлений и реконвалесценции комплексы становятся более крупными, а в их составе начинают преобладать антитела класса IgG.
Представленные данные касаются механизмов развития токсического синдрома в начальном периоде заболевания, но при токсикозе, возникающем на высоте клинических проявлений, они имеют лишь частичное значение и особенно — при развитии печеночной комы.
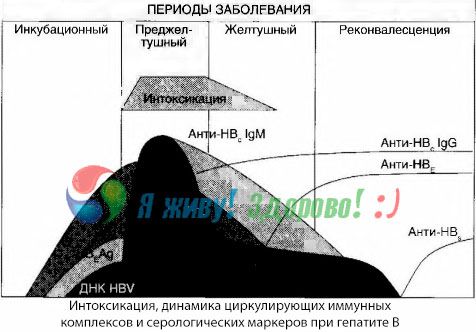
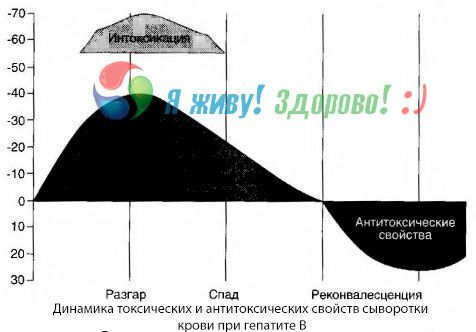
Методом гемокультур удалось показать, что при гепатите В в крови постоянно накапливаются токсины, высвобождающиеся из пораженной распадающейся печеночной ткани. Концентрация этих токсинов пропорциональна тяжести заболевания,они имеют белковую природу.
В периоде реконвалесценции в крови появляются антитела к этому токсину; но в случае возникновения печеночной комы концентрация токсина в крови резко возрастает, а антитела в крови не обнаруживаются.
Источник
Гепатит В (ГВ) — антропонозная вирусная инфекционная болезнь, передающаяся преимущественно парентеральным и половым путями, характеризуется развитием циклически протекающего паренхиматозного гепатита.
История и распространение
Наличие вирусного гепатита, передающегося парентеральным путем (сывороточный гепатит), было доказано в 1937—1940 гг. до обнаружения «австралийского» антигена ГВ Б.Бламбергом в 1962—1964 гг.
ГВ по распространенности занимает 2-е место после гепатита А. На его долю в различных регионах приходится от 10 до 30 % всех вирусных гепатитов. В Российской Федерации заболеваемость составляет в среднем около 25 на 100 000 населения в год.
Этиология
Вирус гепатита В (HBV) уникален среди патогенных вирусов человека, относится к гепаднавирусам — ДНК-содержащим гепатотропным вирусам. НВV имеет сферическую форму, диаметр 42 нм, сложную структуру. В центре нуклеокапсида расположен геном вируса, представленный двунитевой ДНК, и ферменты ДНК-полимераза и РНКаза. Наружная часть ядра вируса представлена НВcАg белковой природы (коровский антиген) и его модификацией — НВеАg — антигеном инфекциозности. Наружная липопротеиновая оболочка содержит поверхностный антиген НВsАg (австралийский антиген), который имеет 4 подтипа, обладающих антигенными различиями.
Существуют и мутантные штаммы вируса по антигенам НbsАg и НbеАg. Процесс репликации вируса сложен, возможно образование полноценных вирусов и дефектных, состоящих из НВsАg-частиц, которые не имеют инфекционных свойств. В последние годы открыты новые антигены НВV, однако роль их неясна. НВеАg и НВsАg циркулируют в крови, НВсАg обнаруживается только в ткани печени, антитела образуются ко всем основным антигенам — анти-НВс, анти-НВе и анти-НВs.
Вирус ГВ отличается исключительно высокой устойчивостью в окружающей среде. При 100 °С погибает через 30 мин, в холодильнике сохраняется до года, в замороженном состоянии — 20 лет, в сухой плазме — 25 лет. Раствор 1—2 % хлорамина инактивирует вирус через 2 ч, а 1,5 % раствор формалина — через 7 сут. При автоклавировании при 120 °С вирус гибнет через 5 мин.
Эпидемиология гепатита В
Единственным источником вируса является человек. Основная эпидемиологическая роль принадлежит вирусоносителям, число которых на земном шаре превышает 300 млн человек, в РФ их более 5 млн. В различных регионах мира частота носительства среди населения варьирует от 1 % (Европа, Северная Америка) до 20—50 % (Юго-Восточная Азия, Центральная Америка). Вторыми по степени важности источником являются больные острым и хроническим ГВ. НВsАg, основной используемый на практике маркер ГВ, обнаруживается во всех биологических жидкостях и экскретах. Однако эпидемиологическое значение, определяющее механизмы передачи инфекции, имеет наличие вируса в крови, сперме и, возможно, в слюне.
Наиболее достоверный тест на заразительность — обнаружение в крови ДНК вируса ГВ методом ПЦР. Естественные пути передачи — половой и вертикальный — от матери плоду через плаценту и чаще в процессе родов при прохождении плода через родовые пути. Возможно и заражение контактно-бытовым путем, через предметы, загрязненные кровью (белье, ножницы, зубные щетки, мочалки и т.д.), особенно при наличии заболеваний или травм кожи. Передача возбудителя при переливании крови уменьшилась в связи с тестированием донорской крови на наличие НВsАg, однако возможно заражение при переливании препаратов крови, пользовании недостаточно простерилизованным медицинским инструментарием многоразового применения.
Особенное распространение получил ГВ среди больных наркоманией, вводящих наркотики внутривенно. Сохраняется опасность заражения и для медицинских работников, имеющих частые контакты с кровью (работники лабораторий, процедурные сестры, работники отделений трансплантации, хирургии, реанимации и др.). В целом группы риска заражения ГВ такие же, как при ВИЧ-инфекции: половые партнеры инфицированных ГВ, дети, родившиеся от инфицированных матерей, проститутки и т.д.
Восприимчивость к ГВ высокая. Иммунитет после перенесенного ГВ в любой форме обычно пожизненный.
Патогенез
Вне зависимости от механизма заражения вирус попадает в кровь и инфицирует гепатоциты, однако механизм повреждения этих клеток существенно отличается от такового при ГА и ГЕ, поскольку репродукция вируса не сопровождается повреждением клеток. Заражение гепатоцита может приводить к различным результатам. Если происходит репликация вируса, развивается острый или хронический гепатит, если вирус интегрирует в геном гепатоцита, развивается вирусоносительство. Причины этого явления, по-видимому, связаны с генотипом макроорганизма, однако и роль вируса (особенность штамма) не исключена.
При репликации вируса, после сборки в цитоплазме гепатоцита вирусной частицы, происходит презентация его антигенов или полного вируса на поверхности мембраны гепатоцита. Вирус и его антигены распознаются естественными клетками-киллерами, Т-киллерами, К-клетками и другими, которые атакуют инфицированные клетки и разрушают их. При этом освобождаются антигены вируса (НВс, НВе, НВs). Против них образуются антитела.
Взаимодействие антител и антигенов обусловливает образование иммунных комплексов. Они фагоцитируются макрофагами и экскретируются почками. Фиксация комплексов на гепатоцитах может приводить к тому, что неинфицированные клетки также подвергаются атаке и разрушению клетками-киллерами. Вместе с тем они могут быть причиной внеклеточных аутоиммунных поражений в виде кожных высыпаний, артралгий, артериита, гломерулонефрита.
Таким образом, течение инфекционного процесса обусловлено генетически детерминированной силой и характером иммунного ответа. При адекватной реакции иммунной системы развивается острый циклически протекающий гепатит, который завершается полной элиминацией вируса и формированием прочного иммунитета.
При слабой реакции иммунной системы повреждение гепатоцитов маловыражено, болезнь протекает легко, но полной элиминации вируса не происходит и создаются условия для хронизации процесса. Напротив, при избыточном иммунном ответе поражаются не только инфицированные клетки, но и клетки, на которых фиксированы иммунные комплексы, что обусловливает обширный некроз печени, тяжелое течение болезни с развитием в некоторых случаях острой печеночной недостаточности. ГВ свойственны те же синдромы, что и ГА (цитолитический, паренхиматозно-мезенхимальный, внутрипеченочный холестаз).
Патоморфология гепатита В
Морфологические изменения характеризуются дистрофией и некрозом гепатоцитов, особенно в центре долек. При тяжелых формах болезни некроз тотальный или субтотальный. При холестатической форме основные морфологические изменения происходят во внутрипеченочных желчных ходах. Наблюдают пролиферацию эндотелия желчных капилляров, образование вокруг них лимфоцитарных инфильтратов, что приводит к развитию внутрипеченочного холестаза.
Клиническая картина
Инкубационный период от 45 до 180 дней, чаще 2—4 мес. Типично постепенное начало болезни. Преджелтушный период продолжительный, в среднем 10—12 дней. В отличие от ГА преобладают общее недомогание, слабость, утомляемость, разбитость, головная боль (особенно вечером), нарушение сна. Примерно у 25—30 % больных наблюдают боли в крупных суставах, преимущественно в ночное время, нередко появляются зуд кожи, уртикарные высыпания. У большинства больных имеются диспепсические расстройства: ухудшение аппетита, снижение вкусовых ощущений, тошнота, иногда рвота, горечь во рту, тяжесть и тупые боли в эпигастральной области и правом подреберье.
При осмотре выявляют увеличение и чувствительность печени, реже селезенки, обложенность языка, вздутие живота. Возможен субфебрилитет. За 2—3 дня до появления желтухи моча приобретает темную окраску, а кал становится гипохоличным.
Переход болезни в желтушный период сопровождается нарастанием явлений интоксикации и диспепсических расстройств. Наблюдаются проявления геморрагического синдрома. Желтуха настает постепенно, достигая максимума на 2—3-й неделе желтушного периода, она обычно интенсивная, на высоте желтухи кал ахоличный. Продолжительность желтушного периода варьирует в широких пределах, в среднем 3—4 нед.
Первыми признаками улучшения состояния являются появление аппетита, окрашивание кала, посветление дневных и вечерних порций мочи. При осмотре в желтушном периоде, помимо желтухи, выявляют обложенность и отечность языка, практически у всех больных увеличена печень, а у 30 % больных — селезенка. Часто отмечают брадикардию, гипотонию, приглушенность тонов сердца. При исследовании крови обнаруживают тенденцию к лейкопении и лимфоцитозу.
Период реконвалесценции от 3—4 нед до 6 мес. В этом периоде могут сохраняться астенизация, гепатомегалия, гиперферментемия, гипербилирубинемия, поражение желчевыводящих путей.
В отдельных случаях циклическое течение ГВ нарушается, особенно при легких, стертых формах болезни, у лиц с отягощенным преморбидным фоном. Прогностическими признаками, свидетельствующими о возможной хронизации процесса, является длительное персистирование НВеАg и ДНК вируса, что свидетельствует о продолжающейся репликации вируса.
Исходом ГВ чаще всего является выздоровление. В редких случаях возможно развитие фульминантного гепатита с летальным исходом; примерно у 5 % больных формируется хронический гепатит, который чаще имеет доброкачественное течение. Характерными признаками хронического гепатита служат увеличение печени, реже селезенки, преходящая субиктеричность склер, появление телеангиэктазий, «печеночных» ладоней, потеря веса, боли в области печени, диспепсические расстройства. В качестве отдаленного неблагоприятного последствия возможно развитие гепатоцеллюлярной карциномы.
Ющук Н.Д., Венгеров Ю.Я.
Опубликовал Константин Моканов
Источник

