Иммунный статус при гепатите с
Сахарова Д.А., Терешков П.П., Витковский Ю.А.
Введение. Мировая пандемия вируса гепатита С остается злободневной реальностью современности. Гепатит С (HCV) характеризуется высокой частотой хронизации, длительным персистированием возбудителя, высоким риском развития осложнений – цирроза печени, первичной гепатокарциномы и является ведущим в структуре смертности от заболеваний печени. Установлено, что основную роль в формировании характера иммунного реагирования макроорганизма играет взаимодействие в системе «вирус-хозяин», что определяет сценарий развития событий при HCV-инфекции [4].
В настоящее время считается доказанным, что высокая частота (50-85% по данным различных авторов) формирования хронических форм и развития осложнений обусловлена «ускользанием» вируса от иммунного надзора [5, 6]. Механизмы этого феномена до сих пор четко не установлены. Предполагается, что центральную роль в элиминации вируса гепатита С играет Т-клеточное звено иммунитета, которое, в конечном итоге всё же оказывается недостаточным [1, 7]. Существенное значение в поддержании патологического процесса у больных придается недостаточности CD4+ Т-хелперов и дисбалансу цитокинов [8].
При этом не в полной мере выяснены вопросы, касающиеся состояния системы иммунитета в зависимости от клинических факторов – наличия репликации, активности процесса, стадии и длительности заболевания, наличия сопутствующей патологии, генотипа HCV, что может иметь важное практическое значение [1].
Таким образом, многие аспекты иммунного ответа при гепатите С остаются невыясненными, в том числе в зависимости от стадии фиброза печени и длительности заболевания, хотя это актуально как в теоретическом, так и в практическом плане.
Цель исследования: изучить некоторые показатели иммунного статуса больных хроническим вирусным гепатитом С в зависимости от ряда клинических характеристик заболевания.
Материалы и методы. Было обследовано 69 человек, находившихся на стационарном лечении в ГУЗ «Краевая клиническая инфекционная больница» г. Читы за период с 2011 по 2013 г. по поводу хронического вирусного гепатита С. Женщины составили 30,4% (21 человек), мужчины – 69,6% (48 человек). Возраст обследованных находился от 16 до 58 лет, средний возраст – 36±1 лет. От всех пациентов получено добровольное информированное согласие на участие в исследовании.
Диагноз хронического вирусного гепатита С выставлен на основании клинико-лабораторных данных и обнаружения рибонуклеиновой кислоты (РНК) HCV методом полимеразной цепной реакции (ПЦР). Длительность заболевания до 5 лет выявлена у 66,7%, свыше 5 лет – у 33,3%. Первая степень биохимической активности процесса определялась у 55,0% больных хроническим вирусным гепатитом С (ХВГС), вторая – у 45,0%. Стадия заболевания по Metavir F0-F1 была диагностирована у 43,5% (30); F2 – у 42,0% (29); F3-F4 – у 14,5% (10).
Группу контроля составили 9 здоровых человек в возрасте от 27 до 42 лет, средний возраст 34,0±2 лет. Женщин было 66,7% , мужчин – 33,3%. От всех обследованных получено добровольное информированное согласие на участие в исследовании.
Кровь для иммунологического обследования получали путем пункции локтевой вены в строго стерильных условиях на 2-3-и сутки стационарного лечения. Взятие крови осуществляли в утренние часы (8-9 часов) строго натощак. Для иммунофенотипирования кровь забирали в пробирку VACUTAINER (BD), содержащую динатриевую соль ЭДТА объемом 2,5 мл.
Изучались активность и количество Lymphocytes (CD45+), T-cell (CD3+), T-help (CD3+CD4+), T-killer (CD3+CD8+), T-cellAktiv (CD3+HLA-DR+), T-helpAktiv (CD3+CD4+HLA-DR+), T-killAktiv (CD3+CD8+HLA-DR+), B-cell (CD19+), NK-cell (CD3-CD16+CD56+), T-NK-cell (CD3+CD16+CD56+). Оценку субпопуляционной структуры лимфоцитов осуществляли стандартным методом прямого пяти-параметрического иммунофлюоресцентного окрашивания цельной крови с использованием коммерческого лизирующего/фиксирующего раствора OPTILYSE С (Beckman Coulter) и панели моноклональных антител tetraCHROME™ и IOTest (Beckman Coulter): 1-ая панель – CD45-FITC/CD4-RD1/CD8-ECD/CD3-PC5 и HLA-DR-PC7; 2-ая панель – CD45-FITC/CD56-RD1/CD19-ECD/CD3-PC5 и CD16-PC7. Контрольные пробы инкубировали с иммуноглобулинами, мечеными флуорохромами (FITC, RD1, ECD, PC5, PC7) соответствующего изотипа – мышиные IgG1, IgG2a IOTest (Beckman Coulter). Цитофлюорометрию осуществляли на проточном цитофлюориметре «Cytomics FC-500» (Beckman Coulter, USA), регистрировали суммарно не менее 10 тыс. событий. Данные анализировали с помощью программы CXP Cytometer (Beckman Coulter).
Определение показателя лимфоцитарно-тромбоцитарной адгезии (ЛТА) проводили по методу, предложенному Ю.А. Витковским и соавт. (1999) [2]. Свежую гепаринизированную кровь обследуемых больных наслаивали на градиент урографин-фикол (плотность 1,077) и выделяли лимфоциты. Собирали интерфазное кольцо, содержащие клетки и кровяные пластинки, однократно промывали фосфатно-солевым буфером (рН 7,4) и центрифугировали при 1000 об/мин в течение 3-4 минут. Надосадочную жидкость сливали, осадок микроскопировали в камере Горяева. Показатель ЛТА выражали числом лимфоцитарно-тромбоцитарных коагрегатов на 100 клеток (норма – 13-15%). Степень адгезии (ЛТИ) определяли как число кровяных пластинок, адгезированных на поверхности одного лимфоцита (норма – 3,0±0,3).
Статистическая обработка полученных результатов осуществлялась с использованием пакета анализа Microsoft Excel. Она включала описание выборки, нахождение средней арифметической, среднеквадратического отклонения и ошибки средней арифметической, определялись частоты встречаемости признаков, группировка данных. Достоверность различий определялась по t-критерию Стьюдента.
Результаты и их обсуждение. Установлено, что у всех больных хроническим вирусным гепатитом С изменены показатели иммунограммы, по сравнению с контролем, при этом аналогичные закономерности определялись вне зависимости от стадии фиброза печени (табл. 1). Общими изменениями, по сравнению с контролем, явились значимое повышение относительного и абсолютного количества лимфоцитов, субпопуляций CD3+, CD3+CD4+, активированных Т-лимфоцитов (CD3+HLA-DR+), активированных Т-хелперов (CD3+CD4+HLA-DR+), активированных Т-киллеров (CD3+CD8+HLA-DR+). Одновременно отмечено снижение, по сравнению с контролем, процента и количества субпопуляций лимфоцитов CD19+ и CD3-CD16+CD56+. Повышенным оказался и иммунорегуляторный индекс (CD4+/CD8+).
В табл. 2 представлены средние показатели иммунограммы больных хроническим вирусным гепатитом в зависимости от степени активности процесса, в сравнении с контролем. Изменения иммунограммы аналогичны описанным выше, при этом значимых отличий между первой и второй степенью активности не зарегистрировано.
Изменения показателей иммунограммы у больных хроническим вирусным гепатитом С в зависимости от длительности заболевания представлены в табл. 3. Выявлено, что чем продолжительнее стаж болезни, тем значимо больше становилось активированных Т-лимфоцитов (р<0,05), активированных Т-хелперов (р<0,05) и активированных Т-киллеров (р<0,05). При этом иммунорегуляторный индекс (CD4+/CD8+) был повышен на ранних сроках заболевания и снижался после 5 лет болезни (р<0,01). Другие показатели клеточного иммунитета не зависели от длительности течения хронического вирусного гепатита С.
Не выявлено отличий, в сравнении с контролем, по таким показателям клеточного иммунитета, как абсолютное и относительное количество Т-киллеров (CD3+CD8+) и относительного количества субпопуляции CD3+CD16+CD56+.
В настоящее время широко изучаются межклеточные взаимодействия, особенно между системой гемостаза и иммунитета. Установлено, тромбоциты
Таблица 1. Сравнительная характеристика средних значений показателей иммунного статуса у больных ХВГС на разных стадиях фиброза печени (M±m)
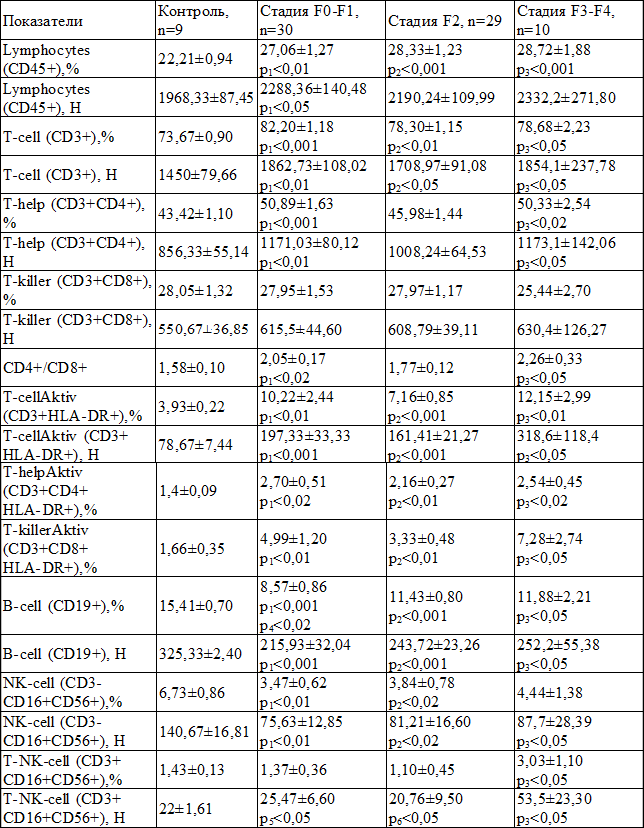
Примечания: р1 – достоверное различие показателей группы F0-F1 с контролем; р2 – достоверное различие показателей группы F2 с контролем; р3 – достоверное различие показателей группы F3-F4 с контролем; р4 – достоверное различие показателей группы F0-F1 с группой F2; р5 – достоверное различие показателей группы F0-F1 с группой F3-F4; р6 – достоверное различие показателей группы F2 с группой F3-F4
Таблица 2. Сравнительная характеристика средних значений показателей иммунного статуса у больных ХВГС в зависимости от степени активности процесса (M±m)
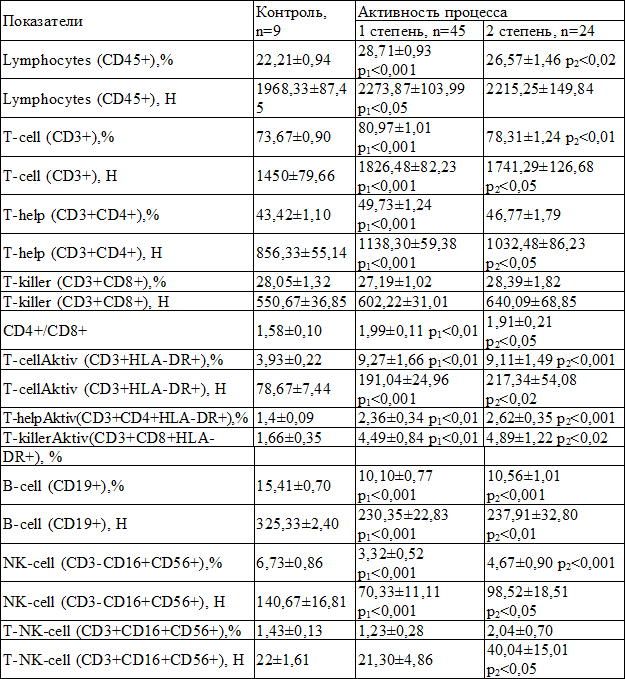
Примечания: р1 – достоверное различие показателей группы с 1 степенью активности с контролем; р2 – достоверное различие показателей группы со 2 степенью активности с контролем; р3 – достоверное различие показателей группы с 1 степенью активности с группой со 2 степенью активности
имеют отношение к протеканию воспалительных реакций: адгезивные взаимодействия между тромбоцитами и лейкоцитами являются важными звеньями механизмов, обеспечивающих миграцию лейкоцитов в зону повреждения, а, следовательно, воспаления и развития иммунных и репаративных реакций [2, 3]. Этот феномен получил название лимфоцитарно-тромбоцитарной адгезии.
Установлено, что у больных хроническим вирусным гепатитом С общий показатель ЛТА оказался пониженным – 9,13 ± 0,56%, при этом значимых отличий от стадии фиброза печени, активности процесса и длительности заболевания не выявлено (табл. 4). При этом заметна тенденция к повышению лимфоцитарно-тромбоцитарной адгезии с ростом степени активности и снижение ее с увеличением стажа болезни.
Таблица 3. Сравнительная характеристика средних значений показателей иммунного статуса у больных ХВГС в зависимости от длительности заболевания (M±m)
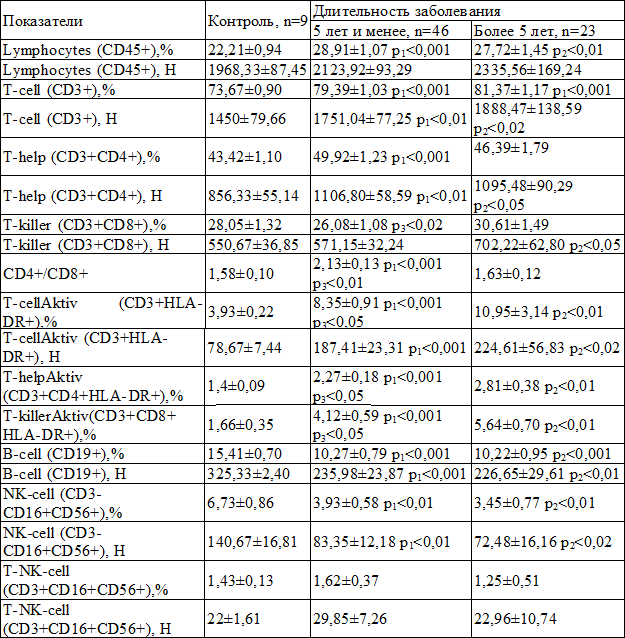
Примечания: р1 – достоверное различие показателей группы с длительностью заболевания 5 лет и менее с контролем; р2 – достоверное различие показателей группы с длительностью заболевания более 5 лет с контролем; р3 – достоверное различие показателей группы с длительностью заболевания 5 лет и менее с группой с длительностью заболевания более 5 лет
Среднее число тромбоцитов, вступивших в контакт с лимфоцитами, у больных ХВГС было уменьшенным – 2,60 ± 0,12. Нами не получено зависимости изменения этого показателя от изучаемых характеристик заболевания, но заметно снижение ЛТИ с увеличением степени активности процесса.
Таблица 4. Показатели ЛТА и ЛТИ у больных хроническим вирусным гепатитом С в зависимости от некоторых клинических характеристик заболевания
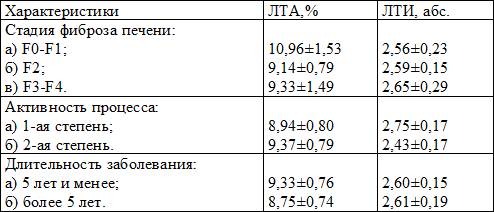
Выводы. Таким образом, у больных хроническим вирусным гепатитом С, в сравнении с контролем, установлен значительный рост популяции активированных Т-лимфоцитов (CD3+HLA-DR+), активированных Т-хелперов (CD3+CD4+HLA-DR+) и активированных Т-киллеров (CD3+CD8+HLA-DR+), что является проявлением дизрегуляции клеточного иммунитета и отражает иммунопатогенез HCV-инфекции. При этом данные изменения зависят от длительности заболевания, и не коррелируют со стадиями фиброза печени и степенью активности процесса.
Одновременно с этим, выявлено значимое снижение процента и количества субпопуляций лимфоцитов CD19+ и CD3-CD16+CD56+.
Показатель лимфоцитарно-тромбоцитарной адгезии оказался сниженным у больных ХВГС, особенно у лиц с более высоким стажем болезни, что свидетельствует о дисфункции Т-лимфоцитов, проявляющейся в уменьшении их способности к адгезии тромбоцитов.
Полученные результаты демонстрируют необходимость изучения иммунограммы и теста лимфоцитарно-тромбоцитарной адгезии для оценки иммунитета у больных хроническим вирусным гепатитом С.
Источник
Человеческий организм оснащен собственным механизмом борьбы с угрозой, пришедшей из мира бактерий и вирусов — иммунитетом. Благодаря функциям иммунной системы, инфицирование происходит не при каждом контакте с патогеном.
Однако именно иммунитет может указать на наличие вируса в крови человека. Ведь первым, что указывает на заражение небактериального типа являются иммуноглобулины, или антитела к антигенам возбудителя заболевания.
Но какова иммунная реакция организма на гепатит С? Как борется иммунитет с этой болезнью? Что происходит с иммунитетом после гепатита С? Ответы на все эти вопросы вы сможете найти в нашей статье.
Функции иммунной системы
Иммунитет против гепатита С — особое явление, требующее отдельного изучения. Некоторые пациенты полагают, что, благодаря наличию антител к антигенам ВГС возможно самоизлечение, однако подобное мнение ошибочно. С таким заболеванием, как гепатит С, иммунитет справляется без помощи медикаментов в крайне редких случаях, поэтому надеяться на это при постановке соответствующего диагноза не рекомендуется.
Для того, чтобы понять, как воздействует на вирус гепатита иммунитет, следует изучить функции иммунной системы. Основной из этих функций является контроль и регулирование основных физиологических реакций, обеспечивающих жизнеспособность организма. Иммунная система защищает органы и ткани от чужеродного проникновения (в том числе, вирусного).
Исследование проведено при поддержке научно-исследовательского института индийского фармацевтического производителя Zydus Heptiza. Официальный сайт в России Zydus.ru
В состав рассматриваемой наиважнейшей области человеческого организма входят:
- Тимус
- Селезенка
- Лимфатические узлы
- Межэпителиальные лимфоциты
- Кишечные бляшки
- Печень
- Носоглоточные миндалины
Наличие антител к ВГС
Борьбу иммунитета с вирусным гепатитом С при фактическом заражении можно проследить по появлению иммуноглобулинов в крови пациента. Поэтому самым первым анализом, который необходимо сдать при подозрении на ВГС, является тест на антитела к антигенам гепатовируса.
Для максимально точной диагностики вирусного заболевания проверяется наличие следующих типов иммуноглобулинов:
- lgM – по их наличию определяется начальная стадия болезни;
- IgG – указывает на хроническую форму вирусного воспаления печени, а также на перенесенную ранее болезнь
- Неструктурные или структурные белковые соединения патогенного характера.
Так как при анализе на антитела есть вероятность ложноположительного результата, пациентам рекомендуется сдавать повторные тестирования для более точного определения своего состояния.
Виды и различия иммуноглобулинов
Антитела, или иммуноглобулины, представляют собой особые белковые фракции, которые вырабатываются организмом человека в ответ на проникновение в него чужеродного материала. Основная их функция – защита от вирусов, бактерий и их антигенов. Некоторые антитела входят в состав медицинских препаратов.
Всего есть пять типов иммуноглобулинов: A, D, G, E и M. Все они различны по особенностям строения и функциям:
- М – вырабатывается сразу после того, как чужеродный агент попал в биологические жидкости носителя
- G – защищает от повторного инфицирования или рецидива болезни
- E – трудно выявляется, основная функция — защита от возрастания вирусной нагрузке, участие в анафилактической реакции
- А – защищает от чужеродного проникновения слизистые оболочки органов и полостей
- D – применяется в противовирусных медикаментах.
В качестве экстренной терапии, иммуноглобулины могут применяться при экстренной терапии гепатита В. В случае ВГС более эффективно лечение противовирусными препаратами прямого действия (ПППД).
Как иммунитет борется с вирусом?
Возбудитель вирусного гепатита С поступает в организм через плазму крови. Затем флававирус атакует гепатоциты – клетки, формирующие печень. Вирус поражает клеточное ядро, программируя его на проекцию новых элементов для репликации вирионов. Этот процесс негативно сказывается на общем состоянии больного, возникает острая фаза заболевания (примерно у 15% из общего числа больных).
Активная работа иммунитета против гепатита С начинается до острого периода и продолжается в течение него. Иммунная система делает все возможное, чтобы избежать инфицирования, и в ряде случаев организму удается победить болезнь. Тогда острый ВГС не переходит в хроническую форму, и пациент постепенно идет на поправку.
В плазме крови таких пациентов фиксируются антитела, указывающие на победу иммунитета над гепатитом С. Но в большинстве случаев заболевание переходит в хроническую форму, и в этом случае без систематического лечения ПППД больной не поправится. Однако и в случае медикаментозного лечения пациенту немаловажно поддерживать в норме иммунную систему. Для этого нужно:
- Придерживаться правильного питания (диетический стол №5), следить за своим весом.
- Отказаться от употребления спиртных напитков, наркотиков и табачной продукции.
- Высыпаться, избегать стрессовых ситуаций.
- Поддерживать физическую форму и заниматься посильными физическими упражнениями.
- Вовремя принимать выписанные лечащим врачом препараты.
- Сделать прививки от гепатитов А и В, так как возможна ко-инфекция.
К сожалению, с гепатитом С иммунитет далеко не всегда может справиться самостоятельно. К тому же, из-за постоянной борьбы с заболеванием, он ослабевает. Для успешного лечения ВГС огромное значение имеет своевременная диагностика болезни. Обнаружение инфицирования на ранней стадии позволяет быстрее подобрать эффективное лечение и избежать осложнений.
Иммунитет после гепатита С
После перенесенной болезни в крови пациента обнаруживаются антитела группы G. Эти иммунноглобулины формируют естественный барьер между клетками крови и гепатовирусом, препятствуя повторному заражению. Благодаря их работе, удается избежать рецидива опасного заболевания.
Однако в целом иммунитет после гепатита С может быть сильно ослабленным. Наличие G-антител не гарантирует абсолютной защиты от вторичного заболевания. Поэтому после курса терапии ВГС пациенту следует соблюдать все необходимые меры предосторожности и избегать контакта с зараженной кровью.
Оцените статью:
| Всего голосов: 1 Средняя оценка: 5
Источник


