Кишечные инфекции у детей методические
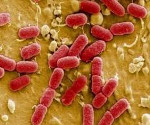
Кишечная инфекция у детей – группа инфекционных заболеваний различной этиологии, протекающих с преимущественным поражением пищеварительного тракта, токсической реакцией и обезвоживанием организма. У детей кишечная инфекция проявляется повышением температуры тела, вялостью, отсутствием аппетита, болями в животе, рвотой, диареей. Диагностика кишечной инфекции у детей основана на клинико-лабораторных данных (анамнезе, симптоматике, выделении возбудителя в испражнениях, обнаружении специфических антител в крови). При кишечной инфекции у детей назначаются антимикробные препараты, бактериофаги, энтеросорбенты; в период лечения важно соблюдение диеты и проведение регидратации.
Общие сведения
Кишечная инфекция у детей – острые бактериальные и вирусные инфекционные заболевания, сопровождающиеся кишечным синдромом, интоксикацией и дегидратацией. В структуре инфекционной заболеваемости в педиатрии кишечные инфекции у детей занимают второе место после ОРВИ. Восприимчивость к кишечной инфекции у детей в 2,5-3 раза выше, чем у взрослых. Около половины случаев кишечной инфекции у детей приходится на ранний возраст (до 3 лет). Кишечная инфекция у ребенка раннего возраста протекает тяжелее, может сопровождаться гипотрофией, развитием дисбактериоза и ферментативной недостаточности, снижением иммунитета. Частое повторение эпизодов инфекции вызывает нарушение физического и нервно-психического развития детей.
Кишечная инфекция у детей
Причины
Спектр возбудителей кишечных инфекций у детей крайне широк. Наиболее часто патогенами выступают грамотрицательные энтеробактерии (шигеллы, сальмонеллы, кампилобактеры, эшерихии, иерсинии) и условно-патогенная флора (клебсиеллы, клостридии, протей, стафилококки и др.). Кроме этого, встречаются кишечные инфекции, вызываемые вирусными возбудителями (ротавирусами, энтеровирусами, аденовирусами), простейшими (лямблиями, амебами, кокцидиями), грибами. Общими свойствами всех возбудителей, обусловливающих развитие клинических проявлений, являются энтеропатогенность, способность к синтезу эндо- и экзотоксинов.
Заражение детей кишечными инфекциями происходит посредством фекально-орального механизма алиментарным (через пищу), водным, контактно-бытовым путями (через посуду, грязные руки, игрушки, предметы обихода и т. д.). У ослабленных детей с низкой иммунологической реактивностью возможно эндогенное инфицирование условно-патогенными бактериями. Источником ОКИ может выступать носитель, больной со стертой или манифестной формой заболевания, домашние животные. В развитии кишечной инфекции у детей большую роль играет нарушение правил приготовления и хранения пищи, допуск на детские кухни лиц-носителей инфекции, больных тонзиллитом, фурункулезом, стрептодермией и пр.
Наиболее часто регистрируются спорадические случаи кишечной инфекции у детей, хотя при пищевом или водном пути инфицирования возможны групповые и даже эпидемические вспышки. Подъем заболеваемости некоторыми кишечными инфекциями у детей имеет сезонную зависимость: так, дизентерия чаще возникает летом и осенью, ротавирусная инфекция — зимой.
Распространенность кишечных инфекций среди детей обусловлена эпидемиологическими особенностями (высокой распространенностью и контагиозностью возбудителей, их высокой устойчивостью к факторам внешней среды), анатомо-физиологическими особенностями пищеварительной системы ребенка (низкой кислотностью желудочного сока), несовершенством защитных механизмов (низкой концентрацией IgA). Заболеваемости детей острой кишечной инфекцией способствует нарушение нормальной микробиоты кишечника, несоблюдение правил личной гигиены, плохие санитарно-гигиенические условия жизни.
Классификация
По клинико-этиологическому принципу среди кишечных инфекций, наиболее часто регистрируемых в детской популяции, выделяют шигеллез (дизентерию), сальмонеллез, коли-инфекцию (эшерихиозы), иерсиниоз, кампилобактериоз, криптоспоридиоз, ротавирусную инфекцию, стафилококковую кишечную инфекцию и др.
По тяжести и особенностям симптоматики течение кишечной инфекции у детей может быть типичным (легким, средней тяжести, тяжелым) и атипичным (стертым, гипертоксическим). Выраженность клиники оценивается по степени поражения ЖКТ, обезвоживания и интоксикации.
Характер местных проявлений при кишечной инфекции у детей зависит от поражения того или иного отдела ЖКТ, в связи с чем выделяют гастриты, энтериты, колиты, гастроэнтериты, гастроэнтероколиты, энтероколиты. Кроме локализованных форм, у грудных и ослабленных детей могут развиваться генерализованные формы инфекции с распространением возбудителя за пределы пищеварительного тракта.
В течении кишечной инфекции у детей выделяют острую (до 1,5 месяцев), затяжную (свыше 1,5 месяцев) и хроническую (свыше 5-6 месяцев) фазы.
Симптомы у детей
Дизентерия у детей
После непродолжительного инкубационного периода (1-7 суток) остро повышается температура (до 39-40° C), нарастает слабость и разбитость, снижается аппетит, возможна рвота. На фоне лихорадки отмечается головная боль, ознобы, иногда – бред, судороги, потеря сознания. Кишечная инфекция у детей сопровождается схваткообразными болями в животе с локализацией в левой подвздошной области, явлениями дистального колита (болезненностью и спазмом сигмовидной кишки, тенезмами с выпадением прямой кишки), симптомами сфинктерита. Частота дефекации может варьировать от 4-6 до 15-20 раз за сутки. При дизентерии стул жидкий, содержащий примеси мутной слизи и крови. При тяжелых формах дизентерии возможно развитие геморрагического синдрома, вплоть до кишечного кровотечения.
У детей раннего возраста при кишечной инфекции общая интоксикация преобладает над колитическим синдромом, чаще возникают нарушения гемодинамики, электролитного и белкового обмена. Наиболее легко у детей протекает кишечная инфекция, вызванная шигеллами Зоне; тяжелее — шигеллами Флекснера и Григорьеза-Шига.
Сальмонеллез у детей
Наиболее часто (в 90% случаев) развивается желудочно-кишечная форма сальмонеллеза, протекающая по типу гастрита, гастроэнтерита, гастроэнтероколита. Характерно подострое начало, фебрильный подъем температуры, адинамия, рвота, гепатоспленомегалия. Стул при сальмонеллезе жидкий, обильный, каловый, цвета «болотной тины», с примесями слизи и крови. Обычно данная форма кишечной инфекции заканчивается выздоровлением, однако у грудных детей возможен летальный исход вследствие тяжелого кишечного токсикоза.
Гриппоподобная (респираторная) форма кишечной инфекции встречается у 4-5% детей. При данной форме сальмонеллы обнаруживаются в посеве материала из зева. Ее течение характеризуется фебрильной температурой, головной болью, артралгией и миалгией, явлениями ринита, фарингита, конъюнктивита. Со стороны сердечно-сосудистой системы отмечаются тахикардия и артериальная гипотония.
На тифоподобную форму сальмонеллеза у детей приходится 2% клинических случаев. Она протекает с длительным периодом лихорадки (до 3-4-х недель), выраженной интоксикацией, нарушением функции сердечно-сосудистой системы (тахикардией, брадикардией).
Септическая форма кишечной инфекции обычно развивается у детей первых месяцев жизни, имеющих неблагоприятный преморбидный фон. На ее долю приходится около 2-3% случаев сальмонеллеза у детей. Заболевание протекает крайне тяжело, сопровождается септицемией или септикопиемией, нарушением всех видов обмена, развитием тяжелых осложнений (пневмонии, паренхиматозного гепатита, отоантрита, менингита, остеомиелита).
Эшерихиозы у детей
Данная группа кишечных инфекций у детей крайне обширна и включает коли-инфекци, вызываемые энтеропатогенными, энтеротоксигенными, энтероинвазивными, энтерогеморрагическими эшерихиями.
Кишечная инфекция у детей, вызванная эшерихиями, протекает с субфебрильной или фебрильной температурой, слабостью, вялостью, снижением аппетита, упорной рвотой или срыгиваниями, метеоризмом. Характерна водянистая диарея (обильный, брызжущий стул желтого цвета с примесью слизи), быстро приводящая к дегидратации и развитию эксикоза. При эшерихиозе, вызываемом энтерогеморрагическими эшерихиями, диарея носит кровавый характер.
Вследствие обезвоживания у ребенка возникает сухость кожи и слизистых оболочек, снижается тургор и эластичность тканей, западает большой родничок и глазные яблоки, снижается диурез по типу олигурии или анурии.
Ротавирусная инфекция у детей
Обычно протекает по типу острого гастроэнтерита или энтерита. Инкубационный период в среднем длится 1-3 дня. Все симптомы кишечной инфекции у детей разворачиваются в течение одних суток, при этом поражение ЖКТ сочетается с катаральными явлениями.
Респираторный синдром характеризуется гиперемией зева, ринитом, першением в горле, покашливанием. Одновременно с поражением носоглотки развиваются признаки гастроэнтерита: жидкий (водянистый, пенистый) стул с частотой дефекаций от 4-5 до 15 раз в сутки, рвотой, температурной реакцией, общей интоксикацией. Длительность течения кишечной инфекции у детей – 4-7 дней.
Стафилококковая кишечная инфекция у детей
Различают первичную стафилококковую кишечную инфекцию у детей, связанную с употреблением пищи, обсемененной стафилококком, и вторичную, обусловленную распространением возбудителя из других очагов.
Течение кишечной инфекции у детей характеризуется тяжелым эксикозом и токсикозом, рвотой, учащением стула до 10-15 раз в день. Стул жидкий, водянистый, зеленоватого цвета, с небольшой примесью слизи. При вторичной стафилококковой инфекции у детей кишечные симптомы развиваются на фоне ведущего заболевания: гнойного отита, пневмонии, стафилодермии, ангины и пр. В этом случае заболевание может принимать длительное волнообразное течение.
Диагностика
На основании осмотра, эпидемиологических и клинических данных педиатр (детский инфекционист) может лишь предположить вероятность кишечной инфекции у детей, однако этиологическая расшифровка возможна только на основании лабораторных данных.
Главную роль в подтверждении диагноза кишечной инфекции у детей играет бактериологическое исследование испражнений, которое следует проводить как можно ранее, до начала этиотропной терапии. При генерализованной форме кишечной инфекции у детей проводится посев крови на стерильность, бактериологическое исследование мочи, ликвора.
Определенную диагностическую ценность представляют серологические методы (РПГА, ИФА, РСК), позволяющие выявлять наличие Ат к возбудителю в крови больного с 5-х суток от начала болезни. Исследование копрограммы позволяет уточнить локализацию процесса в ЖКТ.
При кишечной инфекции у детей требуется исключить острый аппендицит, панкреатит, лактазную недостаточность, дискинезию желчевыводящих путей и др. патологию. С этой целью проводятся консультации детского хирурга и детского гастроэнтеролога.
Лечение кишечной инфекции у детей
Комплексное лечение кишечных инфекций у детей предполагает организацию лечебного питания; проведение оральной регидратации, этиотропной, патогенетической и симптоматической терапии.
Диета детей с кишечной инфекцией требует уменьшения объема питания, увеличения кратности кормлений, использования смесей, обогащенных защитными факторами, употребление протертой легкоусвояемой пищи. Важной составляющей терапии кишечных инфекций у детей является оральная регидратация глюкозо-солевыми растворами, обильное питье. Она проводится до прекращения потерь жидкости. При невозможности перорального питания и употребления жидкости назначается инфузионая терапия: внутривенно вводятся растворы глюкозы, Рингера, альбумина и др.
Этиотропная терапия кишечных инфекций у детей проводится антибиотиками и кишечными антисептиками (канамицин, гентамицин, полимиксин, фуразолидон, налидиксовая кислота), энтеросорбентами. Показан прием специфических бактериофагов и лактоглобулинов (сальмонеллезного, дизентерийного, колипротейного, клебсиеллезного и др.), а также иммуноглобулинов (антиротавирусного и др.). Патогенетическая терапия предполагает назначение ферментов, антигистаминных препаратов; симптоматическое лечение включает прием жаропонижающих, спазмолитиков. В период реконвалесценции необходима коррекция дисбактериоза, прием витаминов и адаптогенов.
Прогноз и профилактика
Раннее выявление и адекватная терапия обеспечивают полное выздоровление детей после кишечной инфекции. Иммунитет после ОКИ нестойкий. При тяжелых формах кишечной инфекции у детей возможно развитие гиповолемического шока, ДВС-синдрома, отека легких, острой почечной недостаточности, острой сердечной недостаточности, инфекционно-токсического шока.
В основе профилактики кишечных инфекций у детей – соблюдение санитарно-гигиенических норм: правильное хранение и термическая обработка продуктов, защита воды от загрязнения, изоляция больных, проведение дезинфекции игрушек и посуды в детских учреждениях, привитие детям навыков личной гигиены. При уходе за грудным ребенком мама не должна пренебрегать обработкой молочных желез перед кормлением, обработкой сосок и бутылочек, мытьем рук после пеленания и подмывания ребенка.
Дети, контактировавшие с больным кишечной инфекцией, подлежат бактериологическому обследованию и наблюдению в течение 7 дней.
Источник
По данным ВОЗ, ежегодно в мире умирают от ОКИ и их осложнений более 5 млн детей. Не менее актуальна эта проблема и для Российской Федерации. По данным Федерального центра Госсанэпиднадзора, в 2009 г. в России на долю детского населения приходится более 60% эпизодов инфекционной диареи.
Актуальность проблемы острой диареи определяется еще и тем обстоятельством, что большинство таких больных (по результатам опросов) предпочитают лечиться самостоятельно.
В патогенезе развития кишечной инфекции особое место занимает нарушение нормальной микрофлоры кишечника, регистрируемое у 95–97% больных. Являясь одной из мощнейших естественных защитных систем организма, нормальная микробиота кишечника также выполняет ряд других, не менее важных, функций, таких как трофическая и энергетическая, стимуляции перистальтики кишечника, участие в дифференцировке и регенерации тканей, детоксикация и выведение эндо– и экзогенных ядовитых соединений, разрушение мутагенов, активация действия лекарственных веществ, поддержание ионного гомеостаза, образование сигнальных молекул (нейротрансмиттеров), стимуляция местного и системного иммунитета, образования иммуноглобулинов, обеспечение цитопротекции и колонизационной резистентности, участие в процессах полостного пищеварения, синтезе витаминов В, К и обмене веществ, и др.
В то же время количественно и качественно измененная микробиота кишечника становится источником интоксикации и сенсибилизации, потенцирует патологические процессы в кишечнике, снижает темпы репаративных процессов, представляет собой одно из ключевых звеньев сложной цепи хронизации заболеваний желудочно–кишечного тракта (ЖКТ) и др. Проведенные ранее исследования показали, что развивающийся при ОКИ дисбактериоз утяжеляет их течение, способствуя хронизации процесса и формированию упорных диарей, снижает эффективность проводимой терапии. Известно, что у детей с ОКИ, успешно леченных по поводу токсикоза и эксикоза, не отмечается нормализация дисбиотических реакций, что приводит к дистрофии, повышению частоты летальных исходов от повторных ОКИ или ОРЗ.
Между тем в работах, посвященных дисбактериозу при ОКИ у детей, речь идет преимущественно об остром периоде болезни. В этой связи особое место в комплексной терапии ОКИ занимает своевременная и эффективная коррекция дисбиотических нарушений. Для этого традиционно используют пробиотические и пребиотические препараты. Первые представляют собой живые микроорганизмы (различные виды лакто– и бифидобактерий, Enterococcus faecium), вторые – неперевариваемые пищевые ингредиенты, оказывающие избирательное влияние на рост и/или активность ограниченного числа бактерий в кишечнике.
Однако эффективным использование пробиотиков в остром периоде ОКИ признано только в отношении ротавирусной инфекции. Нет однозначного мнения об использовании пробиотиков при бактериальных кишечных инфекциях. В данной ситуации использование пребиотиков является более предпочтительным, так как создает условия для скорейшего восстановления баланса собственной облигатной микрофлоры. На сегодняшний день существует большое количество пребиотических препаратов, пищевых добавок, продуктов, обогащенных пребиотиками. Одними из наиболее эффективных препаратов с пребиотическим эффектом, применяемых для коррекции дисбиоза, являются препараты лактулозы.
Лактулоза – дисахарид, состоящий из галактозы и фруктозы, в молоке (женском или коровьем) отсутствует, однако в небольших количествах может образовываться при нагревании молока до температуры кипения. Лактулоза не переваривается ферментами ЖКТ, ферментируется лакто– и бифидобактериями и служит им субстратом для энергетического и пластического обмена, за счет чего способствует их росту и нормализации состава микрофлоры, увеличению объема биомассы и каловых масс, что определяет ее слабительный эффект. Помимо этого, показаны антикандидозная активность лактулозы и ее угнетающий эффект в отношении сальмонелл.
Наиболее известным препаратом лактулозы является Дюфалак. В стандартных дозах он широко используется как слабительное средство, при этом возрастает объем каловых масс за счет высоких адсорбционных свойств препарата и ускоряется кишечный транзит. Пребиотический эффект при такой дозировке незначителен.
С пребиотической целью детям лактулоза назначается в низких дозах (по 1,5–2,5 мл 2 р./сут. в течение 3–6 нед.). Доза лактулозы подбирается индивидуально с тем, чтобы не вызывать слабительного эффекта.
Нередко перенесенная ОКИ приводит к экзокринной дисфункции поджелудочной железы (ПЖ), которая может быть следствием снижения выработки ферментов ПЖ. Нередко ферментная недостаточность обусловлена нарушением активации ферментов в тонком кишечнике. Вследствие нарушения функции экзокринного аппарата ПЖ, приводящей к мальдигестии, часто развивается нарушение всасывания пищевых веществ (мальабсорбция). Известно, что ПЖ обладает большими компенсаторными возможностями, и нарушения панкреатической секреции проявляются лишь при ее тяжелом поражении. Стеаторея и креаторея у взрослых развиваются в тех случаях, когда секреция панкреатической липазы и трипсина снижается более чем на 90%. Среди клинических проявлений внешнесекреторной недостаточности ПЖ у детей отмечаются: понос, метеоризм, боли в животе, стеаторея, тошнота, периодически рвота, нередко – снижение аппетита, общая слабость, похудание, снижение физической активности, отставание в росте (при тяжелых формах).
В основе внешнесекреторной недостаточности ПЖ лежат следующие механизмы [3]:
• незрелость ПЖ;
• деструкция ацинарных клеток (снижается синтез ферментов);
• обструкция панкреатического протока, нарушающая поступление панкреатического сока в 12–перстную кишку;
• уменьшение секреции бикарбонатов эпителием протоков ПЖ, в результате чего происходит снижение рН 12–перстной кишки до 4,0 и ниже, денатурация панкреатических ферментов и преципитация желчных кислот;
• недостаточность активации ферментов вследствие дефицита энтерокиназы и желчи;
• дискинезия 12–перстной и тонкой кишки, вследствие чего наблюдается нарушение смешивания ферментов с пищевым химусом;
• нарушение кишечного микробиоценоза (инактивация и разрушение ферментов);
• гипоальбуминемия вследствие дефицита белка в пище (нарушение синтеза ферментов).
При выявлении симптомов, свидетельствующих об экзокринной недостаточности ПЖ, необходимо рано, до развития мальабсорбции, начать заместительную терапию панкреатическими ферментами в зависимости от степени экзокринной недостаточности ПЖ. Лечение панкреатической недостаточности прежде всего направлено на ликвидацию нарушений переваривания жиров, белков и углеводов и включает назначение специальной высококалорийной диеты и заместительную терапию ферментами. Используя эти методы лечения, можно уменьшить или ликвидировать проявления мальдигестии и мальабсорбции, так как панкреатические энзимы играют ключевую роль в кишечном полостном пищеварении благодаря наличию в них липазы, амилазы и протеазы.
От того, насколько эффективно осуществляется гидролиз нутриентов, зависят их дальнейшее расщепление, всасывание и транспорт. Наиболее трудной задачей является ликвидация стеатореи. Некоторые традиционно используемые педиатрами ферментные препараты обладают определенными технологическими и фармакологическими недостатками, а также низкой активностью в 12–перстной кишке. Препараты для заместительной терапии внешнесекреторной недостаточности ПЖ у детей должны [2–4]:
• иметь в своем составе липазу, расщепляющую липиды и обеспечивающую энергетический баланс организма;
• быть устойчивыми к соляной кислоте (панкреатическая липаза неустойчива в кислой среде);
• быстро смешиваться с химусом и транспортироваться в 12–перстную кишку (процесс расщепления липидов осуществляется в 12–перстной кишке в течение 1–1,5 ч);
• обладать максимумом действия при рН 5–7;
• иметь хорошую переносимость;
• не иметь токсичности.
Препараты панкреатических ферментов способствуют перевариванию белков, жиров и углеводов и назначаются в качестве заместительной терапии при внешнесекреторной недостаточности ПЖ. Несмотря на то, что в арсенале врача в настоящее время имеется много ферментных препаратов ПЖ, не всегда можно обеспечить адекватную заместительную терапию, особенно у больных с хронической панкреатической недостаточностью [4]. Назначая тот или иной препарат, врач прежде всего должен учитывать его состав и иметь сведения об активности его компонентов.
В настоящее время в Российской Федерации зарегистрировано большое количество ферментных препаратов в виде микротаблеток, капсул, драже, таблеток, порошков, гранул, выбор которых для лечения конкретного ребенка представляет определенные трудности.
Целью исследования явилось изучение терапевтической эффективности и переносимости панкреатина (Креон) у детей с нарушениями пищеварения на фоне относительной экзокринной недостаточности ПЖ, возникшей вследствие ОКИ, и лактулозы с пребиотической целью.
Материалы и методы
Под нашим наблюдением были 60 детей, больных ОКИ, в возрасте от 6 мес. до 6 лет, находившихся на стационарном лечении в ДИБ г. Краснодара. С учетом различий в комплексной терапии острой диареи все наблюдавшиеся больные были распределены методом случайной выборки на 3 группы.
В основную группу А были включены 20 детей, которые на фоне традиционной терапии ОКИ, включавшей диету, пероральную регидратацию, сорбентные препараты (неосмектин, энтеросгель), получали лактулозу в пребиотической дозировке (1,5–3 мл). Основную группу В составили 20 пациентов, получавших панкреатин и лактулозу в пребиотической дозировке. В группу сравнения вошли 20 детей, которым были назначены диета, пероральная регидратация, сорбентные препараты (неосмектин, энтеросгель). Средняя продолжительность курса приема лактулозы и панкреатина составила 12±2 дня.
Диагноз и оценку степени тяжести течения ОКИ устанавливали на основании утвержденного Минздравом РФ пособия для врачей «Диагностика и лечение ОКИ у детей» [Милютина Л.Н., Горелов А.В., Воротынцева Н.В., М., 1999].
Анализ клинических наблюдений позволил установить, что заболевание протекало преимущественно по типу водянистой диареи, в форме гастроэнтерита – у 68,3% детей, энтерита – у 28,3%. Течение ОКИ у всех детей было гладким, легкие формы заболевания регистрировали у 45% больных, среднетяжелые формы ОКИ – у 55%. Большинство больных (70%) госпитализировались в стационар в первые 2 дня заболевания, лишь 2 ребенка – в поздние сроки. Начало заболевания у 91,7% детей было острым. У 23,3% больных первым симптомом заболевания стало появление жидкого стула, у 16,6% – рвоты, а у 60,0% – сочетание этих симптомов. У 26,6% больных отмечено повышение температура до субфебрильных цифр, а у 5% – выше 39,5оС. Дети жаловались на снижение аппетита, слабость, вялость, в 36,7% случаев – на боли в животе и урчание. Частота стула уже в первые сутки заболевания была от 4–6 (у 55%) до 10–12 раз (у 23,3%). В большинстве случаев стул был жидкий, без патологических примесей. Как видно из таблицы 1, сравниваемые группы пациентов были полностью сопоставимы.
Для оценки эффективности изучаемых препаратов с целью восстановления микроэкологических нарушений кишечника у 30 детей (по 10 пациентов в каждой из групп) было проведено исследование микрофлоры толстой кишки по методике Р.В. Эпштейн–Литвак и Ф.Л. Вильшанской. Исследования проведены в динамике – до начала приема препаратов и после его окончания.
Обработка цифрового материала результатов исследования проводилась с использованием параметрических и непараметрических методов в соответствии с общепризнанными методами статистики при помощи пакета прикладных программ Statistica 6,0 (StatSoft, USA). Вычисляли следующие величины: среднюю арифметическую (М); среднюю ошибку средней величины (m) (ошибку репрезентативности). Достоверность различий (р) результатов исследования оценивали по критерию Стъюдента. Различие расценивали как достоверное при р<0,05.
Результаты и их обсуждение
Сопоставление динамики клинических симптомов ОКИ позволило установить, что включение в терапию основной группы детей панкреатина и лактулозы с первых дней заболевания сопровождалось более быстрым купированием гастроинтестинальных симптомов.
Наиболее выраженный клинический эффект наблюдался в группе пациентов, получавших сочетание лактулозы с панкреатином (основная группа В). Длительность диареи у больных в данной группе была достоверно меньше (4,24±0,21 сут.), чем в основной группе А (5,6±0,48 сут.) и в группе сравнения (6,2±0,52 сут.) (р<0,01). У больных, получавших пребиотический препарат, наблюдали также более быстрое прекращение метеоризма: 4,4±0,32 сут. в группе А, 3,8±0,46 сут. – в группе В в сравнении с 5,1±0,42 сут. в группе получавших только энтеросорбенты. Нами не было выявлено влияния лактулозы и панкреатина на сроки купирования симптомов инфекционного токсикоза и рвоты.
Необходимо отметить хорошую переносимость лактулозы и панкреатина, а также отсутствие каких–либо негативных побочных реакций, в том числе аллергических.
При комплексной оценке клинической эффективности терапии установлено, что наибольшая частота «хорошего» эффекта от лечения наблюдалась в группе больных, получавших панкреатин совместно с лактулозой (рис. 1).
В то же время при включении только лактулозы в традиционную терапию было отмечено повышение клинической эффективности на 20%. Отсутствие клинического эффекта от проводимого лечения к концу 3–х сут. реже всего наблюдалось в группе получавших лактулозу + панкреатин (у 1 больного). В группе сравнения количество таких детей было значительно больше – 4.
Сравнительная оценка состояния микрофлоры толстой кишки на фоне терапии была проведена у 30 больных – по 10 в каждой из групп. Было установлено, что в остром периоде кишечной инфекции у 100% больных развиваются дисбиотические нарушения различной степени, характеризующиеся снижением уровня лактобактерий (у 63,3% детей), бифидобактерий (у 80%), нормальной кишечной палочки (у 66,7%), повышением уровня кишечной палочки с измененной ферментативной активностью (у 33,3%), гемолизирующей E. coli (у 23,3%), ростом количества условно–патогенных микроорганизмов (у 16,7%), золотистого стафилококка (у 36,7%) и дрожжевых грибов (у 23,3%).
Как видно из данных таблицы 2, характер дисбиотических нарушений до начала лечения существенно не различался между группами (единственным отличием было в 2 раза большее количество детей со сниженным уровнем лактобактерий в группе Стимбифид + бифидумбактерин).
Использование лактулозы при ОКИ способствовало улучшению микроэкологического пейзажа, в том числе восстановлению нормального уровня бифидобактерий у 50% больных, нормальной кишечной палочки – у 50%. Положительные изменения состава облигатной микрофлоры способствовали элиминации E. coli с измененной ферментативной активностью у 30% пациентов, Staphylococcus aureus – у всех больных этой группы, снижению уровня дрожжевых грибов – у 30%.
Еще больший эффект был достигнут при совместном использовании панкреатина и лактулозы: дефицит бифидобактерий был ликвидирован у 70% больных, нормализация уровня E. coli достигнута у 50%, отмечалась также полная элиминация условно–патогенных бактерий (клебсиелла, цитробактер) и St. aureus.
Наименьшие положительные изменения состава микрофлоры толстой кишки наблюдались в группе пациентов, получавших только традиционную терапию: у 60% детей сохранялся дефицит лакто– и бифидобактерий, не изменялся уровень нормальной кишечной палочки, с той же частотой обнаруживались дрожжевые грибы и St. aureus.
При анализе структуры дисбиотических нарушений по степени их выраженности (в соответствии с отраслевым стандартом «Протокол ведения больных. Дисбактериоз кишечника» (утвержден приказом № 231 Минздрава РФ от 9.06.2003)) было установлено, что они в остром периоде заболевания в сравниваемых группах существенно не различались (табл. 3).
Преобладали II и III степени дисбактериоза. На фоне терапии лактулозой с первых дней ОКИ восстановление нормофлоры отмечено у 20% больных, а в комплексе с панкреатином – у 50%.
Среди получавших лактулозу после окончания лечения не было выявлено ни одного пациента с III степенью дисбактериоза. В то же время при использовании бифидумбактерина в виде монотерапии при ОКИ выраженность микроэкологических нарушений не изменялась: дисбактериоз III степени был отмечен у 20% детей, II степени – у 60%, не было зафиксировано ни одного случая восстановления эубиоза.
Выводы
1. Включение в комплексную терапию ОКИ у детей 1–12 лет лактулозы в пребиотической дозировке в сочетании с панкреатином в возрастных дозировках курсом не менее 14 дней повышает эффективность терапии и способствует сокращению длительности диарейного синдрома и метеоризма.
2. Использование лактулозы в остром периоде ОКИ у детей как в виде монотерапии, так и в сочетании с панкреатином оказывает положительное влияние на состояние микроэкологии толстой кишки, обеспечивая восстановление нормального уровня бифидобактерий, повышение уровня нормальной кишечной палочки, а также элиминацию условно–патогенных микроорганизмов. Для обеспечения полноценного восстановления микроэкологии кишечника наиболее целесообразно совместное использование лактулозы и панкреатина.
4. Для повышения эффективности корригирующего биоценоз потенциала монотерапии лактулозой необходимо удлинение курса применения препарата до 30 дней.
Источник


