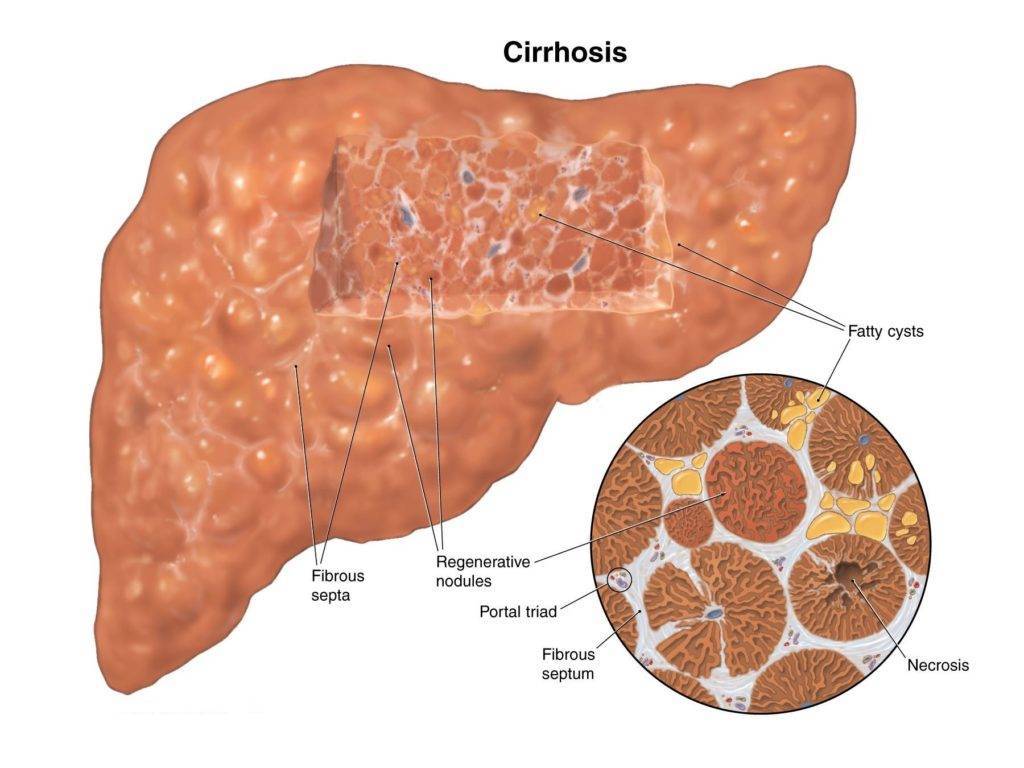
Плазма крови при циррозе
Лечение гепатита путем механического очищения крови


Славский Ростислав Игоревич
Врач-анестезиолог-реаниматолог
Специалист по экстракорпоральным методам лечения
Медицинский портал «Эксперты в области медицины»

Плазмаферез в хирургии применяется как универсальное средство, позволяющее с одной стороны производить дезинтоксикацию после больших оперативных вмешательств, успешно лечить сепсис и иные патологии, с другой в некоторой мере справлять с полиорганной недостаточностью, точнее, с ее первыми клиническими проявлениями. Необходимо заметить, что плазмаферез в настоящее время едва ли способен повлиять на гомеостаз организма при имеющихся дисфункциях со стороны почек. Несмотря на то, что мочевина и креатинин находятся в сосудистом русле в преобладающем количестве, и, казалось бы, при удалении плазмы ее концентрация должна снижаться, но на практике такого не происходит и вот почему.
При механическом очищении крови от плазмы мочевина уходит вместе с ней, но рефлекторно для уравновешивания осмотической концентрации моментально происходит ее выход из тканевой жидкости, что только усугубляет течение болезни. Лабораторно уже в первые часы после процедуры уровень мочевины достигает прежних значений и может даже быть больше, что только указывает на отсутствие эффективности данной процедуры и ее нецелесообразности. В данном случае не поможет даже и более дорогой и сложный метод, как мультрифильтрация крови – результаты примерно аналогичные. Все будет упираться в необходимость проведения гемодиализа и только него.
При заболеваниях печени плазмаферез является отличным эффективным средством очищения крови, недорогим и доступным, однако, он показан и разрешен только при компенсации и субкомпенсации печеночной деятельности. Дело в том, что вместе с плазмой и токсинами, имеющими печеночное происхождение удаляются многое полезные вещества, синтезируемые как раз в печени. А если наблюдается ее значимое угнетение функции, выходит замкнутый круг. Для таких клинических ситуаций как раз показана мультифильтрация, а плазмаферез вовсе запрещен.
Итак, плазмаферез при заболеваниях печени позволяет добиться следующих результатов:
1) Очищение крови от продуктов неполного метаболизма в печени, т.е. различных токсичных метаболитов.
2) Снижение концентрации печеночных ферментов, патологичных для сосудистого русла.
3) Снижение концентрации прямого и непрямого билирубина, т.е. нивелирование симптомов желтухи, что является клинически важным для профилактики осложнений.
Патологии печени и билиарной системы занимают ключевое место в болезнях ЖКТ, и вопросы их лечения крайне актуальны, однако, принципиальных подходов множество, что требует детального изучения. В тексте данной статьи мы решили остановиться на лечении печени плазмаферезом, о нем мы вам и поведали. Необходимо заметить, что речь идет только о симптоматической заместительной терапии, т.е. полностью отказаться от медикаментозных препаратов нельзя, поддерживающих метаболизм в гепатоцитах (клетки печени) нельзя. Также если существует факт обструкции желчных протоков, первоначально подлежит устранению именно та самая причина, а только потом пациент проходит курс восстановительного лечения. Постепенно явления желтухи уйдут, на фоне курсового приема лекарств и плазмафереза в частности, если это возможно в силу технических причин. Мы хотим донести до читателя ту точку зрения, согласно которой ферез плазмы при болезнях печени не является единственным эффективным методом, а также универсальным лечебным методом, а только дополнением к возможной схеме терапии. Плазмаферез является относительно новой технологией, ставшей доступной благодаря техническому прогрессу.
Говоря о лечебной тактике в отношении гепатитов, необходимо понять сперва этиологический фактор в данном патологическом процессе. В арсенале врача множество вариантов лечения, причем комбинация некоторых из них при учете, например, острого вирусного процесса, может только навредить пациенту. Необходимо понимать, что сам термин гепатит означает наличие воспалительного процесса, а последний бывает как вирусный, так и токсический, или с неизвестной этиологией. Лечение гепатита плазмаферезом эффективно только как дополнение при любом раскладе, что мы перечислили. Острые фазы необходимо компенсировать путем применения ультрафильтрации, более дорогого и технически сложного метода, а хронические варианты течения, которые перешли из острого процесса, более благоприятны для терапии.
Цирроз печени, использование современных методов очищения крови
Цирроз печени представляет собой необратимый патологический процесс, при котором на месте функционально активной печеночной ткани появляется патологическая соединительно-тканная. Заболевание достаточно хорошо изучено, в том числе этиологический фактор, тем не менее, эффективного лечения на данный момент не существует. Мы же упомянем про популярные у населения эфферентные методы лечения цирроза печени. Безусловно, при цирротическом процессе функция очищающей способности печени снижается в зависимости от стадии развития болезни. И в силу этих обстоятельств применяются различные способы компенсировать интоксикацию продуктами обмена или распада. Ультрафильтрация технически совершенный метод лечения, позволяющий его применять даже на самых поздних стадиях цирроза, когда имеются даже нарушения со стороны свертывающей системы крови, имеются признаки расширения вен пищевода (эндоскопическое исследование), другие тяжелые осложнения. Ультрафильтрация позволяет продлить жизнь больного, очищая при этом кровь путем постоянной циркуляции через специальные фильтры. Точного процента очищения крови нет, но приблизительно свыше 80% всех патогенных частиц могут элиминироваться из сосудистого русла. Метод эффективен, однако, технически более недоступен. Лечение цирроза печени плазмаферезом позволяет добиться 100% снижения всех видов патогенных соединений, так как удаляется определенная фракция плазмы, но в количественном соотношении он намного уступает ультрафильтрации, так как убрать всю плазму вместе с продуктами распада невозможно по причине удаления и полезного белка, гормонов и других биологически активных соединений. Также необходимо обратить внимание, что плазмаферез противопоказан при имеющихся нарушений со стороны свертывающей систем крови, при сниженном белке на фоне болезни и многих других осложнениях. Одним словом, речь идет только о начальных и средних стадиях.
Итак, плазмаферез показан при лечении гепатитов, цирроза печени как средства дополнительного выбора на стадии компенсации и субкомпенсации печеночной деятельности. Необходимо понимать, что лечение гепатитов и цирроза печени плазмаферезом требует индивидуального подхода к каждому пациента, обсуждая схемы лечения. Выраженность заболеваний печени может крайне варьировать, что на практике позволяет выбирать количество циклов от 2 до 8 в месяц.
Источник
Несмотря на то, что отечно-асцитический синдром при циррозе печени является одним из ярких и типичных проявлений манифестации заболевания, патофизиология асцита у пациентов с портальной гипертензией все еще не ясна. Она является последствием сложного нарушения гомеостаза электролитов и воды, вызванного структурными и функциональными нарушениями функции печени, дисрегуляцией системной гемодинамики и изменениями почечной функции. На этот процесс оказывают влияние некоторые гормоны, медиаторы, а также нейрогуморальные нарушения.
Повышенное портальное давление является необходимой предпосылкой для возникновения асцита. Пониженный синтез альбумина печенью приводит к сдвигу сил Старлинга. Однако портальная гипертензия сама по себе, как правило, не ведет к возникновению асцита, нарушение системной гемодинамики является обязательным условием ее возникновения. Периферическое расширение сосудов имеет место уже на стадии компенсированного цирроза. Изменения, вызванные ренином, альдостероном, вазопрессином и норадреналином, приводят к сужению почечных сосудов и удержанию натрия и воды, на начальной стадии заболевания могут быть компенсированы при помощи расширения объема плазмы. При суб- и декомпенсированном циррозе расширение объема плазмы недостаточно для компенсации периферической вазодилатации, и кроме того, возникновение гипоальбуминемии способствует развитию асцита.
На поздних стадиях цирроза печени асцит развивается у 50-85% больных, у 25% больных он является первым симптомом болезни. Развитие у больного отечно-асцитического синдрома означает переход заболевания в сложную по патогенезу стадию и меняет принципы лечения.
Патогенез асцита при циррозе печени связан с взаимодействием нескольких факторов:
механического, обусловленного портальной гипертензией;
гормонального;
нервно-гуморального звеньев;
обусловленных гемодинамическими сдвигами и нарушениями водно-электролитного равновесия.
Повышение синусоидального гидростатического давления при внутрипеченочной портальной гипертензии приводит к повышенной транссудации богатого белком фильтрата через стенки синусоидов в пространства Диссе, выраженному увеличению образования печеночной лимфы и объема интерстициальной жидкости на фоне снижения ее онкотического давления в результате дефицита синтеза альбумина. Значительная часть лимфы, образующейся при избытке интерстициальной жидкости, поступает в большой круг кровообращения через систему лимфатических сосудов печени и грудной лимфатический проток, при этом накопление интерстициальной жидкости превышает ее эвакуацию через лимфатическую систему, поэтому жидкость пропотевает в брюшную полость в результате чего возникает асцит. Отток лимфы от печени при циррозе печени достигает 15-20 л/сут. и более при норме 8-9 л.
Наряду с накоплением асцитической жидкости снижается центральное внутрисосудистое давление. Объем плазмы крови при циррозе печени повышен, значительная ее часть депонирована в сосудах брюшной полости, поэтому эффективный, т.е. участвующий в циркуляции, объем плазмы снижен. Снижение эффективного объема плазмы приводит к активации ренин-ангиотензин-альдостероновой системы, одной из функций которой в физиологических условиях является регуляция эффективного объема плазмы крови, водно-электролитного, кислотно-основного состояния и артериального давления.
Ренин-ангиотензин-альдостероновая система активируется непосредственно под влиянием нарушения внутрипеченочной гемодинамики. Повышенная секреция ренина в юкстагломерулярном аппарате почек приводит к нарастанию синтеза ангиотензина I из синтезируемого печенью ангиотензиногена (а2-глобулина); ангиотензин I превращается в ангиотензин II, обладающий сосудосуживающим эффектом и уменьшающий гломерулярную фильтрацию и почечный кровоток. Ангиотензин II стимулирует секрецию антидиуретического гормона гипофиза (АДГ, вазопрессин) и минералокортикоидного гормона — альдостерона, который вырабатывается в клетках клубочковой зоны коры надпочечников и метабол из и руется печенью. Альдостерон вызывает повышение реабсорбции натрия и воды в обмен на экскрецию ионов калия и водорода в дистальных отделах нефрона — восходящей части петли Генле и дистальных канальцах при наличии в просвете этих частей нефрона ионов натрия, поступающих сюда из проксимальных отделов.
Чрезмерная потеря калия и водорода в условиях повышенной продукции альдостерона сопровождается гипокалиемией (калий сыворотки крови < 3,5 ммоль/л), гипомагниемией (< 1,4 ммоль/л) и метаболическим алкалозом. Экскреция натрия с мочой значительно снижена (< 150 ммоль/сут.). Несмотря на задержку натрия, у большинства больных развивается гипонатриемия (натрий сыворотки < 135 ммоль/л) в результате перехода большей части натрия в интерстициальную и асцитическую жидкость. Повышенная реабсорбция почками натрия и воды ведет к накоплению асцитической жидкости. Данная теория «недостаточного наполнения» центрального венозного и артериального сосудистого русла доказывает главное значение гемодинамических и гормональных сдвигов и вторичность реакции почек в отношении задержки натрия.
Однако за последние годы было установлено, что у 2/3 больных циррозом печени, не получавших лечения гипонатриевой диетой и мочегонными средствами (факторы, активирующие выработку альдостерона), стимуляция ренин-ангиотензин-альдостероновой системы отсутствует. Возможно, у таких больных имеется повышенная чувствительность почечных канальцев к альдостерону. Активность ренина плазмы почти всегда повышена у больных циррозом печени с асцитом и сопутствующей почечной недостаточностью при гепаторенальном синдроме, особенно при резкой гипонатрийурии (< 2 ммоль/сут.). Причиной этого является снижение почечного кровотока. Препараты, увеличивающие почечный кровоток (допамин и др.), снижают активность ренина. Эти данные способствовали обоснованию альтернативной теории формирования при циррозе печени асцита — теории «избыточного притока», согласно которой задержка натрия у 2/3 больных циррозом, является первичным феноменом, независимым от активации ренин-ангиотензин-альдостероновой системы и возникающим в результате уже увеличенного до появления асцита объема плазмы и крови. Предполагается, что причиной может быть и недостаток натрийурического гормона, вырабатываемого печенью и выявляемого в асцитической жидкости. Задержка натрия сопровождается нарастанием объема интерстициальной жидкости, что приводит к угнетению активности ренин-ангиотензин-альдостероновой системы. При наличии портальной гипертензии, снижении онкотического давления плазмы, нарушении дренажа лимфы в печени происходит скопление избытка внеклеточной жидкости в полости брюшины и в периферических межкапиллярных интерстициальных пространствах, и как результат возникают асцит и отеки.
Против теории «избыточного притока» существует ряд факторов, указывающих на недостаточное наполнение кровью центрального сосудистого русла у больных циррозом печени, несмотря на увеличение объема плазмы. Это низкое артериальное давление, выраженный натрийурический эффект при погружении на продолжительный период больного с асцитом в воду, что ведет к увеличению притока плазмы к почкам. Натрийурический и диуретический эффекты перитонеально-венозного шунта приводят к увеличению объема плазмы крови в результате перераспределения асцитической жидкости в сосудистое русло.
Эти данные послужили основанием оценить теорию «недостаточного наполнения» с современных позиций, согласно которой в начальной стадии имеет место задержка натрия почками и увеличение объема плазмы. Избыток жидкости в связи с портальной гипертензией и увеличением коллоидно-осмотического давления плазмы дренируется в полость брюшины, а затем в брюшную полость (свободная жидкость определяется при УЗИ, перкуссии в правом и левом фланке и пальпации методом баллотирования). Это приводит к снижению объема плазмы и последующему за этим повышению реабсорбции натрия и воды в почечных канальцах. Гиповолемия центрального сосудистого русла вызывает также стимуляцию со стороны внутригрудных объемных сосудистых рецепторов. Активация симпатической нервной системы на уровне почек приводит к почечной вазоконстрикции, снижению почечного кровотока и гломерулярной фильтрации, повышению проксимальной канальцевой реабсорбции натрия и к последующей за этим активации ренин-ангиотензин-альдостероновой системы с повышенной дистальной реабсорбцией натрия. Аналогичное описанному действие вызывает инфузия ангиотензина II или норадреналина. Согласно этой теории нарастание натрийуреза, калийуреза и экскреции воды с одновременным резким увеличением натрийурического эффекта антагониста альдостерона спиронолактона у больных, погруженных по шею в воду, обусловлено перераспределением жидкости из интерстиция в циркуляторный внутригрудной проток, что лежит в основе устранения центральной гиповолемии.
Выраженный натрийурический и диуретический эффекты антагонистов альдостерона (верошпирон, спиронолактон) у большинства больных циррозом печени в асцитической стадии, особенно на начальной его стадии и при отсутствии функциональной почечной недостаточности, показывает, что следует учитывать гормональные изменения в патогенезе формирования асцита. Вторичный, т.е. не связанный непосредственно с поражением надпочечников, гиперальдостеронизм при циррозе печени является таким же клинически установленным фактом, как и у больных застойной сердечно-сосудистой или почечной недостаточностью, пиелонефритом с потерей натрия или калия или при других нарушениях водно-солевого равновесия. Причиной гиперальдостеронизма при циррозе печени, как и при сердечно-сосудистой и почечной недостаточности, является снижение печеночного кровотока и уменьшение метаболического клиренса альдостерона и экскреции его с мочой.
Несмотря на то, что диагноз асцита не представляет трудностей, важно иметь в виду, что увеличение объема живота — обязательный, но наименее надежный симптом асцита. Увеличение живота наблюдается при метеоризме, у больных с общим ожирением или ожирением сальника, при атонии передней брюшной стенки, опухолях брюшной полости, больших кистах яичника, беременности. В начальных стадиях накопления асцитической жидкости важными симптомами являются отрицательный диурез, прибавка в массе тела, появление перемещающегося при перемене положения тела притупления перкуторного звука в левом и правом фланках подвздошных областей и в нижней половине живота. На обзорной рентгенограмме живота контуры органов брюшной полости нечеткие, определяется высокое стояние куполов диафрагмы. Массивный асцит вызывает расхождение прямых мышц живота, подъем диафрагмы с поворотом сердца и смещением верхушечного толчка влево, увеличение давления в правом желудочке сердца, сопровождающееся набуханием шейных вен.
При небольших асцитах больной отмечает чувство полноты в животе, периодическое вздутие, тесной становится одежда в талии. Перкуссия и пальпация при начальной стадии асцита часто неэффективна. Для диагностики ранних стадий асцита применяют УЗИ. Асцит средних и больших размеров, когда в брюшной полости содержится 3-6 л жидкости и более, определяется пальпаторно и перкуторно.
Асцит может осложняться гепаторенальным синдромом и спонтанным бактериальным перитонитом. Гепаторенальный синдром, скорее всего, является наиболее тяжелой формой декомпенсации системной гемодинамики. Теоретически он может быть обратимым в случае проведения трансплантации печени. Спонтанный бактериальный перитонит определяется как инфекция асцита без внутриабдоминального источника. Пупочная грыжа и плевральный выпот также могут быть осложнениями асцита.
Источник