Прогноз эффективности терапии хронического гепатита с
Лечение хронического гепатита С (ХГС) – одна из самых обсуждаемых тем в гастроэнтерологии и гепатологии. Связано это с высоким удельным весом ХГС в структуре хронических заболеваний печени как в нашей стране, так и за рубежом. В последние годы в лечении данной нозологии достигнуты немалые успехи. В статье обсуждаются результаты современной противовирусной терапии (ПВТ) у пациентов с ХГС, особое внимание уделяется препаратам с прямым антивирусным действием (ингибиторы протеаз и полимераз).
![Рис. 1. Заболеваемость хроническими вирусными гепатитами в РФ в 2002–2009 гг. (на 100 тыс. населения) [19]](https://umedp.ru/upload/resize_cache/iblock/cea/195_350_1/pegintron1.jpg)
Рис. 1. Заболеваемость хроническими вирусными гепатитами в РФ в 2002–2009 гг. (на 100 тыс. населения) [19]
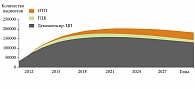
Рис. 2. Прогноз прогрессирования HCV-ассоциированных заболеваний печени в 2012–2027 гг. в США
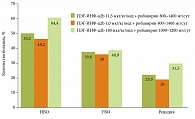
Рис. 3. Сравнительная эффективность ПЭГ-ИФН-α2а и ПЭГ-ИФН-α2b по результатам IDEAL (n = 3070)

Таблица 1. Принципы лабораторного мониторинга при проведении терапии ПЭГ-ИФН-α и рибавирином
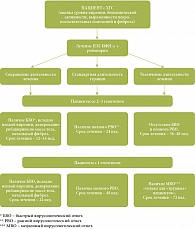
Рис. 4. Алгоритм выбора длительности терапии у пациентов с ХГС
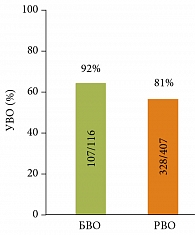
Рис. 5. Частота УВО при достижении БВО и РВО у пациентов с 1 генотипом HCV (n = 1019) при терапии ПЭГ-ИФН-α2b и рибавирином
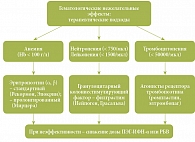
Рис. 6. Алгоритм коррекции гематологических нежелательных явлений

Таблица 2. Терапевтическая тактика при гематологических нежелательных эффектах
Эпидемиологические и фармакоэкономические аспекты лечения гепатита С По данным ВОЗ, в 2007 г. число носителей вируса гепатита С в мире составляло около 180 млн человек (то есть 3% населения планеты). При этом ежегодно регистрировалось 3–4 млн новых случаев гепатита С. Можно предположить, что рост заболеваемости будет сохраняться на том же уровне, в первую очередь из-за отсутствия профилактических вакцин против HCV-инфекции. В подтверждение сказанному, по данным Федерального центра гигиены и эпидемиологии Роспотребнадзора, в России за последние 10 лет наблюдается постоянная тенденция к повышению заболеваемости ХГС, уровень которой в 2009 г. составил почти 41 на 100 тыс. населения (рис. 1).
Кроме того, не вызывает сомнения факт, что ХГС является наиболее частой причиной развития цирроза печени (ЦП), печеночной недостаточности, гепатоцеллюлярной карциномы (ГЦК) и, как следствие, основным показанием к ортотопической трансплантации печени (ОТП) в развитых странах [1]. Следует также помнить, что в 65–85% случаев острая HCV-инфекция переходит в хроническую.
В связи с вышеизложенным важное значение имеет прогноз заболеваемости на ближайшие десятилетия. Специалисты подсчитали, как будет прогрессировать частота HCV-ассоциированных заболеваний в США в течение 20 лет, начиная с 2009 г. (рис. 2). Было показано, что число больных с «продвинутой» стадией заболевания (выраженный фиброз/цирроз печени) к 2029 г. увеличится в 4 раза. Прогнозируется, что еще больше увеличится частота ГЦК и число ОТП по поводу HCV-инфекции, примерно так же вырастут и затраты на медицинское обеспечение данной категории пациентов. По-видимому, следует ожидать похожей динамики HCV-ассоциированных заболеваний и в нашей стране.
В последние годы достаточно часто обсуждаются вопросы фармакоэкономики ПВТ, которые, на наш взгляд, связаны с достижением устойчивого вирусологического ответа (УВО).
На сегодняшний день имеются данные, что при наличии УВО вероятность авиремии в течение 5 лет превышает 99%, а достижение УВО может свидетельствовать о клиническом излечении больного ХГС [2].
С другой стороны, один из последних метаанализов, посвященных значению УВО, показал, что частота декомпенсации ЦП, развития ГЦК и смерти от заболеваний печени у больных ХГС с выраженным фиброзом в случаях терапевтической неудачи составляет около 2–3% в год, в то время как у пациентов, достигших УВО, относительный риск составил лишь 0,16–0,23% [3]. Приводятся также данные, что экономическая эффективность противовирусного лечения ХГC сопоставима с эффективностью таких широко проводимых лечебно-профилактических мероприятий, как лечение артериальной гипертонии, скрининг на рак молочной железы и колоректальный рак и т.д. (Wright J., Weinstein M., 1998).
Современные подходы к диагностике при ХГС
ХГС у большинства пациентов имеет мало- или бессимптомное течение, что требует точности при выполнении диагностических тестов у пациентов данной категории. Выполнение диагностического алгоритма необходимо не столько для установления полного диагноза с указанием стадии заболевания, уровня репликации, генотипа HCV, осложнений, сколько для представления так называемого портрета пациента, который позволяет правильно оценить показания и противопоказания для ПВТ, выявить благоприятные и неблагоприятные предикторы для достижения УВО, исключить или выявить сопутствующие заболевания, коррекция которых может потребоваться в процессе лечения, определить «базальный» уровень лабораторных показателей, мониторинг которых требуется при проведении ПВТ.
Необходимо, на наш взгляд, по-прежнему выделять группу пациентов, которые имеют один или несколько неблагоприятных предикторов (так называемая группа «трудных» пациентов), которые могут привести к неудачным результатам ПВТ.
В течение последнего года активно обсуждается возможность применения в качестве диагностических тестов различных генетических маркеров у пациентов c ХГС. К настоящему времени доказано, что интерлейкин-28В (IL-28B) может рассматриваться как один из самых «сильных» предикторов УВО. В частности, было показано, что генотип C/C является самым «сильным» предиктором УВО у нелеченых пациентов с 1 генотипом (OR = 5,2; 95-процентный ДИ 4,1–6,7; р
Современные подходы к ПВТ
Прежде всего, хотелось бы подчеркнуть, что современные подходы к ПВТ отнюдь не являются догмой, их можно рассматривать как точку отсчета на пороге новой эры прямых антивирусных агентов (в зарубежной литературе часто используется термин DAA – direct-antiviral agent).
Принципы терапии укладываются в понимание и знание ответов на представленные ниже вопросы:
- Каковы цели терапии?
- Кого лечить?
- Чем лечить?
- Как долго лечить?
- Каковы правила мониторинга?
Цели терапии. В настоящее время считается, что основная цель ПВТ – стойкое подавление репликации НСV и достижение УВО, который определяется как отсутствие вирусной РНК в сыворотке крови пациента через 24 недели после окончания противовирусного лечения. При этом доказано: УВО улучшает прогноз заболевания вплоть до полного пожизненного излечения (D.R. Nelson, G.L. Davis, I. Jacobson и соавт., 2009).
Основываясь на данных последних и наиболее представительных клинических исследований, можно утверждать, что в случаях гепатита, вызванного 2 и 3 генотипом вируса, при применении пегилированного интерферона-α (ПЭГ-ИФН-α) и рибавирина УВО составляет 67–82% [5–8]. При 1 генотипе эффективность лечения ниже: УВО составляет 39–44% [5, 8–11].
Кого лечить? Если в начале 2000-х гг. большинство экспертов, учитывая низкую эффективность ПВТ (5–15%), высказывались в пользу выжидательной тактики, то в настоящее время такой подход пересмотрен. Сейчас считается, что все пациенты должны рассматриваться как потенциальные кандидаты для ПВТ. Исключение могут составлять пациенты с неблагоприятным генотипом IL-28В (в первую очередь ТТ) при невозможности включения в схему ПВТ прямых антивирусных агентов.
К вопросу «Чем лечить?», несомненно, следует подходить с позиции доказательной медицины. Стандартом лечения во всем мире считается комбинация ПЭГ-ИФН-α и рибавирина. При выборе между ПЭГ-ИФН-α2а (Пегасис) и ПЭГ-ИФН-α2b (Пегинтрон) следует руководствоваться результатами самого доказательного на сегодняшний день клинического исследования в этой области IDEAL (международное мультицентровое проспективное сравнительное), в котором было показано отсутствие достоверной разницы в достижении УВО (рис. 3) при применении указанных лекарственных препаратов [12].
Важным является вопрос «Как долго лечить?». Стандартная длительность терапии составляет 48 недель при 1 и 4 генотипе HCV; при 2 и 3 генотипе – 24 недели. Однако в настоящее время считается, что длительность ПВТ зависит от вирусологического ответа (в зарубежной литературе используется термин response-guided strategy). Речь идет об индивидуализации подхода к лечению пациента на основе оценки динамики вирусной нагрузки. При этом обсуждается как возможность сокращения, так и пролонгирования (в ряде случаев) сроков ПВТ с позиции доказательной медицины [13]. Указанный подход или алгоритм выбора длительности терапии (рис. 4) должен включать ряд важнейших критериев: наличие быстрого вирусологического ответа (БВО), исходная виремия, отсутствие фиброза или его начальных проявлений, а также дозирование рибавирина в зависимости от массы тела.
Так, в случае 2–3 генотипа при наличии низкой исходной виремии (менее 400000 МЕ/мл) и БВО, при отсутствии выраженного фиброза/цирроза, а также при назначении рибавирина в зависимости от массы тела сроки ПВТ могут быть сокращены с 24 до 16 недель. У пациентов с 1 генотипом при наличии перечисленных условий длительность ПВТ может быть сокращена с 48 до 24 недель. С другой стороны, при наличии медленного вирусологического ответа у пациентов с 1 генотипом сроки терапии могут быть увеличены до 72 недель.
Следует иметь в виду, что уменьшение длительности ПВТ будет способствовать не только сокращению расходов на лечение, но и позволит избежать возможных нежелательных явлений (НЯ), а также обеспечит повышение приверженности пациентов к терапии.
Принципы и правила мониторинга. Как известно, мониторинг при проведении любого вида лечения включает 3 основных направления: эффективность, безопасность и приверженность.
Основная задача – наиболее ранняя оценка эффективности терапии, что достигается с помощью оценки динамики вирусной нагрузки. К настоящему времени получены убедительные данные, что БВО (то есть отрицательная HCV РНК после 4 недель терапии) является самым сильным предиктором УВО. Вместе с тем достаточно важным предиктором остается полный ранний вирусологический ответ (рис. 5) [14].
Другая задача мониторинга – безопасность лечения. При этом важно уметь не только диагностировать, но и эффективно проводить коррекцию возможных НЯ. Особенно важными среди таковых считаются гематологические НЯ.
Достижением современного этапа является доказательство того, что не существует корреляции между частотой инфекционных осложнений и нейтропенией [16, 17], частотой кровотечений и снижением тромбоцитов [18] при проведении ПВТ, что позволяет пересмотреть существующие рекомендации по модификации дозы противовирусных препаратов.
Терапевтические подходы, рекомендованные фирмами-производителями в зависимости от степени снижения гематологических показателей, представлены в таблице 3.
Однако большинство исследователей сходятся во мнении, что критерии анемии, лейкопении, нейтропении, тромбоцитопении, рекомендуемые сегодня для модификации дозы и отмены ПВТ, индивидуальны. При этом большое значение приобретают подходы, связанные не с модификацией дозы, а с использованием препаратов, стимулирующих различные звенья гемопоэза (рис. 6). Так, при развитии анемии ниже 100 г/л рекомендуется подкожное введение эритропоэтина-α (или -β) (Эпокрин, Рекормон) в дозах 8–40 тыс. ЕД/нед (2–3 раза в неделю). При развитии нейтропении (
Применение препаратов, стимулирующих гемопоэз, обусловлено, в первую очередь, необходимостью выполнять правило «80 + 80 + 80»: кумулятивная доза ИФН и рибавирина, полученная пациентом, должна составлять не менее 80% от назначенных доз, общая длительность лечения – не менее 80% от необходимой продолжительности терапии.
В то же время, несмотря на несомненные успехи ПВТ, у части пациентов с ХГС терапия оказывается неэффективной (так называемые нон-респондеры). По прогнозам ведущих экспертов, число нон-респондеров к концу 2011 г. достигнет в мире более 500 тыс. человек. В связи с этим особенно важно появление в клинической практике первых ингибиторов протеазы NS3/4A (Боцепревир, Телапревир), которые показаны в первую очередь для указанной категории пациентов и будут применяться в качестве третьего компонента в известной стандартной схеме (ПЭГ-ИНФ-α + рибавирин). К сожалению, в клинических исследованиях тройная терапия показала большее количество нежелательных явлений, в том числе таких, как анемия, сыпь, извращение вкуса и другие, которые, по-видимому, будут являться лимитирующим фактором для полноценной ПВТ.
Достижением последних лет явились итоги клинического исследования HALT-C (Hepatitis C Antiviral Long-term Treatment against Cirrhosis) по изучению эффективности длительной поддерживающей терапии у пациентов с циррозом печени (ЦП) в исходе ХГС. Результаты исследования показали, что длительная терапия поддерживающими дозами ПЭГ-ИНФ-α у пациентов ЦП не приводит к каким-либо достоверным положительным эффектам по сравнению с группой без лечения по таким критериям, как выживаемость, прогрессирование фиброза, частота декомпенсаций и частота развития ГЦК [15], что вызывает необходимость применения более агрессивной тактики лечения уже на стадии начального и тем более продвинутого фиброза. С другой стороны, ПВТ у больных c ЦП может рассматриваться «запоздалым» мероприятием, учитывая еще и полиморбидность указанной категории пациентов, потенциально низкую частоту УВО, повышенную частоту развития у них нежелательных явлений.
Заключение
Лечение ХГС остается серьезной медико-социальной проблемой. Современные подходы к противовирусному лечению при ХГС во многих случаях требуют от специалистов не только понимания закономерностей инфекционного процесса, но и информированности в области достижений современной медицинской науки и фармацевтики с позиций доказательной медицины. За последние годы произошла ревизия взглядов на показания, противопоказания, фармакоэкономические показатели противовирусной терапии. Ожидаемый эффект от лечения включает эрадикацию вируса, улучшение морфологии печени, снижение инфицированности населения и уменьшение риска развития гепатоцеллюлярного рака.
Современные подходы к противовирусной терапии пациентов c ХГС включают:
- оценку благоприятных и неблагоприятных предикторов эффективности ПВТ;
- выбор антивирусных агентов;
- мониторинг эффективности (на основании динамики вирусной нагрузки или response-guided strategy) и безопасности (диагностика и коррекция нежелательных явлений).
Указанные положения особенно актуальны при применении новых антивирусных препаратов. Появление в клинической практике ингибиторов протеазы открывает новые перспективы повышения эффективности ПВТ. В то же время существует риск увеличения частоты различных нежелательных явлений, а также развития резистентности к новым антивирусным агентам, что потребует от специалистов, занимающихся лечением ХГС, еще больших знаний и опыта.
Источник
Воспалительные поражения печени несут серьезную угрозу здоровья. Одним из самых распространенных заболеваний является хронический гепатит C. Это вирусное поражение, провоцирующие воспаление тканей с последующим отмиранием гепатоцитов. Отсутствие своевременной терапии приводит к развитию тяжелых осложнений.
Возбудитель гепатита C
Рассматривая симптомы и лечение хронического гепатита C, необходимо определить возбудитель патологии. Болезнь имеет инфекционное происхождение. Провоцируется вирусными микроорганизмами, поражающими печеночные клетки.
Особенностью вируса является длительный срок жизни – 10-20 лет. Инфекция устойчива к неблагоприятным внешним факторам, ультрафиолетовому излучению, обеззараживающим веществам, стойко переносит перепады температуры.
После заражения организма, вирус длительное время сохраняет латентность. При этом инфицированный человек является потенциальным переносчиком патогена. До наступления острой фазы выявить болезнь можно только при помощи лабораторного исследования крови.
Причины заболевания
Патология провоцируется проникновением возбудителя в кровь человека. Заражение происходит разными способами. Развитию болезни сопутствует ряд факторов.
К ним относятся:
- Повышенная чувствительность организма к инфекциям
- Наличие ВИЧ-инфекции
- Злоупотребление алкоголем
- Несоблюдение гигиенических норм
- Контакты с инфицированными
- Сопутствующие патологии печени
- Токсическое воздействие на гепатобилиарный тракт
- Паразитарные инвазии
- Неправильное питание
Заболевание провоцируется вирусной инфекцией, однако риск заражения повышается при влиянии сопутствующих факторов.
В каких случаях болезнь переходит в хроническую форму?
Патология протекает в несколько стадий. Болезнь характеризуется длительным, вялым течением с низкой интенсивностью симптомов. Часто поражение печени долгое время остается необнаруженным, что повышает риск осложнений. Длительный инкубационный период, латентное течение, обострения хронического гепатита характерны для большинства генотипов.
Начальный этап – развитие острой формы. Данный период не сопровождается интенсивной симптоматикой. Состояние пациентов удовлетворительное, ввиду чего заподозрить присутствие патологии сложно.
В дальнейшем развивается фаза реактивации. Данный период характеризуется постепенным переходом острой стадии в затяжную с последующим развитием хронического гепатита C.
Основная причина перехода – отсутствие своевременной терапии. При правильном лечении, железа постепенно восстанавливается. Нормализуются главные функции, свойства органа.
Если терапии нет, клетки печени постепенно отмирают, развивается фиброз. Очаги некроза замещаются рубцовой тканью. Увеличивается вирусная нагрузка, что означает рост числа пораженных клеток. Частота трансформации составляет 75%-80%.
Как передается хронический гепатит C?
Инфекция, вызывающая болезнь, отличается высокой распространенностью. Главный механизм передачи – парентеральный. Источник инфекции – кровь зараженного человека. Реже вирус содержат другие биологические жидкости (кал, семенная жидкость, моча, слюна, секрет слизистых оболочек).
Наиболее распространенные источники заражения:
- Незащищенный половой контакт с инфицированным человеком (в том числе гомосексуальные)
- Нарушение гигиенических норм
- Несоблюдение стандартов стерильности при проведение хирургических операций
- Косметологические процедуры с использованием нестерильных инструментов
- Многократное использование одноразовых шприцев
- Переливание зараженной донорской крови
- Антисанитарные условия жизни
- Применение индивидуальных вещей, предметов гигиены, одежды, столовых приборов инфицированного
- Внутриутробное заражение
- Инфицирование при прохождении ребенком родовых путей
Считается, что вирус неспособен передаваться бытовыми путями, через попадание слюнной жидкостей, других биологических веществ. Однако известны случаи такой передачи инфекции, что указывает на потенциальный риск для каждого человека.
Группы повышенного риска:
- Инъекционные наркоманы
- Население регионов с повышенной эпидемиологической ситуацией
- Мужчины, поддерживающие гомосексуальные половые связи
- Лица, пребывающие в местах лишения свободы
- Персонал медицинских учреждений, фармацевтических производств, лабораторий
- Сотрудники сферы ЖКХ
- Люди, члены семьи которых заражены
Заболевание передается многочисленными способами, что объясняет высокую распространенность.
Симптомы хронического гепатита C
Клиническая картина провоцируется фиброзными изменениями органа, разрушением функциональных клеток. Симптомы хронического гепатита с минимальной степенью активности, во многом похожи на острую форму. Патология протекает вяло, выраженные признаки поражения печени отсутствуют. Интенсивная симптоматика развивается при последующих обострениях, сопутствующих осложнениях.
Признаки:
- Тошнота
- Рвота
- Метеоризм
- Отрыжка
- Горький привкус во рту
- Желтушность кожи
- Гепатомегалия
- Отсутствие аппетита
На фоне интоксикации возникают болевые синдромы. Поражаются суставные, мышечные ткани. Отмечаются выраженные головные боли, спазмы брюшной области с правой стороны. При ощупывании наблюдается увеличение, уплотнение печени. Помимо желтухи присутствуют другие кожные проявления: высыпания, зуд.
Общее состояние пациента ухудшается. Снижается работоспособность, повышается утомляемость, слабость. Больной испытывает сонливость, головокружение. Тяжелое течение хронической формы сопровождается расстройствами нервной системы, судорогами, обмороками, мигренями.
Диагностика
При возникновении симптомов поражения печени требуется комплексное обследование. Начальный этап диагностики подразумевает сбор жалоб пациента, изучение анамнеза, пальпацию, внешний осмотр. Полученные сведения позволяют предположить о наличии болезни. Дальнейшие процедуры направлена на подтверждение диагноза, определение генотипа, выбор методов лечения хронического вирусного гепатита.
Методы диагностики:
- Анализы крови (общий, иммуноферментный, биохимический)
- Полимеразная цепная реакция
- Иммуноглобулиновый тест
- УЗИ печени
- Пункционная биопсия
- МРТ
- Коагулограмма
Пациентам, у которых диагностирована хроническая форма гепатита, должны регулярно проходить повторное обследование для изучения динамики развития процесса, определения эффективности терапии.
Лечение хронического гепатита C
Терапия назначается с учетом стадии, степени тяжести болезни, индивидуальных особенностей больного, наличия осложнений, противопоказаний. Основным способом является медикаментозная терапия в сочетании с диетой. При активном фиброзе лечение хронического гепатита c проводится хирургическими методами.
Медикаментозная терапия
Патология успешно лечится при помощи противовирусных медикаментов. В терапевтических целях применяют сильнодействующим препараты, направленные на подавление ретровирусной инфекции. Подобные медикаменты применяют при гепатитах и ВИЧ.
Хроническую форму лечат при помощи препаратов, содержащих Интерферон и Рибавирин. Они обладает выраженной противовирусной активностью, взаимно дополняют эффект друг друга.
Инновационным методом терапии считается прием препаратов прямого действия. К ним относятся ингибиторы протеаз и аналоги нуклеозидов.
Применяемые препараты:
- Софосбувир
- Даклатасвир
- Ледипасвир
- Симепревир
- Даклинза
- Телапревир
Курс терапии зависит от генотипа вируса. Минимальный срок лечения составляет 12 недель. Максимальный достигает 36 и более.
После противовирусной терапии назначают вспомогательные медикаментозные средства:
- Диуретики
- Желчегонные препараты
- Сорбенты
- Гепатопротекторы
- Витаминные комплексы
Медикаментозное лечение хронического вирусного гепатита производится при условии отсутствия противопоказаний.
Диета
Пациентам с поражениями печени назначается лечебная диета. Главная задача – снижение нагрузки на печень, органы пищеварение, одновременное обеспечение организма питательными веществами.
Принципы питания:
- Дробный режим
- Отказ от жирного (копчености, колбасные изделия, жареное, консервы)
- Снижение потребления соли, острых специй
- Исключение жирной молочной продукции, кондитерских изделий, мучного
- Обогащение рациона сложными углеводами, белками
- Обильный питьевой режим
- Исключение алкоголя
Калорийность рациона подбирается таким образом, чтобы пациенты с лишним весом, худели на 600-800 г еженедельно. Средний суточный объем калорий – 2000-2500 ккал.
Народные средства
Подвергается ли хронический гепатит c лечению при помощи нетрадиционных методов – вопрос, интересующий каждого, кто столкнулся с заболеванием. Избавиться от инфекции, вызывающей патологию при помощи народных средств нельзя. Однако нетрадиционная медицина предлагает большое количество рецептов, помогающих восстанавливать функции пораженного органа, способствующих регенерации тканей, ускоряющих выздоровление.
Популярные рецепты:
- Травяной настой. Необходимо смешать в равных пропорциях пижму, шалфей, тысячелистник, репешок, листья лопуха. Сбор дополняют плодами шиповника, цветками зверобоя, ромашки. 4 ложка сбора заливают 1 л кипятка, оставляют настаиваться 3 часа. Лекарство принимают трижды в сутки по 0.5 стакана.
- Мумие. 3 г растворяют 3 л кипяченной прохладной воды. Жидкость принимают утром, вечером по 1 стакану. Длительность курса терапии – 10 дней.
- Шрот расторопши. Семена растения измельчают кофемолкой. Полученный порошок принимают утром, перед завтраком, запивая водой по 1 ложке.
- Отвар семян. Измельченные семена расторопши (3 ложки) заливают 0.5 л кипятка, держат на паровой бане пока не выкипит половина жидкости. Готовое лекарство процедить, пить за несколько приемов.
- Кукурузные рыльца. Столовая ложка рылец заливается стаканом кипятка. Лекарство настаивают 2 часа. Принимают средство по 3 больших ложки перед едой.
Лечение воспалительных поражений печени – комплексный процесс, предполагающий применение медикаментозных средств, народных лекарств, соблюдение диеты.
Профилактика и прогноз
Спрогнозировать течение болезни трудно. Терапевтический процесс осложняется различными факторами.
К ним относятся:
- Вредные привычки
- Несоблюдение гигиены
- Нарушение врачебных предписаний
- Неправильный прием медикаментов
- Избыточный вес
- Нарушение режима питания
- Присоединение сопутствующих заболеваний
При отсутствии лечения, либо если оно проводится неправильно, возрастает риск осложнений. Потенциально опасны для жизни цирроз печени, гепатоцеллюлярная карцинома, внутренние кровотечения, брюшная водянка – наиболее распространенные последствия гепатита C.
Соблюдение профилактических мероприятий уменьшает вероятность летального исхода. Соблюдать профилактику рекомендуют с целью предотвращения заражения, развития осложнений у больных, для понижения уровня распространенности патологии.
Меры профилактики:
- Соблюдение стерильности при медицинских, косметологических манипуляциях
- Защищенная половая жизнь
- Отказ от вредных привычек
- Укрепление иммунитета
- Вакцинация против других вирусных заболеваний
- Правильное питание
- Исключение контактов с инфицированными
Предотвратить заражение со стопроцентной вероятность нельзя. Но соблюдение профилактики существенно снижает возможность занесения инфекции с последующими осложнениями.
Можно ли полностью вылечить хронический гепатит C?
Вопрос о том, лечится ли описанное заболевание, интересует многих пациентов. Современные методы противовирусной терапии позволяют подавить инфекцию. При соблюдении рекомендаций врача, грамотной профилактике, печень восстанавливается за 2-3 года. Для выздоровления важно начать терапию как можно раньше, пока не возник фиброз, другие патологические изменения органа.
Гепатит C относится к числу распространенных хронических заболеваний. Несвоевременная диагностика, лечение приводят к развитию осложнений, провоцирующих летальные последствия. При помощи инновационных противовирусных медикаментов можно полностью вылечить патологию, исключив угрозу для жизни.
Источник


