Тройная пвт при гепатите с
Телапревир (Иинсиво, Incivek) и Боцепревир (Виктрелис, Victrelis) – новые возможности противовирусного лечения
Стандартная противовирусная терапия препаратами интерферона и
рибавирина за последние годы спасла жизнь огромному количеству
пациентов с вирусным гепатитом С. Эффективность препаратов используемых при стандартном лечении позволила объявить вирусный гепатит излечимым заболеванием.
Однако, далеко не все пациенты могут получить полное выздоровление.
Результат зависит от давности заболевания, степени поражения печени на
момент обращения к врачу-гепатологу, пола, возраста, генотипа интерлейкина 28В, генотипа вируса.
Наиболее проблемными группами для лечения являются пациенты с
генотипом вируса 1, с циррозом печени, а также пациенты, не ответившие
на терапию или после успешного лечения получившие рецидив.
Именно для таких пациентов продолжается поиск новых препаратов, дающих и этим категориям больных надежду на выздоровление.
Как результат огромной научной работы в течение 20 лет, на
фармацевтическом рынке появились новые препараты прямого
противовирусного действия, ингибиторы протеаз — Телапревир (ИНСИВО) И Виктрелис (БОЦЕПРЕВИР). Они разрешены в 76 странах мира, во многих странах включены в программу госзакупок.
Оба препарата зарегистрированы в России и их можно приобрести в специализированных аптеках.
В условиях клинических испытаний при рандомизированном отборе пациентов
по полу и возрасту и с определёнными критериями включения и исключения
из испытания получены многообещающие данные. В особенности это важно
для достаточно тяжелых случаев уже сформированного цирроза, а также для
пациентов, ранее не ответивших на стандартную терапию препаратами
интерферона и рибавирина.
Исследования показали, что важным предиктором ответа на ПВТ
является интерлейкин 28В. Генотип СС характеризуется более высокой
частотой достижения УВО, чем СТ или тем более ТТ у ранее нелеченых
пациентов с ХГС и генотипом 1. Лечение Телапревиром (ТП) позволило констатировать практически одинаково высокую частоту ответа
на лечение независимо от варианта полиморфизма IL28В как у ранее не
получавших терапию, так и с неэффективной терапией. Таким образом, Телапревир позволяет преодолеть генетический барьер, мешающий достижению эффекта у пациентов со стандартной ПВТ.
В 5 клинических исследованиях препарата Телапревир
получена авиремии на 4-й недели терапии, что является сильнейшим
предиктором достижения УВО (устойчивого вирусологического ответа) при
всех схемах применения телапревира. При этом 57 % пациентов из них
никак не реагировали на предшествующую терапию («неответчики), у 36 %
был рецидив, у 7 % — вирусологический прорыв. Частота рецидивов была на
20 % ниже у пациентов, получавших телапревир. Отмечено, что в зависимости от ответа к 12-й неделе ПВТ можно сократить до 24 недель при сохранении одинаково высоких шансов на получение УВО. У пациентов с циррозом печени, ранее не получавших ПВТ, частота УВО составила 62-92 %.
Основными побочными эффектами лечения ТП были
диарея, тошнота, слабость, сухость кожи. Появление сыпи отмечено в
46-63 %. Частота отмены лечения из-за этих побочных действий составила
3-11 %.
Использование ТП и иных ингибиторов
протеаз может вызвать мутацию HCV с формированием резистентности к
препарату. В таких случаях следует прекратить терапию и через несколько
недель после отмены возможно проведение повторного лечения.
Генетический анализ выявил возможность перекрестной резистентности,
изменяющей чувствительность как к ТП, так и к боцепревиру.
Телапревир – оральный препарат,
назначается пациентам с 1-м генотипом HCV по 750 мг три раза в день во
время еды с достаточным количеством жира. Для впервые леченых пациентов
и пациентов с предшествующим рецидивом болезни продолжительность приема ТП составляет 12 недель
при условии, что уровень HCV-РНК становится неопределяемым с 4-ой
недели и сохраняется таким до 12 недели. В таких случаях
продолжительность терапии будет составлять еще 12 недель интерфероном и
рибавирином. Общая продолжительность лечения – 24 недели.
Для пациентов с предшествующим частичным ответом или «неответчиков» продолжительность последующей после ТП терапии составляет 36 недель (интерферон и рибавирин). Общая продолжительность терапии – 48 недель.
У пациентов с циррозом печени независимо от результата предшествующей терапии продолжительность ПВТ после терапии ТП должна составлять 36 недель. Препарат не рекомендован с циррозом печени класса В и С по Child-Pough.
Клинические испытания Виктрелиса, в
том числе в России, показали увеличение эффективности (получения УВО) в
1.7 раз у пациентов, не получавших ранее терапию стандартными
препаратами (двойная терапия — ДТ), и в 3 раза у «не ответчиков».
В реальной практике вне испытаний, ожидаемые результаты увеличения эффективности лечения у всех групп составляет около 40-50 %, а при циррозе и фиброзе F3 – 55 %.
Рекомендована доза препарата 800 мг , принимается перорально 3
раза в день с едой. Прием препарата без еды может сопровождаться
снижением его эффективности вследствие недостаточной его концентрации в
крови.
Длительность терапии препаратом Виктрелис определяется
в зависимости от вирусологического ответа через 8, 12 и 24 недели.
Для всех пациентов с циррозом печени и пациентов с нулевым ответом на
предшествующую терапию рекомендована длительность терапии 48 недель, из
них первые 4 недели препаратами пегилированых интерферонов и
рибавирина (двойная терапия) с последующей тройной терапией 44 недели в
комбинации с Виктреликс.
Длительность тройной терапии у не леченых пациентов без цирроза
после первых 4 недель двойной терапии в случае раннего ответа должна
составлять не менее 24 недель.
В случае позднего ответа общая длительность терапии составляет 48
недель: после первых 4 недель двойной терапии, тройная терапия до 28
недель и затем продолжается двойная терапия с 28 по 48 неделю.
Тройная терапия должна быть прекращена, если содержание вируса в
крови через 12 недель лечения составит >100 МЕ/мл, а также, если
через 24 недели есть определяемый уровень HCV-РНК в крови.
Побочные действия препарата Виктрелис
изучены в клиническом исследовании с участием 1500 пациентов.
Наиболее распространенными нежелательными реакциями были анемия,
бронхит, поражение щитовидной железы (гипотериоз). Кроме того,
наблюдали нарушение липидного обмена, расстройства сна, внимания,
памяти. Реже были выражены кашель, отдышка, стоматит, мышечные спазмы,
боли в костях, снижение массы тела.
Индивидуальная реакция пациента на тройную терапию может различаться.
Исходя из экономических реалий, Тройную
терапию следует назначать в первую очередь пациентам с рецидивом после
предшествующей терапии или пациентам с компенсированным циррозом, не
получавшим ранее лечения.
ТЕЛАПРЕВИР И ВИКТРЕЛИС – первые
зарегистрированные препараты прямого противовирусного действия. Нам
только предстоит на собственном опыте с пациентами из реальной жизни, а
не специально подобранными для клинических испытаний, всесторонне
изучить их клиническую эффективность, оценить частоту развития побочных
эффектов, выработать тактику их коррекции.
Много лет назад такие же проблемы стояли
перед нами, когда мы начинали лечение пегилированными препаратами
интерферона и рибавирином. Теперь понятно, что побочные действия не
являются критичными и ими можно управлять.
Появление таких препаратов, как ТЕЛАПРЕВИР И
ВИКТРЕЛИС, может существенно изменить ситуацию с противовирусным
лечения, значительно сократив сроки лечения и повысив его
эффективность. Значительно большее число пациентов сможет надеяться на
полное выздоровление
Обследование для назначения лечения гепатита С
- Полное обследование вируса гепатита С (генотип и вирусная нагрузка);
- Анализы на вирус гепатита В для того, чтобы сделать прививку, если позволят результаты анализов;
- Полное обследование печени: биохимические
анализы, отражающие структурное и функциональное состояние печеночных
клеток, УЗИ брюшной полости с допплерографией, оценка степени фиброза
(Эластометрия, ФиброМакс, фибротест); - Анализы для исключение противопоказаний для
назначения терапии: клинический анализ крови, гормоны и УЗИ щитовидной
железы, аутоиммунные антитела; - Для пациентов старше 40 лет назначается обследование сердца, сосудов и дыхательной системы.
Обследование проводится в день обращения и занимает около 2-х часов. Ориентировочнпя стоимость обследования 25000 руб
(может изменяться при наличии у Вас уже сделанных анализов либо при
необходимости других анализов дополнительно к стандартному
обследованию).
Запишитесь на бесплатную консультацию для назначения обследования.
Источник
У российских пациентов, инфицированных 1 генотипом вируса гепатита С, появилась возможность применять препараты прямого противовирусного действия – ингибиторы протеазы – телапревир и боцепревир. В России телапревир зарегистрирован в декабре 2012 г., боцепревир – в мае 2013 г. Как показали результаты многочисленных рандомизированных клинических исследований, в случае применения тройной терапии повышается эффективность лечения и сокращаются сроки противовирусной терапии.

Таблица 1. Эффективность боцепревира и телапревира у пациентов, ранее не получавших лечения

Таблица 2. Эффективность боцепревира и телапревира в зависимости от полиморфизма гена IL28B у ранее не получавших лечения пациентов европеоидной расы (по результатам исследования ADVANCE)
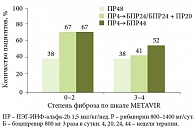
Рис. 1. Частота устойчивого вирусологического ответа в зависимости от степени фиброза (по результатам исследования SPRINT-2)
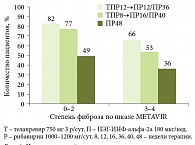
Рис. 2. Частота устойчивого вирусологического ответа в зависимости от степени фиброза (по результатам исследования ADVANCE)
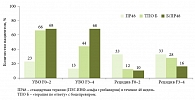
Риc. 3. Частота устойчивого вирусологического ответа и рецидива в зависимости от степени фиброза (по результатам исследования RESPOND-2)
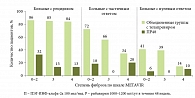
Рис. 4. Эффективность терапии в зависимости от степени фиброза (по результатам исследования REALIZE)
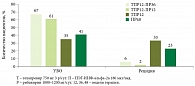
Рис. 5. Частота устойчивого вирусологического ответа и рецидива (по результатам исследования PROVE-1)
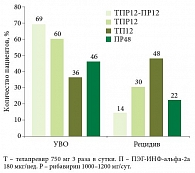
Рис. 6. Частота устойчивого вирусологического ответа и рецидива (по результатам исследования PROVE-2)
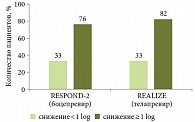
Рис. 7. Снижение HCV РНК после вводной фазы (4-я неделя терапии)
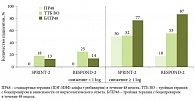
Рис. 8. Частота устойчивого вирусологического ответа после вводного периода у пациентов с 3–4-й степенью фиброза по шкале METAVIR (по результатам клинических исследований SPRINT-2 и RESPOND-2)

Таблица 3. Длительность противовирусной терапии с применением боцепревира в зависимости от категории пациентов

Таблица 4. Длительность противовирусной терапии с применением телапревира в зависимости от категории пациентов

Таблица 5. Алгоритм преждевременного прекращения терапии
Еще 10 лет назад хронический гепатит C считался заболеванием, трудно поддающимся лечению. Благодаря внедрению новых схем терапии частота устойчивого вирусологического ответа (УВО) значительно возросла. В частности, особую роль сыграл переход от монотерапии интерфероном-альфа к комбинированной терапии пегилированным интерфероном-альфа (ПЭГ-ИНФ-альфа) и рибавирином. Комбинация ПЭГ-ИНФ-альфа и рибавирина является стандартом противовирусной терапии (ПВТ) у пациентов с хроническим гепатитом C. Длительность терапии – 16–48 недель в зависимости от генотипа вируса. Эффективность в виде достижения УВО составляет в среднем 42–52% у пациентов с 1 генотипом вируса гепатита С (HCV) и 76–82% – у пациентов с 2 и 3 генотипами [1, 2]. К недостаткам ПВТ можно отнести недостаточную эффективность, особенно у пациентов с 1 генотипом, и длительный курс лечения (при 1 генотипе – 24–48 недель, при 2 и 3 генотипах – 16–24 недели).
В 2011 г. Агентство по контролю пищевых продуктов и лекарственных препаратов США (United States Food and Drug Administration, FDA) и Европейское агентство лекарственных средств (European Medicines Agency, EMA) одобрили для клинического применения препараты прямого противовирусного действия – ингибиторы протеазы HCV – телапревир и боцепревир – для лечения хронического гепатита C у больных, инфицированных 1 генотипом HCV. Результаты рандомизированных клинических исследований (РКИ) показали, что у таких пациентов тройная терапия достоверно более эффективна по сравнению со стандартной ПВТ. Кроме того, тройная терапия – единственная альтернатива для пациентов с неэффективной предшествующей ПВТ.
Тройная терапия сложна как для пациента, так и для лечащего врача. От стандартной ПВТ тройную терапию отличают повышение эффективности лечения, сокращение сроков ПВТ, набор благоприятных предикторов УВО (до сегодняшнего дня продолжает уточняться), строгие правила отмены, при нарушении которых возникает риск развития резистентности к ингибиторам протеазы, риск лекарственных взаимодействий, дополнительные нежелательные явления.
Главное преимущество тройной терапии – повышение эффективности и сокращение сроков ПВТ при использовании принципа «терапия по ответу». Результаты множества опубликованных РКИ демонстрируют увеличение частоты УВО в группах пациентов, не получавших ранее лечения. Кроме того, частота УВО возрастала при неэффективности предшествующей терапии [2–5]. Основываясь на результатах РКИ II и III фазы применения боцепревира или телапревира в схемах тройной терапии, можно судить о достоверном повышении УВО как минимум на 20–25% (табл. 1).
В ряде исследований выявлена зависимость УВО от полиморфизма гена IL28В и обозначен круг пациентов с заведомо низкой вероятностью достижения УВО. Так, среди представителей европеоидной расы частота УВО составила 69, 33 и 27% в группах генотипов СС, СТ, ТТ соответственно, среди пациентов негроидной расы – 48, 15 и 13%. При анализе показателей пациентов, не получавших ранее лечения, выявлено существенное увеличение частоты УВО при тройной терапии в группах «неблагоприятного» варианта полиморфизма гена IL28В. В исследовании III фазы SPRINT-2 частота достижения УВО составила 80, 71 и 59% в группах генотипов СС, СТ и ТТ, по результатам исследования ADVANCE – 90, 71 и 73% у пациентов с генотипами СС, СТ, ТТ соответственно. Эти данные позволяют рекомендовать тройную терапию пациентам, ранее не получавшим лечения, в зависимости от наличия «неблагоприятного» варианта полиморфизма гена IL28В (табл. 2).
Данные исследований ADVANCE и SPRINT-2 демонстрируют снижение эффективности стандартной терапии по мере прогрессирования фиброза. Так, согласно результатам SPRINT-2, частота достижения УВО при стандартной терапии составила 38% [6], по данным ADVANCE – 49% при 0–2-й степени фиброза и 36% – при 3-й и 4-й степени. В то же время эффективность тройной терапии была существенно выше: у пациентов с выраженным фиброзом частота УВО при использовании боцепревира достигла 52% (рис. 1), телапревира – 66% (рис. 2). Несмотря на различия в схемах применения, группы тройной терапии сопоставимы по эффективности. Частота достижения УВО достоверно выше по сравнению с контрольной группой пациентов, получавших только ПЭГ-ИНФ-альфа и рибавирин.
Такая же закономерность прослеживается в группах с выраженным фиброзом у пациентов с неэффективной предшествующей ПВТ (нон-респондеры). Для обсуждения результатов исследований II и III фазы с применением препаратов боцепревир и телапревир нон-респондеров целесообразно разделить на три группы:
- первая – рецидив: неопределяемая HCV PHK по окончании стандартной терапии, но обнаружение HCV PHK в период наблюдения;
- вторая – частичный вирусологический ответ: при снижении виремии на 2 log10 и более в течение 12 недель терапии, но при этом неопределяемый уровень HCV PHK не достигнут;
- третья – нулевой ответ: при снижении HCV PHK менее 2 log10 к 12-й неделе терапии.
В исследовании RESPOND-2 (рис. 3) продемонстрировано влияние исходной стадии фиброза на достижение УВО при двойной терапии. В группе сравнения (при двойной терапии) частота достижения УВО составила 13–23% в зависимости от варианта вирусологического ответа, при тройной терапии – 68% [7].
При анализе результатов исследования REALIZE (телапревир применяли в комбинации с ПЭГ-ИНФ-альфа и рибавирином) выявлена та же закономерность. Эффективность тройной терапии у больных с рецидивом при фиброзе 0–2-й, 3-й и 4-й степени составила 86, 85 и 84% соответственно. Меньшая эффективность отмечена в группах больных с частичным и нулевым ответом. Кроме того, при сравнении эффективности стандартной и тройной терапии установлена достоверная разница в частоте УВО у больных с частичным и нулевым ответом (рис. 4).
Важным теоретическим и практическим достижением стандартной терапии является обоснование принципа «терапии по ответу», что позволяет оптимизировать курс лечения, делая его более персонализированным и экономически выгодным. В РКИ II и III фазы тройной терапии также доказана возможность применения принципа «терапия по ответу», в результате чего у пациентов без цирроза печени появилась возможность не только увеличить частоту УВО, но и сократить курс лечения [8], что кроме всего прочего означает снижение и медикаментозной, и финансовой нагрузки на пациента.
В исследованиях PROVE-1
и PROVE-2 с применением телапревира продемонстрированы результаты в отношении достижения УВО в группах сокращенного курса на основе «терапии по ответу». Частота УВО в исследовании PROVE-1 достигла 67% в группе ПВТ в течение 48 недель и 61% в группе «терапии по ответу» в течение 24 недель (рис. 5). В исследовании PROVE-2 частота УВО составила 69 и 60% соответственно (рис. 6).
В исследовании III фазы SPRINT-2 показано, что эффективность «терапии по ответу» с боцепревиром при возможности сокращения курса лечения не уступала эффективности полного курса ПВТ. Результаты РКИ III фазы демонстрируют более высокую частоту УВО по сравнению со II фазой. Скорее всего это объясняется эффективной коррекцией нежелательных явлений [9, 10, 11].
Результаты РКИ позволили составить четкие алгоритмы ведения пациентов при тройной терапии в зависимости от категории больных, наличия цирроза, вирусологического ответа.
Для терапии боцепревиром обязательным условием является наличие вводной фазы (вводного периода). В связи с этим важно отметить несколько моментов.
Основная задача вводного периода – наметить группу пациентов, у которых стандартная ПВТ прогностически малоэффективна и которым требуется тройная терапия. Это позволит избежать необоснованных затрат на лечение и необязательной медикаментозной нагрузки в случае продолжения двойной терапии. Таким образом, можно говорить об использовании динамики снижения уровня HCV PHK после вводной фазы в качестве критерия прогнозирования достижения УВО и для решения вопроса о тактике дальнейшего лечения (рис. 7 и 8).
При изменении вирусной нагрузки менее чем на 2 log10 (а тем более – менее чем на 1 log10) можно говорить о низкой чувствительности пациента к ПЭГ-ИНФ-альфа, что дает основания для продолжения ПВТ только в виде тройной терапии.
Вводный период позволяет оценить переносимость стандартной терапии, темпы развития анемии, несколько снизить агрессивность развития последней. Так, по результатам РКИ [12] отсутствие вводной фазы можно считать предиктором и фактором риска развития тяжелой анемии, а также анемии, требующей проведения гемотрансфузии.
Результаты исследований RESPOND-2 и PROVE-2 продемонстрировали, что вводный период при отсутствии снижения виремии можно использовать как ранний предиктор развития мутантных штаммов HCV, резистентных к проводимой терапии. В этом случае своевременная отмена ПВТ позволит избежать развития лекарственной резистентности.
Перечислим схемы лечения с применением боцепревира в зависимости от категории пациентов.
Для пациентов, ранее не получавших лечения, по окончании 4 недель вводного периода дополнительно назначается боцепревир строго в сочетании со стандартной терапией ПЭГ-ИНФ-альфа и рибавирином:
- при отсутствии HCV PHK на 8-й и 24-й неделе терапии ее длительность составляет 28 недель;
- при наличии HCV PHK на 8-й неделе терапии и отсутствии на 24-й неделе тройная терапия продолжается 32 недели с последующим применением стандартной терапии ПЭГ-ИНФ-альфа и рибавирином в течение 12 недель.
Для нон-респондеров предусмотрен следующий алгоритм:
- при отсутствии HCV PHK после 8-й и 24-й недели для пациентов с рецидивом и частичным вирусологическим ответом продолжительность терапии составляет 32 недели;
- при наличии HCV PHK после 8 недель терапии и отсутствии после 24 недель тройная терапия продолжается 32 недели с последующим применением стандартной терапии ПЭГ-ИНФ-альфа и рибавирином в течение 12 недель.
Для пациентов с циррозом печени длительность тройной терапии всегда составляет 48 недель (табл. 3).
РКИ с применением телапревира показали отсутствие достоверной разницы в достижении УВО у пациентов при наличии и отсутствии вводной фазы [13], что послужило поводом для одобрения телапревира к использованию в клинической практике без вводной фазы.
У пациентов, ранее не получавших лечения, телапревир назначается с первого дня терапии строго в сочетании со стандартной терапией ПЭГ-ИНФ-альфа и рибавирином длительностью 12 недель:
- при отсутствии виремии, HCV PHK(-), после 4-й и 12-й недели длительность терапии составляет 24 недели;
- при обнаружении вируса, HCV РНК(+), после 4-й или 12-й недели – 48 недель.
Для нон-респондеров (рецидив, частичный вирусологический ответ, нулевой ответ), как и для пациентов с циррозом печени, возможен единственный вариант назначения тройной терапии с телапревиром – 12 недель, общая продолжительность ПВТ – 48 недель (табл. 4).
Важный момент: при проведении тройной терапии необходимо строго соблюдать правила отмены. Неэффективная тройная ПВТ с применением боцепревира должна быть вовремя остановлена, чтобы предотвратить формирование боцепревир-резистентных штаммов HCV. Если на 12-й неделе ПВТ (то есть на 8-й неделе тройной терапии) уровень HCV PHK составляет более 100 МЕ/мл или на 24-й неделе ПВТ (то есть на 20-й неделе тройной терапии) не достигнута авиремия, лечение должно быть остановлено.
Что касается телапревира, лечение должно быть прекращено, если уровень HCV PHK превышает 1000 МЕ/мл после 4-й и/или 12-й недели тройной терапии, и при определяемом количестве HCV PHK на 24-й неделе ПВТ (табл. 5) [14].
Эти правила основаны на данных доказательной медицины, полученных в ходе многоцентровых РКИ. Наличие HCV PHK в указанных выше титрах свидетельствует о неэффективной ПВТ, продолжение которой не обосновано ни клинически, ни экономически. Кроме того, продолжение терапии может стать причиной возникновения резистентных штаммов, что показано в РКИ II и III фазы в группах с рецидивом и отсутствием вирусологического ответа.
К особенностям тройной терапии можно отнести риск развития нежелательных явлений, не характерных для стандартной ПВТ. К сожалению, в РКИ тройная терапия показала множество нежелательных явлений, которые, вероятно, впоследствии станут ограничивать применение ингибиторов протеазы I поколения.
Исходя из изложенного можно сделать следующие выводы:
1. Новые препараты для лечения хронического гепатита C – ингибиторы сериновой протеазы (боцепревир, телапревир) послужили основой для создания схем тройной терапии. Эффективность лечения у пациентов с 1 генотипом HCV заметно возросла.
2. Применение принципа «терапия по ответу» максимально обеспечивает индивидуальный подход при проведении ПВТ, что позволяет сократить длительность лечения, снизить медикаментозную нагрузку и экономические расходы.
3. Максимальная эффективность лечения достигается при использовании дифференцированного подхода к выполнению всех режимов ПВТ в зависимости от исходных данных пациента, при наличии знаний и навыков по диагностике и коррекции нежелательных явлений и соблюдении правил отмены тройной терапии.
Источник


