Высокая репликация вируса гепатита с
Вирус гепатита С – возбудитель инфекционного заболевания, сопровождающегося постоянным прогрессированием некротических изменений тканей печени, вплоть до злокачественного перерождения и формирования метастатических опухолей.

РНК вируса обнаруживается в крови лабораторными методиками уже спустя 7–14 дней после инфицирования. Но выделение патогена в отдельной культуре и его искусственная репликация до недавнего времени представляли серьезную проблему.
И только в середине 2000-х годов удалось выделить главные структурные протеины и неструктурные белки вируса, механизмы его репликации в гепатоцитах.
Основные случаи инфицирования вирусом HCV связаны с непосредственным попаданием патогена в кровь при гемотрансфузии, с засохших частиц контаминированного материала на медицинских, диагностических и косметологических инструментах.
Гораздо реже возбудитель HCV передается при половом акте. Вероятность внутриутробного инфицирования не превышает 3–5%. При этом окончательно не установлено, происходит передача вируса через плаценту либо во время родов.
История и эпидемиология инфекционной болезни
Впервые о гепатите «ни А ни В» заговорили в 1970-х годах. Но клонировать патоген удалось только в начале 1990-х годов. История болезни связана с разнообразными теориями, впоследствии не получившими подтверждения.
Изначально большинство специалистов склонялось к мнению, что заболевание является асимптоматическим расстройством функциональной активности печени. При этом утверждалось, в отличие от других известных на тот момент инфекционных болезней органа, гепатит С не способен вызвать значимых осложнений (за исключением неспецифического увеличения концентрации аминотрансфераз).
Но последующее наблюдение за пациентами с HCV продемонстрировало, что у каждого пятого без лечения спустя 10–11 лет развивался цирроз.
С появлением лабораторных методик, позволяющих подробно изучить, как выглядит вирус под микроскопом, выделить из сыворотки крови специфические антитела стали возможными долговременные клинические исследования. Провели культивирование и анализ образцов биологического материала, ранее полученных от пациентов, инфицированных HCV (до 5–10 –15 и более лет назад). Таким образом появились убедительные данные относительно эволюции HCV-инфекции.
Одним из главных выводов стало подтверждение возможности самостоятельной эрадикации вируса на острой стадии течения заболевания. Причем чаще это происходит у больных младше 12 лет.
Риск развития цирроза установили на уровне 15%, и подобные нарушения печени формировались спустя 20–25 лет. Позже, по мере накопления клинического и практического опыта, данные были скорректированы.
Сформировалось четкое представление о прогрессировании вирусной инфекции. Установлена взаимосвязь между HCV и разнообразными внепеченочными проявлениями. Изучение иммунологического ответа на антигены вируса позволило предположить вероятность формирования аутоиммунных нарушений, которые затрагивают щитовидную железу, сосудистую систему, опорно-двигательный аппарат.
Причем если доктора могут с уверенностью сказать, как HCV повлияет на работу печени через 5–20 и более лет после заражения, то прогнозировать внепеченочные проявления инфекции невозможно.
Только недавно частицы вируса были обнаружены в различных структурах нервной системы, в частности, головном мозге. Это позволило предположить прямую связь первых симптомов инфекции (усталости, слабости, психоэмоциональных расстройств и т.д.) с особенностями патогенеза заболевания.
Постоянно появляются новые тест-системы. Причем каждое последующее поколение диагностических наборов отличается большей специфичностью, точностью и чувствительностью.
Эпидемиологические аспекты развития гепатита С
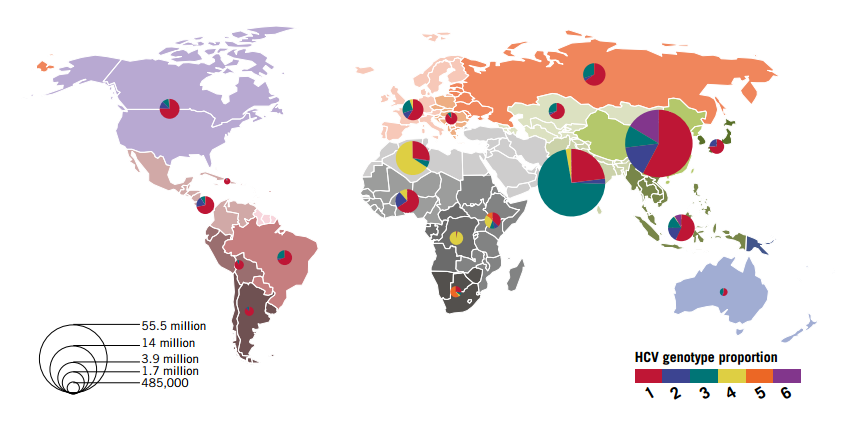
Общее количество инфицированных колеблется в пределах 3–5% населения земного шара. Но медицинская статистика учитывает только официальные данные, на практике эта цифра гораздо выше. Патология преимущественно распространена в странах, расположенных на севере Африканского континента, в Европе – на юге Италии.
Недавно появились данные относительно увеличения количества заболевших в Китае, Пакистане и некоторых других азиатских странах. Минимальное число пациентов (менее 0,1%) зарегистрировано в Великобритании и странах Скандинавии.
Эпидемиология гепатита С на территории России изучена недостаточно. Полагают, что количество заболевших составляет 2,0–2,9%.
Способы заражения
Передача инфекционного гепатита С возможна при:
- переливании крови и ее продуктов;
- трансплантации органов, изъятых у инфицированных доноров;
- инъекциях и другие инвазивных процедурах, выполняемых контаминированным инструментарием.
С появлением высокочувствительных тест-систем вероятность инфицирования при гемотрансфузии практически сведена к нулю. А большая часть случаев заболевания связана с заражением при использовании общих игл (например, в США эта цифра достигает 60% от общего количество заболевших).
По сравнению с парентеральным путем передачи, вероятность заразиться при половом контакте либо внутриутробно низка. Так, при случайном, единоразовом повреждении кожи контаминированным инструментом риск заражения оценивают в 7–10%, перинатально – не более 5–6%.
Данные относительно полового пути передачи HCV противоречивы. Известны случаи длительных постоянных отношений, когда один из партнеров инфицирован, при этом другой оставался совершенно здоровым. Точный источник заражения вирусом установить чаще всего затруднительно.
Что значит РНК вируса гепатита С
К настоящему моменту идентифицировано 6 основных генотипов инфекционного гепатита С, которые отличаются специфической географической привязанностью. Определение конкретной разновидности заболевание имеет огромное значение в подборе схемы терапии патологии. Установлено, что если выявлен 1 генотип, вероятность положительного эффекта лечения ниже.
HCV относится к семейству Flaviviridae. Как и другие представители этого класса, представляет собой заключенный в оболочку нуклеокапсид, который проникает в клетки печени из кровотока. После попадания в гепатоциты внешняя мембрана патогена разрушается, и высвобождаются частицы вируса, размер которых не превышает 70 нм.
РНК вируса гепатита С – это значит геном патогена, состоит из одной цепи и включает короткие некодируемые участки, каждый из которых заканчивается кодируемой последовательностью полипротеинов. На 341 «звене» находится 5 нетранслируемый участок, который формирует сложную вторичную структуру, необходимую для репликации вируса.

N-участок полипротеинов кодирует структурные белки, включая основной элемент нуклеокапсида core и гликопротеины оболочки Е1 и Е2, которые в сочетании с неструктурными протеинами NS2–NS5B формируют вирусные частицы (NS3, NS4A, NS4B, NS5A и NS5B также играют огромную роль в репликации HCV).
С-конечный участок core и протеины оболочки при помощи специфических пептидаз обеспечивают проникновение вируса в клетку печени и последующее взаимодействие с эндоплазматическим ретикулумом и другими органеллами гепатоцита.
Core и фактически каждый из неструктурных протеинов являются антигенами, провоцирующими выработку антител (АТ). Установление их титра лежит в основе иммуноферментного анализа – одного из основных диагностических тестов для подтверждения болезни. При позитивном результате обследование пациентов продолжают при помощи полимеразной цепной реакции, основная цель которой – определение РНК HCV.
Если РНК не обнаружена, лечение не назначают, даже при позитивном ИФА. Но наличие РНК, подтвержденное результатами ПЦР, свидетельствует об инфицировании. При минимальной виремии (без роста показателей) человек долгое время может оставаться носителем болезни. Но в любой момент распространение процесса может ускориться.
После постановки диагноза у пациента возникает вопросы:
- HCV является вирусом или бактерией?
Возбудитель заболевания – РНК-содержащий вирус, поэтому прием антибиотиков не только нецелесообразен, но и опасен из-за гепатотоксичности подавляющего большинства антибактериальных средств. - Когда лучше делать анализ на HCV?
Антитела к патогену выделяются сразу же после проникновения вируса в организм. Но в количестве, достаточном для определения лабораторным путем, иммуноглобулины накапливаются в среднем через 2 месяца. Что касается ПЦР, сроки выявления зависят от аналитической чувствительности РНК. При использовании современных тестов анализ можно делать уже через 10–14 суток.
Изучение под микроскопом и при помощи других технологий строение вируса позволило создать высокоэффективные препараты, необратимо останавливающие процессы деления РНК.
Устойчивость возбудителя
Распространенность HCV и существующий риск заражения при различных манипуляциях, включая эстетические процедуры, обуславливает устойчивость вируса гепатита С во внешней среде. Перечень биологических жидкостей, где содержится возбудитель в концентрациях, достаточных для заражения, ограничен.
В первую очередь, это кровь (как в «свежем», так и в засохшем состоянии). В сперме, выделениях из влагалища, менструальной крови HCV присутствует в минимальной концентрации. Как правило, ее недостаточно для заражения человека с полноценно работающей иммунной системой. Но при снижении резистентности организма, вероятность инфицирования многократно возрастает.
В слюне вирус практически не обнаруживается. Это связывают с находящимися в ротовой полости ферментами, которые разрушают белки, составляющие структуру HCV. Поэтому вероятность передачи патогена при поцелуях минимальна.
Жизненный цикл вируса таков, что он сохраняет активность и контагиозность продолжительное время в засохшей крови. При благоприятных температурных условиях (от 6 до 20 градусов выше нуля) этот срок длится до 4–6 недель. При повышении температуры данный период сокращается до 5–6 суток. При заморозке (в том числе донорского материала) HCV остается жизнеспособным на протяжении неопределенного времени и является заразным и после размораживания.
Какие процессы запускаются после инфицирования
Основной «мишенью» для HCV являются клетки печени. Однако при хроническом течении инфекции (по данным клинических экспериментов, проведенных с участием шимпанзе) частицы вируса обнаруживаются в лимфоидной ткани и дендритных клетках.
Но применительно к течению патологии у человека эта информация требует подтверждения. Достоверно известно, что HCV отличается тропностью именно к тканям печени.
Лабораторная диагностика
Выявить возбудителя гепатита С в крови можно при помощи ряда диагностических тестов:
- иммуноглобулины к HCV определяют иммуноферментным анализом;
- установить наличие РНК можно методом качественной или количественной ПЦР.
Косвенно на вирусное поражение печени могут указывать результаты печеночных проб и биохимического анализа крови. Если антитела или РНК патогена в крови не обнаружены, но риск заражения слишком велик (например, после случайного пореза, незащищенного полового акта и т.д.) исследования повторяют через 2–3 месяца.

Генотипирование вируса гепатита С
Разница в структуре между разновидностями патогена составляет порядка 30–35%. Внутри одного генотипа выделяют субтипы, различия между ними не превышают 25%. У каждого пациента Hepatitis C Virus может мутировать с формированием так называемых квази-типов.
Генотипирование вируса гепатита С – один из основных анализов, назначается только один раз и обязательно проводится перед началом курса противовирусной терапии.
Для определения разновидности патогена РНК HCV должна содержаться в крови в достаточно высокой концентрации. Поэтому, если не определяется генотип патогена, исследование повторяют через 1–2 недели.
Тип возбудителя гепатита С в целом влияет как на медикаменты, составляющие схему лечения, так и на прогноз. При 3 генотипе обязательны инструментальные исследования печени из-за высокого риска осложнений. Первый тип крайне сложно поддается терапии.
Генотипирование проводится методом ПЦР.
Лечение и профилактика
Эффективность противовирусной терапии напрямую зависит от стадии болезни, когда был поставлен диагноз. Софосбувир, Даклатасвир, Велпатасвир и другие медикаменты прямого действия позволяют вывести вирус из организма практически у всех пациентов вне зависимости от генотипа.
Поэтому при подозрении на заражение следует сдать кровь на ИФА или ПЦР. Для постановки диагноза на ранней стадии эти исследования повторяют ежегодно.
Специфической профилактики (вакцины) от гепатита С не существует.
Как убить патоген
Для обработки медицинских инструментов и рабочей поверхности используют химические растворы и соединения, способные убить вирус, т. е. содержащие хлористоводородную, фосфорную кислоту, пропанол, этанол.
Когда пациенты интересуются, убивает ли спирт вирус, доктора дают положительный ответ. Но объясняя, погибает ли от спирта возбудитель гепатита С, врач подчеркивает, что концентрация этанола должна быть не менее 70%.
Также патоген уничтожается при термической обработке. При какой температуре убивается возбудитель HCV? При 60°для этого требуется 20–30 минут, при температуре кипячения – до 5 минут, при дезинфекции в автоклаве – около 1,5–2 минут. Подобные режимы обработки подходят для стерилизации медицинского и косметического инструментария, стирки белья, загрязненного контаминированным материалом.
Источник
Вирус гепатита С (ВГС) представляет собой небольшой (55-65 нм в размере) сферический РНК-содержащий вирус из семейства Flaviviridae. HCV является причиной развития гепатита С в организме человека. ВГС состоит из основного генетического материала (РНК), окруженной защитной белковой оболочкой, а также липидной (жировой) оболочкой сотовой структуры, которая содержит два оболочечных белка — гликопротеины E1, E2, встроенные в липидные оболочки. 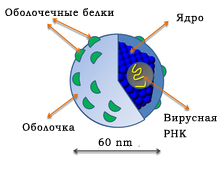 Белки E1 и E2 обеспечивают проникновение вируса в клетку и закрепление в ней.
Белки E1 и E2 обеспечивают проникновение вируса в клетку и закрепление в ней.
Геном HCV включает в себя одноцепочную РНК, имеющую 9600 нуклеотидных оснований. На 5′ и 3′ концах РНК ВГС расположены нетранслируемые регионы, имеющие приблизительно 340 и 60 оснований, которые важны для жизнедеятельности и репликации вирусной РНК. Гены, кодирующие структурные белки, расположены у 5′ области генома вируса, а неструктурные — у 3′ области. 5′ участок генома вируса гепатита С кодирует три структурных белка ВГС: два оболочечных белка, кодированных зоной Е1 и Е2 и C (кор) нуклеокапсидный белок.
3′ область генома кодирует неструктурные белки NS2 , NS3, NS4 , NS4A, NS4B, NS5 , NS5A и NS5B. 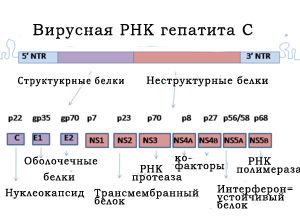 Белки, кодированные с зон NS2 и NS4, выполняют клеточную мембранную функцию. Белок зоны NS3 является РНК-протеазой. Белок, синтезированный NS4A зоной, выполняет стабилизирующую функцию. Зона NS5B представляет собой РНК-полимеразу. NS5A устойчив к интерферону и играет значительную роль в вирусном патогенезе.
Белки, кодированные с зон NS2 и NS4, выполняют клеточную мембранную функцию. Белок зоны NS3 является РНК-протеазой. Белок, синтезированный NS4A зоной, выполняет стабилизирующую функцию. Зона NS5B представляет собой РНК-полимеразу. NS5A устойчив к интерферону и играет значительную роль в вирусном патогенезе.
Репликация HCV включает в себя несколько этапов. Вирус размножается в основном в гепатоцитах печени, где, по оценкам, ежедневно каждая инфицированная клетка производит около пятидесяти вирионов (вирусных частиц). Вирус может также реплицировать в мононуклеарных клетках периферической крови, что способствует высокому уровню иммунологических нарушений, обнаруживаемых у инфицированных хроническим гепатитом С (ХВГС). 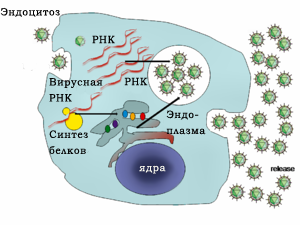 Вступление в клетки хозяина происходит через сложные взаимодействия между вирионами и клеточными поверхностями молекул. Оказавшись внутри гепатоцитов, ВГС использует внутриклеточный механизм репликации. Геном ВГС использует для получения одного белка более 3000 аминокислот. Полипротеин взаимодействует с вирусной и клеточной протеазой для производства трех структурных и семи неструктурных (NS) белков. РНК формируется с помощью РНК-зависимой полимеразы NS5B, которая производит отрицательную цепь промежуточных РНК. Отрицательные цепи РНК затем служат шаблоном для производства новых позитивно-ориентированных вирусных геномов. Находящиеся в стадии становления геномы могут далее реплицироваться и образовывать новые вирусные частицы, которые впоследствии выходят из клетки.
Вступление в клетки хозяина происходит через сложные взаимодействия между вирионами и клеточными поверхностями молекул. Оказавшись внутри гепатоцитов, ВГС использует внутриклеточный механизм репликации. Геном ВГС использует для получения одного белка более 3000 аминокислот. Полипротеин взаимодействует с вирусной и клеточной протеазой для производства трех структурных и семи неструктурных (NS) белков. РНК формируется с помощью РНК-зависимой полимеразы NS5B, которая производит отрицательную цепь промежуточных РНК. Отрицательные цепи РНК затем служат шаблоном для производства новых позитивно-ориентированных вирусных геномов. Находящиеся в стадии становления геномы могут далее реплицироваться и образовывать новые вирусные частицы, которые впоследствии выходят из клетки.
Наиболее широко используются классификация вируса гепатита С по следующим генотипам (основным типам): 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 и 11. Генотипы ВГС могут быть разбиты на подтипы, некоторые из которых включают в себя:
1a, 1b, 1c
2a, 2b, 2c
3a, 3b
4a, 4b, 4c, 4d, 4e
5a
6a
7a,7b
8a, 8b
9a
10a
11a
HCV эволюционировал в течение нескольких тысяч лет. Этот факт может объяснить нынешние особенности глобального распространения генотипов и подтипов:
1а — распространен в основном в Северной и Южной Америке, а также в Австралии
1b — чаще всего встречается в Европе и Азии.
2a — наиболее распространен в Японии и Китае.
2b — в США и Северной Европе
2c — в Западной и Южной Европе.
3а — Австралия, Европа и Южная Азия.
4а — Египет
4с — Центральная Африка
5а — Южная Африка
6а — Гонконг, Макао и Вьетнам
7а и 7b — Таиланд
8а, 8b и 9а — Вьетнам
10а и 11а — Индонезия
Всемирная организация здравоохранения на сегодня выделяет 6 основных генотипов вируса, их распространенность представлена ниже:
В Европе и России частота определения генотипов располагается в следующем порядке: 1b, 3а, 2а, 2b. Генотип является клинически важным при определении потенциального ответа на терапию различными препаратами и продолжительности такой терапии.
Генотипы 1 и 4 более устойчивы к терапии на основе интерферона, чем другие генотипы (2, 3, 5 и 6). При применении безинтерфероновых схем лечения генотип также влияет на стратегию лечения. Инфицирование одним генотипом не дает иммунитета против инфицирования другим типом, поэтому возможно одновременное заражение двумя и более штаммами. В большинстве из этих случаев, один из штаммов доминирует над другим.
Анимация действия вируса HCV
Еще материалы: О вирусе гепатита С
Источник
Классификация вируса: | |
Группа: | Группа IV ((+)ssRNA) |
Семейство: | Flaviviridae |
Род: | Гепацивирус |
Вид Вирус гепатита С | |
Вирус гепатита С (HCV или иногда HVC) – это маленький (размером 55–65 нм) позитивный однонитевой РНК-вирус в оболочке из семейства Flaviviridae. Вирус гепатита C – это причина гепатита C у людей.
Содержание статьи:
- Таксономия вируса гепатита С
- Структура
- Геном вируса гепатита С
- Молекулярная биология
- Репликация вируса гепатита С
- Видео о вирусе гепатита С
- Генотипы
- Клиническая важность
- Эволюция вируса гепатита С
- Вакцинация от вируса
- Текущие исследования
- Стабильность в окружающей среде
Таксономия вируса гепатита С
Вирус гепатита C принадлежит к роду гепацивируса, члена семейства Flaviviridae. До недавних пор он считался единственным членом этого рода. Однако у собак был открыт другой член этого рода – canine hepacivirus. Также есть, по крайней мере, один вирус в этом роде, который инфицирует лошадей.
Структура
Частица вируса гепатита C состоит из ядра генетического материала (РНК), окруженного икосаэдрической защитной оболочкой из белка и далее погруженного в жировую оболочку клеточного происхождения. Два гликопротеина вирусной оболочки, Е1 и Е2, встроены в жировую оболочку.
Геном вируса гепатита С
Вирус гепатита C имеет геном позитивной однонитевой РНК. Геном состоит из единой открытой рамки считывания длиной 9600 нуклеотидных основ. Эта единая открытая рамка считывания транслируется для образования единого белкового продукта, который далее обрабатывается для образования меньших активных белков.
На 5′ и 3′ концах РНК находятся участки UTR, которые не транслируются в белки, но важны для трансляции и репликации вирусной РНК. Участок 5′ UTR имеет место связывания рибосомы (IRES – участок внутренней посадки рибосомы), который начинает трансляцию очень длинного белка, содержащего около 3000 аминокислот. Домен ядра IRES вируса гепатита C (HCV) содержит четырехстороннее спиральное соединение, объединенное в прогнозированном псевдоузле. Конформация этого домена ядра сдерживает направление открытой рамки считывания для позиционирования на рибосомальной субъединице 40S. Большой первичный белок затем разрезается клеточными и вирусными протеазами на 10 меньших белков, которые позволяют репликацию вируса в клетке носителя или собираются в зрелые вирусные частицы.
Структурные белки, образованные вирусом гепатита С, включают капсидный белок, E1 и E2; неструктурные белки включают NS2, NS3,NS4, NS4A, NS4B, NS5, NS5A и NS5B.
Молекулярная биология
Белки этого вируса упорядочены вдоль генома в следующем порядке: N конец-ядро-оболочка (E1)-E2-p7-неструктурный белок 2 (NS2)-NS3-NS4A-NS4B-NS5A-NS5B-C-конец. Поколение зрелых неструктурных белков (от NS2 до NS5B) полагается на активность вирусной протеиназы. Соединение NS2/NS3 расщепляется металл-зависимой автокаталитической протеиназой, закодированной в NS2 и в N-конце NS3. Оставшееся расщепление ниже от этого участка катализируется сериновой протеиназой, также содержащейся в N-концевом участке NS3.

Капсидный белок имеет 191 аминокислоту и может быть разделен на три домена на основе гидрофобности: домен 1 (остатки 1-117) содержит главным образом основные остатки с двумя короткими гидрофобными участками; домен 2 (остатки 118-174) менее основной и более гидрофобный, и его С-конец находится в конце p21; домен 3 (остатки 175-191) высоко гидрофобный и действует, как сигнальная последовательность для белка оболочки Е1.
Оба белка оболочки (E1 и E2) высоко гликозилированны и важны в проникновении клетки. E1 служит в качестве сливающей субъединицы, а Е2 служит, как белок связывания рецепторов. Е1 имеет 4-5 N-связанных гликанов и E2 имеет 11 участков N-гликозилации.
Вернуться к содержанию
Белок p7 необязателен для репликации вирусного генома, но играет важную роль в вирусном морфогенезе. Этот белок – это трансмембранный белок из 63 аминокислот, который располагается в эндоплазматической сети. Расщепление p7 опосредовано сигнальными пептидазами эндоплазматической сети. Два трансмембранных домена р7 соединены цитоплазматической петлей и направлены к просвету эндоплазматической сети.
Белок NS2 – это трансмембранный белок 21-23 килодальтон (кДа) с активностью протеаз.
NS3 – это белок 67 кДа, чей N-конец имеет активность сериновой протеазы и С-конец имеет активность NTP-азы/геликазы. Он расположен в эндоплазматической сети и формирует гетеродимерный комплекс NS4A – мембранный белок из 54 аминокислот, который выступает, как кофактор протеиназы.
NS4B — это маленький (27 кДа) гидрофобный цельный мембранный белок с 4 трансмембранными доменами. Он расположен в пределах эндоплазматической сети и играет важную роль для рекрутинга других вирусных белков. Он стимулирует морфологические изменения в эндоплазматической сети, образуя структуру под названием «мембранная сеть».
NS5A – это гидрофобный фосфопротеин, играющий важную роль в вирусной репликации, модуляции сигнальных путей клеток и реакции интерферона. Он связывается с васкулоадгезивными белками человека, закрепленными на эндоплазматической сети.
Белок NS5B (65 кДа) – вирусная РНК-зависимая РНК-полимераза. NS5B имеет ключевую функцию репликации вирусной РНК вируса гепатита С, используя положительно полярную нить РНК вируса в качестве матрицы, и катализирует полимеризацию рибонуклеозид—трифосфатов (rNTP) во время репликации РНК. Несколько структур кристаллов полимеразы NS5B в нескольких кристаллических формах были определены на основе той же консенсусной последовательности BK (HCV-BK, генотип 1). Структура может быть представлена в форме правой руки с пальцами, ладонью и большим пальцем. Охваченный по окружности активный участок, уникальный для NS5B, содержится в структуре ладони белка. Недавние исследования структуры нити J4 (HC-J4) генотипа 1b белка NS5B указали на присутствие активного участка, где возникает возможный контроль связывания нуклеотидов и инициация синтеза РНК заново. Процесс заново добавляет необходимые праймеры для инициации репликации РНК. Текущее исследование пытается связать структуры с этим активным участком для изменения его функциональности, чтобы предотвратить дальнейшую репликацию вирусной РНК.
Также был описан 11-й участок. Этот белок кодируется +1 сдвигом рамки считывания в капсидном гене. Он кажется антигенным, но его функция не известна.
Репликация вируса гепатита С
 Репликация вируса гепатита С включает несколько этапов. Вирус воспроизводится в основном в печеночных клетках, где по оценкам ежедневно каждая инфицированная клетка производит приблизительно пятьдесят вирионов (вирусных частиц), при этом подсчитанная сумма составляет один триллион генерированных вирионов. Вирус также может производиться в одноядерных клетках периферической крови, потенциально являясь причиной высоких уровней иммунологических нарушений, обнаруженных у пациентов, хронически инфицированных вирусом гепатита С. Вирус гепатита С имеет широкое разнообразие генотипов и быстро мутирует из-за высокого процента ошибок на части РНК-зависимой РНК-полимеразы вируса. Скорость мутации порождает так много вариантов вируса, что они считаются квазивидами, а не традиционными видами вируса. Вход в клетки-хозяева происходит через комплексное взаимодействие между вирионами и молекулами клеточной поверхности CD81, рецептором ЛНП, SR-BI, DC-SIGN, клаудином-1 и окклудином.
Репликация вируса гепатита С включает несколько этапов. Вирус воспроизводится в основном в печеночных клетках, где по оценкам ежедневно каждая инфицированная клетка производит приблизительно пятьдесят вирионов (вирусных частиц), при этом подсчитанная сумма составляет один триллион генерированных вирионов. Вирус также может производиться в одноядерных клетках периферической крови, потенциально являясь причиной высоких уровней иммунологических нарушений, обнаруженных у пациентов, хронически инфицированных вирусом гепатита С. Вирус гепатита С имеет широкое разнообразие генотипов и быстро мутирует из-за высокого процента ошибок на части РНК-зависимой РНК-полимеразы вируса. Скорость мутации порождает так много вариантов вируса, что они считаются квазивидами, а не традиционными видами вируса. Вход в клетки-хозяева происходит через комплексное взаимодействие между вирионами и молекулами клеточной поверхности CD81, рецептором ЛНП, SR-BI, DC-SIGN, клаудином-1 и окклудином.
Вернуться к содержанию
Попав внутрь печеночной клетки, вирус гепатита C овладевает частями внутриклеточной механики для репликации. Геном вируса гепатита C транслируется для образования одного белка из приблизительно 3011 аминокислот. Затем полипротеин проходит протеолитическую обработку вирусными и клеточными протеазами для образования трех структурных (вирион-ассоциированных) и семи неструктурных (NS) белков. Альтернативно сдвиг рамки может возникнуть в области ядра для образования белка альтернативной рамки считывания (ARFP). Вирус гепатита C кодирует две протеазы, аутопротеазу цистеина NS2 и сериновую протеазу NS3-4A. NS белки затем вербуют вирусный геном в комплекс репликации РНК, который связан с перегруппированными цитоплазматическими мембранами. Репликация РНК происходит через РНК-зависимую РНК-полимеразу NS5B, которая производит промежуточную форму отрицательно полярной нити РНК. Отрицательно полярная нить РНК затем выступает в качестве матрицы для новых вирусных геномов с положительной полярностью. Появляющиеся геномы затем могут быть транслированы, далее воспроизведены или упакованы в новых вирусных частицах. Новые вирусные частицы, как считается, пускают ростки в выделительные пути и выпускаются на поверхности клетки.
Вирус воспроизводится на внутриклеточных липидных мембранах. В частности, эндоплазматическая сеть деформируется в мембранные структуры уникальных форм под названием «мембранные сети». Эти структуры могут быть вызваны единой экспрессией вирусного белка NS4B. Белок ядра соединяется с липидными капельками и использует микротрубочки и динеины для изменения их местоположения в перинуклеарном распределении.
Выпуск из печеночной клетки может вовлекать выделительные пути липопротеинов очень низкой плотности.
Видео о вирусе гепатита С
Вернуться к содержанию
Генотипы
На основе генетических различий между изолятами вируса гепатита C его виды классифицируются на семь генотипов (1-7) с несколькими подвидами в каждом генотипе (в названиях представлены строчными буквами). Подвиды далее подразделяются на квазивиды на основе их генетического разнообразия. Генотипы различаются на 30-35% нуклеотидных участков по всему геному. Разница в геномном составе подвидов генотипа составляет обычно около 20-25%. Подвиды 1a и 1b обнаружены по всему миру и вызывают 60% всех случаев.
Клиническая важность
Генотип имеет клиническую важность в определении потенциальной реакции на терапию на основе интерферона и требуемой длительности такого лечения. Генотипы 1 и 4 менее восприимчивы к лечению на основе интерферона, чем другие генотипы (2, 3, 5 и 6). Длительность стандартной терапии на основе интерферона для генотипов 1 и 4 составляет 48 недель, в то время как лечение для генотипов 2 и 3 длится 24 недели. Устойчивые вирусологические реакции возникают в 70% случаев генотипа 1, около 90% случаев генотипов 2 и 3, 65% — генотипа 4 и 80% — генотипа 6.
Инфицирование одним генотипом не дает иммунитета против других, и возможно сопутствующее инфицирование двумя штаммами. В большинстве этих случаев один из штаммов удаляет другой из хозяина в короткий период времени. Эта находка открывает дверь для замещения штаммов, не реагирующих на медикаменты, другими штаммами, которые легче поддаются лечению.
Эволюция вируса гепатита С
Определение происхождения этого вируса было трудным, но генотипы 1 и 4 кажутся имеющими общее происхождение. Байсовский анализ предполагает, что главные генотипы разошлись около 300-400 лет назад от вируса-предка. Второстепенные генотипы разошлись около 200 лет назад от главных генотипов. Считается, что все сохранившиеся до наших дней генотипы возникли от подтипа 1b генотипа 1.
Исследование штаммов генотипа 6 предполагает более раннюю дату эволюции: около 1100-1350 лет назад (95% вероятная область, от 600 до >2500 лет назад). Оцененная скорость мутации была 1,8 × 10−4 (95% вероятная область: 0,9 × 10−4 to 2.9 × 10−4). Этот генотип может быть предком других генотипов.
Исследование изолятов из Европы, США и Японии предполагает, что датой происхождения генотипа 1b является приблизительно 1925 г. Оцененные даты происхождения типов 2a и 3a – 1917 и 1943 гг., соответственно. Время расхождения типов 1a и 1b было оценено приблизительно в 200-300 лет назад.
Исследование генотипа 1a и 1b оценило следующие даты происхождения: 1914-1930 (95% вероятный интервал: 1802-1957 гг.), для типа 1a – 1911-1944 гг. (95% вероятный интервал: 1806-1965 гг.), для типа 1b. Оба вида 1a и 1b перенесли массовую экспансию в размере эффективной популяции между 1940 и 1960 гг. Экспансия подвида 1b вируса гепатита C предшествовала экспансии подвида 1а минимум на 16 лет (95% вероятный интервал: 15–17 лет). Оба вида, как кажется, распространились из развитых стран в развивающиеся страны.
Вернуться к содержанию
Штаммы генотипа 2 из Африки можно разделить на четыре клада, которые связаны со страной своего происхождения:
- Камерун и Центральная Африканская Республика;
- Бенин, Гана и Буркина-Фасо;
- Гамбия, Гвинея, Гвинея-Биссау и Сенегал;
- Мадагаскар.
- Считается, что генотип 3 происходит из Юго-Восточной Азии.
 Эти данные из разных стран предполагают, что этот вирус мог возникнуть в Юго-Восточной Азии и распространился в Западную Африку торговцами из Западной Европы. Позднее он попал в Японию, когда была снята само-изоляция страны. После попадания в страну на его распространение повлияли многие локальные факторы, в том числе переливания крови, программы вакцинации, злоупотребление внутривенными наркотиками и режимы лечения. Учитывая уменьшение скорости распространения после введения скрининга продуктов крови на гепатит C в 1990-х, кажется, что, по крайней мере, в недавнее время переливание крови являлось важным способом распространения этого вируса. Для определения данных эволюции разнообразных генотипов и сроков их распространения по всему миру требуется дополнительная работа.
Эти данные из разных стран предполагают, что этот вирус мог возникнуть в Юго-Восточной Азии и распространился в Западную Африку торговцами из Западной Европы. Позднее он попал в Японию, когда была снята само-изоляция страны. После попадания в страну на его распространение повлияли многие локальные факторы, в том числе переливания крови, программы вакцинации, злоупотребление внутривенными наркотиками и режимы лечения. Учитывая уменьшение скорости распространения после введения скрининга продуктов крови на гепатит C в 1990-х, кажется, что, по крайней мере, в недавнее время переливание крови являлось важным способом распространения этого вируса. Для определения данных эволюции разнообразных генотипов и сроков их распространения по всему миру требуется дополнительная работа.
Вакцинация от вируса
В отличие от гепатита A и B в настоящий момент не существует вакцины для предотвращения инфекции гепатита C.
Текущие исследования
Исследованию вируса гепатита C помешал узкий диапазон хозяев вируса гепатита С. Использование репликонов было успешным, но они были открыты только недавно. Вирус гепатита C, как и большинство РНК-вирусов, существует в качестве вирусных квазивидов, что делает очень трудным выделение одной нити или типа рецептора для исследования. В настоящий момент исследование сфокусировано на ингибиторах вирусной протеазы с низким молекулярным весом, полимеразы РНК и других неструктурных генов. Два вещества, ингибиторы протеазы NS3, – боцепревир компании «Merck» и телапревир от «Vertex Pharmaceuticals Inc» — были одобрены для применения 13 мая 2011 г. и 23 мая 2011 г., соответственно.
Сообщалось о возможной связи между низкими уровнями витамина D и плохой реакцией на лечение. В работе в лабораторных условиях было показано, что витамин D может быть способен уменьшить репликацию вируса. Хотя эта работа выглядит многообещающей, все еще не получены результаты клинических исследований.
Другие исследуемые вещества включают аналог-игибиторы нуклеозида/нуклеотида и ненуклеозидные ингибиторы РНК-зависимой РНК-полимеразы, ингибиторы неструктурного белка 5А и нацеленные на хозяина соединения, такие как ингибиторы циклофилина и силибинин.
Вернуться к содержанию
Стабильность в окружающей среде
Как множество вирусов, вирус гепатита C постепенно инактивируется снаружи тела носителя. Присутствие тепла может оказать сильное влияние на продолжительность жизни вируса за пределами тела. Вирус может оставаться заразным снаружи носителя в течение приблизительно 16 дней при 25°C и двух дней при 37°C, хотя он может оставаться активным в течение более 6 недель при температуре менее или равной 4°C. При нагреве до температур 60°C и 65°C, однако, вирус гепатита C может быть инактивирован за 8 и 4 минуты, соответственно.
Источник