Хронический вирусный гепатит современное лечение
Восстановить здоровое состояние клеток печени и ликвидировать воспаление помогают препараты, содержащие глицирризиновую кислоту (ГК) и эссенциальные фосфолипиды (ЭФ).
Перейти к примеру…
Имеются противопоказания. Необходимо проконсультироваться со специалистом.
Имеются противопоказания. Необходимо проконсультироваться со специалистом.
Гепатит С – серьезное вирусное заболевание, которое многими воспринимается как приговор. Однако новейшие методы лечения и медицинские препараты позволяют существенно замедлить или приостановить течение этой коварной болезни печени. В данной статье мы рассмотрим современные методы лечения гепатита С при помощи противовирусных и гепатопротекторных препаратов последнего поколения.
Гепатит С – болезнь века
Заболевание вызывает РНК-содержащий вирус из семейства Flaviviridae, обнаруженный учеными в 1989 году. Сокращенно вирус гепатита С называется ВГС или HCV. Вирус размножается в основном в клетках печени (гепатоцитах). Проникая в них, он использует внутриклеточный механизм репликации (самокопирования генома): каждая вирусная частица производит в день до 50 реплик, которые впоследствии выходят за пределы клетки-хозяина.
HCV – достаточно «старый» вирус, который эволюционировал в течение нескольких тысяч лет. Этим объясняется большое количество его разновидностей (на сегодняшний день известно 6 генотипов вируса и 90 субтипов). В Европе и России наиболее часто встречаются следующие типы гепатита С: 1b, 3а, 2а, 2b. Определение генотипа является важным для выбора схемы лечения гепатита С и продолжительности терапии.
Важно знать!
Инфицирование одним генотипом не дает иммунитета против других типов вируса гепатита С. В связи с этим возможно одновременное заражение двумя и более штаммами.
Гепатит С обычно протекает бессимптомно или с неярко выраженными проявлениями. Именно поэтому для обозначения данного заболевания применяются образные выражения «ласковый убийца» и «кроткая смерть». Начальный период (2–3 недели) может сопровождаться признаками, сходными с простудными инфекциями: слабость, суставные боли, расстройство пищеварения. Хронический гепатит С (далее – ХГС) приводит к развитию целого «букета» сопутствующих заболеваний, связанных с мочеполовой и сосудистой системой. В хроническом виде гепатит С нередко (в 50–90% случаев) переходит в цирроз и рак печени. Однако следует понимать, что на сегодняшний день гепатит С признан излечимым заболеванием, главное – вовремя обнаружить присутствие вируса и правильно лечиться.
Международная статистика
Около 150 миллионов человек в мире инфицированы гепатитом С. Ежегодно этот вирус поражает 3–4 миллиона, и более 350 тысяч умирает от связанных с ним болезней печени.
Уровень заболеваемости в различных регионах мира колеблется: от 0,6–1,4% в США и до 4–5% в африканских странах.
В России уровень излечимости 2 и 3 групп вируса достигает от 83 до 91%. По последним данным в нашей стране гепатитом С больны около 8 миллионов жителей. При этом в 1–5% случаев гепатит С приводит к летальному исходу. Согласно официальной статистике Роспотребнадзора, в 2014 году зарегистрировано более 2200 случаев заболевания острой формой гепатита С и более 57 000 – хронической. С января по август 2015 года данные показатели составили 1300 и 37 200 человек соответственно.
Причины заболевания
Многие ошибочно полагают, что гепатит С передается исключительно половым путем или во время введения наркотических средств с помощью шприца, однако это не так. Заражение нередко происходит во время медосмотров и различных медицинских манипуляций (около 10% от общего числа больных), когда имеет место контакт с кровью пациента: например, в стоматологическом кабинете, при введении инъекций и переливании крови, во время хирургического вмешательства, при проведении гинекологических и урологических исследований и т.д. Заражение может произойти и бытовым путем – например, при использовании маникюрных принадлежностей, бритв или зубных щеток, которые до этого контактировали с кровью носителя гепатита С. Инфицирование также возможно во время нанесения тату или пирсинга и т.д.
Следует помнить!
По данным российской статистики, каждый второй случай заболевания гепатитом С связан с внутривенным введением наркотических средств. Остальные 50% приходятся на больных гемофилией, а также хирургов, стоматологов, медсестер, парикмахеров – тех, кому приходится контактировать с кровью своих клиентов и пациентов.
Методы лечения гепатита С
Основная цель лечение гепатита С – эррадикация вируса (удаление вируса из организма). При невозможности эррадикации целями лечения могут быть: прекращение или замедление воспалительных процессов в печени, предотвращение перехода заболевания в цирроз или рак, Выбор лечения зависит от многих факторов: пола, возраста, вирусной нагрузки, состояния печени, характера течения заболевания (острый, хронический). Если риск развития цирроза высокий, то лечение должно быть назначено как можно скорее.
Сбалансированное питание и здоровый образ жизни
При лечении гепатита С обязательным условием является изменение образа жизни и режима питания. В частности, следует отказаться от вредных привычек – курения и чрезмерного употребления алкоголя. Принцип диеты заключается в нормализация функций печени, улучшении желчеотделения и обеспечении защиты желудка и кишечника от любых повреждений. Основные правила диеты «Стол № 5», которая обычно назначается больным гепатитом:
- отказ от жареного, предпочтение – приготовленной на пару или отварной пище;
- прием пищи 5-6 раз в день небольшими порциями;
- обильное питье с достаточным количеством воды – не менее 1,5 литров в день;
- в дневном рационе должно содержаться не более 100 граммов белков, до 100 граммов жира, до 450 граммов углеводов (из них сахаров – до 50 граммов). Соль – не более 10 граммов в день.
Запрещенные продукты:
- Специи, а также все жареное, соленое, маринованное, копченое и консервированное.
- Жирное мясо, рыба и птица (в том числе мясные бульоны).
- Сдобные изделия, шоколад, мороженое.
- Кондитерские жиры (крема), маргарин, жиры животного происхождения.
- Сладкие газированные напитки, крепкий чай и кофе.
- Молочные продукты с высокой жирностью, соленые сыры.
- Бобовые, редька, шпинат, редис, щавель, чеснок, лук.
- Кислые фрукты и ягоды.
- Алкоголь.
Медикаментозное лечение: лекарственные препараты для лечения гепатита С
Основным методом лечения гепатита С в настоящее время является противовирусная терапия (ПВТ) с помощью препаратов препаратом прямого действия, основными мишенями которых являются вирусные белки, необходимые для его размножения (эффективность более 90-95%). Являвшееся до недавнего времени «Золотым стандартом» применение пегилированных интерферонов в сочетании с рибавирином на сегодняшний день не представляет оптимальный выбор по причине низкой эффективности (около 50%) и недостаточно хорошей безопасности.
В некоторых случаях ПВТ не может быть назначена по ряду причин:
- наличие противопоказаний для назначения противовирусных препаратов;
- непереносимость противовирсуных препаратов;
- опыт неудачного лечения противовирсуными препаратами (повторное лечение, как правило, не целесообразно);
- высокая стоимость противовирусных препаратов;
- ожидание доступных/эффективных/безопасных противовирсуных препаратов.
В таких случаях для замедления прогрессирования заболевания в цирроз и рак печени показано назначение лекарственных препаратов, способных уменьшать воспаление и темпы прогрессирования фиброза. Зачастую различные методы лечения гепатита С применяются в совокупности.
Вне зависимости от выбранных противовирусных препараторов врач в обязательном порядке назначает так называемые гепатопротекторы – средства, которые повышают устойчивость печени к патогенным факторам, восстанавливают гепатоциты и их нормальное функционирование. Например, высокой действенностью обладают препараты на основе глицирризиновой кислоты, которая является основным активным компонентом корня солодки.
Источник
Хронические вирусные гепатиты в силу неуклонного прогрессирующего течения с последующим развитием фиброза и цирроза печени представляют актуальную медицинскую и социально-экономическую проблему. Между тем благодаря фундаментальным успехам в молекулярной биологии и генной инженерии, а также разработкам рекомбинантной технологии и схем противовирусной терапии в изучении и лечении хронических вирусных гепатитов наметился прогресс.
Препараты прямого противовирусного действия
Заболеваемость и смертность от хронических диффузных заболеваний печени постоянно увеличиваются. В мире среди всех причин смерти цирроз печени занимает девятое место (шестое место среди лиц трудоспособного возраста) – от 14 до 30 случаев на 100 000 населения. В России этот показатель значительно выше – 60,5 случая на 100 000 населения [1, 2]. Высоким остается риск развития гепатоцеллюлярной карциномы (в 30 раз чаще) у пациентов с фиброзом печени [3]. Оценка степени фиброзных изменений печени при ее поражении – очень важный диагностический этап, поскольку позволяет прогнозировать течение хронического заболевания, проводить отбор пациентов для специфической (противофиброзной) терапии и контролировать эффективность лечения [4]. На протяжении многих лет стандартом диагностики фиброза и цирроза печени у больных хроническими гепатитами различной этиологии остается биопсия печени [5].
Неинвазивные методы диагностики фиброза печени, широко применяемые в настоящее время, подразделяют на три группы:
- прямые (определение биомаркеров фиброза в сыворотке крови больных), в частности визуальные (эластография печени);
- непрямые (с использованием расчетных индексов определения стадий фиброза печени на основании стандартных гематологических и биохимических параметров крови);
- комбинированные (сочетание прямых и непрямых методов).
Согласно данным литературы, высокоинформативными признаны индексы FIB-4, Fibroindex, Fibro Test, Hepascore, Zeng [6, 7].
Фиброгенез – универсальный процесс прогрессирования хронических заболеваний печени, не зависящий от этиологических факторов, связанный с заменой паренхиматозных клеток соединительной тканью с избыточным накоплением продуктов внеклеточного матрикса и тканевых коллагенов. Накопление фибриллообразующих коллагенов в пространстве Диссе приводит к «капилляризации» и нарушению архитектоники печени, что препятствует нормальному обмену веществ между кровью синусоидов и гепатоцитами [8–10].
Долгое время фиброз печени считался необратимым патологическим состоянием. Ключевое значение при антифибротической терапии имеет устранение причины повреждения печени. Имеются данные об обратном развитии фиброза после эффективной терапии гемохроматоза и болезни Вильсона – Коновалова, при аутоиммунном гепатите на фоне иммуносупрессивной терапии, вторичном билиарном циррозе печени после хирургической декомпрессии желчевыводящих путей, неалкогольном стеатогепатите при уменьшении массы тела, алкогольном гепатите при абстиненции. Таким образом, фиброз печени на ранних стадиях развития – процесс обратимый [11, 12].
В настоящее время в отношении хронических диффузных заболеваний печени предусмотрено комплексное разнонаправленное лечение. Выделяют два основных направления – этиотропную терапию, предполагающую подавление патологического возбудителя при поражениях печени вирусной этиологии, и патогенетическую, корректирующую универсальные звенья фиброгенеза печени. В большинстве случаев препараты для устранения этиологического фактора гепатитов являются и антифибротическими средствами.
Фиброз печени на фоне вирусных гепатитов – процесс динамичный, причем как в сторону прогресса, так и регресса, что подтверждает клиническая практика противовирусной терапии.
В ходе многочисленных исследований выявлена корреляция между репликативной активностью вируса хронического гепатита B (ХГВ) и риском развития цирроза печени и гепатоцеллюлярной карциномы при хронической инфекции, вызванной вирусом гепатита B [13]. По данным метаанализа исследований эффективности противовирусной терапии ХГВ, снижение виремии сопровождается регрессом фиброза печени только при подавлении репликативной активности вируса. У пациентов с элиминацией HBeAg (маркер вирусного гепатита B, указывающий на активное размножение вируса в организме) достоверно уменьшается выраженность цирроза печени, гепатоцеллюлярной карциномы и увеличивается выживаемость по сравнению с контрольной группой.
Стойкое подавление репликативной активности вируса при лечении ламивудином также сопровождается значительным улучшением прогноза. В многоцентровом исследовании у больных ХГВ HBeAg с выраженным фиброзом печени на фоне лечения ламивудином снижался риск осложнений (р = 0,047) [14]. Зафиксированы значимое уменьшение выраженности фиброза (по данным эластометрии) и улучшение гистологической картины у 95% больных циррозом печени.
Сходные результаты получены и при изучении других аналогов нуклеозидов. При лечении адефовиром в течение четырех-пяти лет выраженность фиброза печени снизилась у 70% больных HBeAg-негативным ХГВ [13]. В сравнительном исследовании у пациентов с выраженным фиброзом или циррозом печени, получавших телбивудин в течение года, индекс фиброза снижался в 68 и 56% случаев при HBeAg-позитивном и HBeAg-негативном ХГВ соответственно.
При лечении энтекавиром достижение авиремии также ассоциировалось с улучшением гистологической картины печени у больных HBeAg-негативным и HBeAg-позитивным ХГВ, в том числе с ламивудин-резистентными штаммами вируса. В 35–60% случаев уменьшалась выраженность фиброза печени (по данным эластометрии) [13].
Помимо вирус-индуцированного иммуноопосредованного воспаления и некроза ткани печени рассматривают прямое профиброгенное действие вируса гепатита C (Hepatitis C Virus, HCV) при хроническом гепатите C (ХГС). Геном HCV состоит из нескольких участков, которые кодируют различные структурные и неструктурные белки вируса. Белки HCV влияют на внутриклеточные процессы, в том числе активируют различные профиброгенные факторы. Доказано, что эффективная противовирусная терапия уменьшает выраженность фиброза печени у больных ХГС. Стойкий вирусологический ответ ассоциируется с улучшением выживаемости, уменьшением риска развития цирроза печени и гепатоцеллюлярной карциномы.
До недавнего времени золотым стандартом терапии ХГС оставалось сочетание пегилированного интерферона и рибавирина [15]. Эффективность подобной терапии, по данным разных авторов, не превышает 46–51% у больных с 1-м генотипом вируса и 80% у больных с не 1-м генотипом вируса [16]. По данным метаанализа клинических исследований эффективности интерферона/пэгинтерферона альфа-2а и рибавирина у 1013 больных ХГС, индекс фиброза снижался в 25,7% случаев, динамика отсутствовала в 63,6%. Значительное уменьшение фиброза печени зарегистрировано у 33,8% из 198 пациентов с компенсированным циррозом печени (от F4 до F3/F2 в 24,2% случаев до F1 – в 9,6% случаев) [17]. Результаты лечения больных циррозом печени представляют особый интерес, поскольку позволяют обсуждать его возможную обратимость.
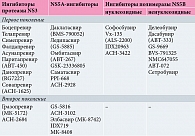
Последние годы на смену стандартной противовирусной терапии пришли более эффективные схемы тройной терапии с применением ингибиторов протеаз, а также безинтерфероновые схемы. Эти схемы включают моно- или комбинации препаратов прямого противовирусного действия (ПППД), характеризующиеся высокой безопасностью и возможностью использования у пациентов с противопоказаниями к применению интерферонов. ПППД нарушают репликацию вируса за счет прямого взаимодействия с вирусными протеинами или нуклеиновыми кислотами [18]. За основу их классификации взяты белки-мишени, с которыми непосредственно взаимодействуют препараты. Исследуемые и одобренные препараты с прямым противовирусным действием представлены в таблице.
Боцепревир и телапревир, продемонстрировавшие эффективность только в отношении 1-го генотипа вируса, характеризуются низким барьером резистентности и высокой частотой развития нежелательных явлений. Симепревир активен в отношении 1-го, 2-го и 4-го генотипов, имеет хороший профиль безопасности, но обладает низким барьером резистентности [19]. NS5A-ингибиторы первого поколения с достаточно высокой эффективностью имеют низкий барьер резистентности. Даклатасвир – препарат с высокой противовирусной активностью против всех генотипов вируса [20]. Гразопревир активен в отношении всех типов вируса, имеет более высокий барьер резистентности по сравнению с препаратами первого поколения.
Софосбувир характеризуется мощной противовирусной активностью в отношении всех генотипов, а также высоким барьером резистентности, незначительным числом описанных нежелательных явлений и низким спектром лекарственного взаимодействия [21].
Источник

